Prove recenti suggeriscono che il fluoro (F) e l’arsenico (As) possano influire negativamente sui punteggi del quoziente intellettivo (QI). Esploriamo l’associazione tra l’esposizione a F e As nell’acqua potabile e l’intelligenza nei bambini. Sono state studiate tre comunità rurali in Messico con livelli contrastanti di F e As nell’acqua potabile:
Il campione finale dello studio era composto da 132 bambini di età compresa tra 6 e 10 anni. Dopo aver controllato i fattori confondenti, è stata osservata un’associazione inversa tra F nelle urine e punteggi di Performance, Verbale e QI completo (valori beta = -13, -15,6, -16,9, rispettivamente). Risultati simili sono stati osservati per F nell’acqua potabile (valori beta = -6,7, -11,2, -10,2, rispettivamente) e As nell’acqua potabile (valori beta = -4,30, -6,40, -6,15, rispettivamente). I valori p per tutti i casi erano < 0,001. È stata osservata un’associazione significativa tra As nelle urine e punteggi di QI completo (beta = -5,72, p = 0,003). Questi dati suggeriscono che i bambini esposti a F o As hanno un rischio maggiore di punteggi di QI ridotti.
GUARDA LA NOSTRA BIO E EFFETTUA UNA DONAZIONE…
GUARDA ANCHE IL FONDAMENTALE DOCUMENTARIO SUL FLUORO DOPPIATO ITALIANO BY LVOGRUPPO.COM IN CUI AL MINUTO 15:00 VIENE CITATO LO STUDIO
L’elevata concentrazione di fluoro (F) o arsenico (As) presenti in natura nell’acqua potabile è un problema mondiale. Molti paesi asiatici e latinoamericani hanno segnalato concentrazioni di F o As spesso superiori ai valori guida dell’Organizzazione Mondiale della Sanità (OMS) di 1,5 mg/L e 10 µg/L, rispettivamente, o ai loro standard nazionali prevalenti 1,2 . In molte comunità degli stati centrali e settentrionali del Messico le persone sono esposte a F e/o As nell’acqua potabile 3,4,5,6 . Secondo i dati dell’Istituto Nazionale di Statistica, Geografia e Informatica (INEGI: http://www.inegi.gob.mx/ , consultati il 03/09/2006), circa 14 milioni di persone vivono in aree a rischio in Messico.
Gli effetti sulla salute umana associati all’esposizione a F (fluorosi scheletrica e dentale ed effetti riproduttivi) o As (cancro della pelle, della vescica e dei polmoni) sono ben documentati 7,8 . Inoltre, la letteratura riporta conseguenze neurologiche associate all’esposizione a F o As. Nei bambini, l’effetto più segnalato riguarda le capacità cognitive, in particolare la riduzione dell’intelligenza 9,10,11,12,13,14,15,16 . Anche in studi con limitazioni metodologiche, la riduzione del quoziente intellettivo (QI) è una conclusione coerente. L’evidenza della neurotossicità di F e As è supportata da studi sugli animali, che mostrano deficit cognitivi associati all’esposizione a F 17 , e cambiamenti comportamentali (attività locomotoria) e apprendimento ritardato sono associati all’esposizione ad As 18 . Finora, gli studi hanno valutato solo l’effetto individuale di F o As sul QI, senza tenere conto del fatto che potrebbero condividere la stessa fonte di esposizione (acqua potabile, carbone ecc.). In Messico molte falde acquifere sono inquinate da F e/o As. Di conseguenza, considerando che è stato dimostrato che entrambi i contaminanti sono neurotossici, l’obiettivo di questo studio era quello di esplorare l’influenza di F e As sul QI nei bambini che vivono in tre aree rurali con livelli contrastanti di F e As.
Popolazione dello studio
Tutti i bambini che frequentano la prima, la seconda e la terza elementare nelle scuole pubbliche di tre aree rurali del Messico sono stati sottoposti a screening per l’idoneità allo studio tramite interviste di persona (n = 480). Le domande includevano l’età del bambino, il periodo di residenza e l’indirizzo. L’ubicazione delle comunità è mostrata inFigura 1. Moctezuma e Salitral si trovano nella regione nord-occidentale dello stato di San Luis Potosí, mentre 5 de Febrero si trova nella regione centrale dello stato di Durango.
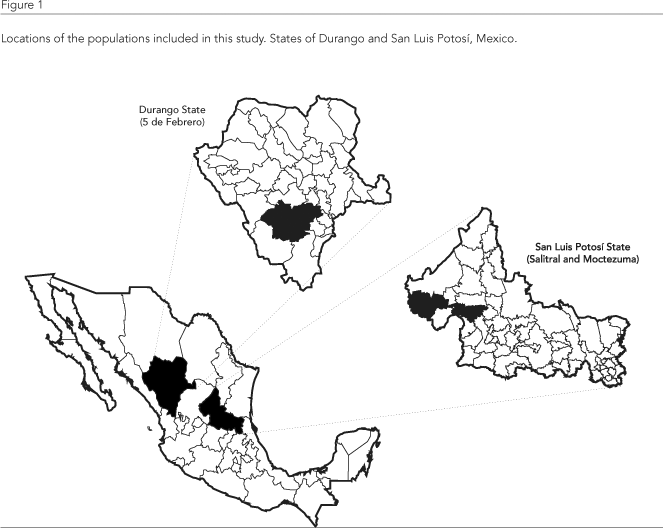
Le tre comunità selezionate erano simili per popolazione e caratteristiche demografiche generali. I bambini residenti nella zona dalla nascita e di età compresa tra 6 e 10 anni al momento dello studio erano idonei a partecipare (n = 308). Tra questi, 155 bambini sono stati selezionati casualmente per la partecipazione allo studio. Il tasso di risposta è stato dell’85%. Non sono state osservate differenze significative in termini di età, proporzione di genere o periodo di residenza tra i partecipanti allo studio e i non partecipanti.
Valutazione neuropsicologica
Il profilo neuropsicologico è stato valutato utilizzando la Wechsler Intelligence Scale for Children – Versione Messicana Riveduta (WISC-RM). Tutti i test sono stati somministrati a scuola da un neuropsicologo qualificato, all’oscuro dei livelli di urina o acqua dei partecipanti (F o As). È stata somministrata una versione standardizzata della WISC-RM 19 . A ciascun bambino sono stati somministrati dieci diversi subtest, cinque prevalentemente verbali (informazione, somiglianze, aritmetica, vocabolario e comprensione) e cinque prevalentemente orientati alla prestazione (completamento di immagini, disposizione di immagini, progettazione di blocchi, assemblaggio di oggetti e codifica). I punteggi grezzi sono stati aggiustati per età e sommati per ottenere misure convenzionali di scale di QI complete, verbali e di prestazione.
Analisi ambientale e biologica
Campioni di acqua di rubinetto e di acqua in bottiglia (ove disponibili) sono stati raccolti in bottiglie di polietilene presso il domicilio di ciascun bambino lo stesso giorno del monitoraggio biologico. I livelli di F sono stati quantificati aggiungendo tampone TISAB ai campioni con un elettrodo a ioni specifici sensibile appena prima dell’analisi. Come controllo di qualità interno, è stato analizzato il materiale di riferimento standard primario (NIST SRM 3183: Fluoride Anion Standard Solution; National Institute of Standards and Technology, Stati Uniti). L’accuratezza è stata del 98±3%. L’acqua As è stata analizzata con uno spettrofotometro ad assorbimento atomico con sistema a idruri (Perkin-Elmer, modello Aanalyst 100, Wellesley, Stati Uniti). Per il controllo di qualità sono stati utilizzati gli elementi in tracce nell’acqua naturale (NIST SRM 1640; National Institute of Standards and Technology, Stati Uniti). L’accuratezza è stata del 99±2%.
I campioni di urina sono stati raccolti in flaconi di polietilene lo stesso giorno delle valutazioni neuropsicologiche. Il Fluoruro nelle urine è stato analizzato secondo il Metodo 8308 ( Fluoro nelle urine ) del National Institute of Occupational Safety and Health 20 . Per il controllo di qualità, è stato analizzato lo standard di riferimento Fluoro nelle urine liofilizzate (NIST SRM 2671a; National Institute of Standards and Technology, Stati Uniti). L’accuratezza è stata del 97±6%. Per l’As, i campioni di urina sono stati digeriti a 70°C con una miscela di HNO3 : HCIO4 1 :6. La soluzione è stata ridotta per 5 minuti a 80°C con KI al 10%, acido ascorbico al 5% e HCl 21 . L’As nelle urine è stato analizzato utilizzando lo spettrofotometro ad assorbimento atomico con sistema a idruri (Perkin-Elmer, modello Aanalyst 100, Wellesley, Stati Uniti). Per il controllo di qualità, è stato analizzato lo standard di riferimento “Metalli tossici nelle urine liofilizzate” (NIST SRM 2670; National Institute of Standards and Technology, Stati Uniti). L’accuratezza è stata del 98±4%. I livelli di F e As nelle urine sono stati aggiustati per i livelli di creatinina urinaria, analizzati con un kit diagnostico colorimetrico Bayer (Sera-Pak Plus).
Per analizzare l’esposizione al piombo (Pb), i campioni di sangue sono stati ottenuti tramite puntura venosa utilizzando provette Vacutainer senza piombo contenenti EDTA come anticoagulante e sono stati conservati a 4 °C fino all’analisi. Il Pb nel sangue è stato analizzato con un modificatore di matrice (idrogenofosfato di diammonio-Triton X-100 in presenza di acido nitrico allo 0,2%), seguendo il metodo Subramanian 22. Tutte le analisi sono state eseguite in duplicato con uno spettrofotometro ad assorbimento atomico Perkin-Elmer 3110 utilizzando un fornetto in grafite. Per tutte le analisi è stata utilizzata acqua distillata deionizzata. Vetreria e altri materiali sono stati immersi in acido nitrico al 10%, risciacquati con acqua bidistillata e asciugati prima dell’uso. Al momento dell’analisi, il nostro laboratorio ha partecipato al programma di test di competenza per il piombo nel sangue condotto dai Centers for Disease Control and Prevention (CDC).
Valutazione dello stato nutrizionale e socioeconomico
Altezza e peso per età, come indici di denutrizione cronica, sono stati calcolati utilizzando tabelle di riferimento del National Center for Health Statistics (NCHS) statunitense 23 . Gli Z-score sono stati calcolati con il programma Epi Info (Centers for Disease Control and Prevention, Atlanta, Stati Uniti). Come indicatore dello stato del ferro, la percentuale di saturazione della transferrina è stata calcolata dividendo la concentrazione di ferro sierico (SI) per la capacità totale di legare il ferro (TIBC) e moltiplicando per 100. SI e TIBC sono stati misurati con un kit diagnostico colorimetrico Bayer (Serapack, Bayer). Per il controllo di qualità, sono stati analizzati campioni di siero Seracheck (Serapack, Bayer). L’accuratezza per SI e TIBC è stata rispettivamente del 95±5% e del 92±4%.
Lo status socioeconomico è stato calcolato secondo l’indice Bronfman. Le variabili predittive erano: materiale di pavimentazione della casa, affollamento, disponibilità di acqua potabile, sistema di drenaggio e livello di istruzione del padre24 . Ulteriori informazioni sul tipo di acqua utilizzata per cucinare (del rubinetto o in bottiglia), condizioni di salute, ecc. sono state raccolte tramite questionario.
Analisi statistica
Questo studio ha testato l’ipotesi di un’associazione tra l’esposizione a F e As (misurata nelle urine e nell’acqua) e i punteggi di QI (Performance, Verbale e Completo). È stata condotta un’analisi bivariata per analizzare le differenze nelle medie o nelle proporzioni tra le tre comunità al fine di confrontare esposizioni e covariate potenzialmente correlate all’effetto di interesse (ANOVA seguita da test pos hoc, quando necessario, e test del chi-quadrato). Inizialmente, abbiamo modellato regressioni lineari semplici per F o As nelle urine o nell’acqua. Successivamente, abbiamo modellato regressioni lineari multiple includendo le seguenti variabili: F o As nelle urine o nell’acqua (da sole e interazione F-As), Pb nel sangue, istruzione della madre, stato socioeconomico, punteggio z altezza per età e saturazione della transferrina. Le variabili di esposizione sono state trattate come continue e tutti i dati (n = 132) sono stati inclusi nei modelli di regressione. La logica di questa procedura è stata la seguente: all’inizio dello studio, abbiamo selezionato le tre comunità in base alle loro concentrazioni di F e As nell’acqua potabile. Tuttavia, analizzando i valori di F e As nelle urine, abbiamo osservato che i bambini della comunità del 5 febbraio (con la più alta esposizione) presentavano livelli di F o As nelle urine persino inferiori a quelli dei bambini di Salitral (con esposizione media). Questa osservazione è spiegata dall’accesso ad acqua in bottiglia con livelli inferiori di F o As nella comunità del 5 febbraio. Alcune persone in questa popolazione utilizzavano l’acqua del rubinetto per cucinare e l’acqua in bottiglia per bere, una pratica che contribuiva a ridurre l’esposizione. Poiché i livelli di F e As nelle urine sono indicatori migliori di esposizione (perché integrano tutte le fonti) e i dati di F e As nelle urine delle tre comunità seguivano una distribuzione unimodale, abbiamo previsto che gli esiti di interesse, data la variabile di esposizione (F o As nelle urine), sarebbero stati continui per l’intera popolazione. Il livello di significatività è stato fissato a 0,05. Tutte le analisi sono state eseguite con SPSS versione 12.0 (SPSS Inc., Chicago, Stati Uniti).
Risultati
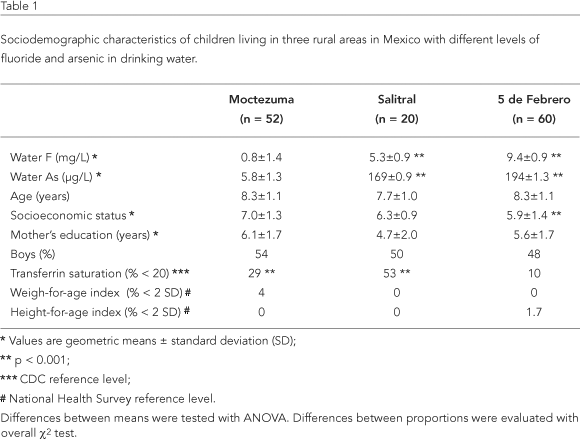
Le caratteristiche sociodemografiche dei bambini delle tre comunità sono presentate inTabella 1. Confrontando le concentrazioni medie di F e As nell’acqua, sono state osservate differenze statisticamente significative tra Moctezuma e Salitral e 5 de Febrero (p < 0,001). I livelli medi di F nell’acqua erano rispettivamente quasi 3,5 e 6 volte superiori ai limiti OMS in Salitral e 5 de Febrero. I livelli medi di As nell’acqua erano rispettivamente 17 e 19 volte superiori ai limiti OMS in Salitral e 5 de Febrero. Non sono state osservate differenze statisticamente significative nell’età dei partecipanti, nel livello di istruzione della madre, nella proporzione di genere o nei punteggi z (peso per età e altezza per età) tra le tre comunità. Tuttavia, vi erano differenze statisticamente significative (p < 0,01) nello stato socioeconomico e nella proporzione di bambini con saturazione della transferrina inferiore al 20%.
Le tre comunità selezionate erano simili per popolazione e caratteristiche demografiche generali. I bambini residenti nella zona dalla nascita e di età compresa tra 6 e 10 anni al momento dello studio erano idonei a partecipare (n = 308). Tra questi, 155 bambini sono stati selezionati casualmente per la partecipazione allo studio. Il tasso di risposta è stato dell’85%. Non sono state osservate differenze significative in termini di età, proporzione di genere o periodo di residenza tra i partecipanti allo studio e i non partecipanti.
Valutazione neuropsicologica
Il profilo neuropsicologico è stato valutato utilizzando la Wechsler Intelligence Scale for Children – Versione Messicana Riveduta (WISC-RM). Tutti i test sono stati somministrati a scuola da un neuropsicologo qualificato, all’oscuro dei livelli di urina o acqua dei partecipanti (F o As). È stata somministrata una versione standardizzata della WISC-RM 19 . A ciascun bambino sono stati somministrati dieci diversi subtest, cinque prevalentemente verbali (informazione, somiglianze, aritmetica, vocabolario e comprensione) e cinque prevalentemente orientati alla prestazione (completamento di immagini, disposizione di immagini, progettazione di blocchi, assemblaggio di oggetti e codifica). I punteggi grezzi sono stati aggiustati per età e sommati per ottenere misure convenzionali di scale di QI complete, verbali e di prestazione.
Analisi ambientale e biologica
Campioni di acqua di rubinetto e di acqua in bottiglia (ove disponibili) sono stati raccolti in bottiglie di polietilene presso il domicilio di ciascun bambino lo stesso giorno del monitoraggio biologico. I livelli di F sono stati quantificati aggiungendo tampone TISAB ai campioni con un elettrodo a ioni specifici sensibile appena prima dell’analisi. Come controllo di qualità interno, è stato analizzato il materiale di riferimento standard primario (NIST SRM 3183: Fluoride Anion Standard Solution; National Institute of Standards and Technology, Stati Uniti). L’accuratezza è stata del 98±3%. L’acqua As è stata analizzata con uno spettrofotometro ad assorbimento atomico con sistema a idruri (Perkin-Elmer, modello Aanalyst 100, Wellesley, Stati Uniti). Per il controllo di qualità sono stati utilizzati gli elementi in tracce nell’acqua naturale (NIST SRM 1640; National Institute of Standards and Technology, Stati Uniti). L’accuratezza è stata del 99±2%.
I campioni di urina sono stati raccolti in flaconi di polietilene lo stesso giorno delle valutazioni neuropsicologiche. Il Fluoruro nelle urine è stato analizzato secondo il Metodo 8308 ( Fluoro nelle urine ) del National Institute of Occupational Safety and Health 20 . Per il controllo di qualità, è stato analizzato lo standard di riferimento Fluoro nelle urine liofilizzate (NIST SRM 2671a; National Institute of Standards and Technology, Stati Uniti). L’accuratezza è stata del 97±6%. Per l’As, i campioni di urina sono stati digeriti a 70°C con una miscela di HNO3 : HCIO4 1 :6. La soluzione è stata ridotta per 5 minuti a 80°C con KI al 10%, acido ascorbico al 5% e HCl 21 . L’As nelle urine è stato analizzato utilizzando lo spettrofotometro ad assorbimento atomico con sistema a idruri (Perkin-Elmer, modello Aanalyst 100, Wellesley, Stati Uniti). Per il controllo di qualità, è stato analizzato lo standard di riferimento “Metalli tossici nelle urine liofilizzate” (NIST SRM 2670; National Institute of Standards and Technology, Stati Uniti). L’accuratezza è stata del 98±4%. I livelli di F e As nelle urine sono stati aggiustati per i livelli di creatinina urinaria, analizzati con un kit diagnostico colorimetrico Bayer (Sera-Pak Plus).
Per analizzare l’esposizione al piombo (Pb), i campioni di sangue sono stati ottenuti tramite puntura venosa utilizzando provette Vacutainer senza piombo contenenti EDTA come anticoagulante e sono stati conservati a 4 °C fino all’analisi. Il Pb nel sangue è stato analizzato con un modificatore di matrice (idrogenofosfato di diammonio-Triton X-100 in presenza di acido nitrico allo 0,2%), seguendo il metodo Subramanian 22. Tutte le analisi sono state eseguite in duplicato con uno spettrofotometro ad assorbimento atomico Perkin-Elmer 3110 utilizzando un fornetto in grafite. Per tutte le analisi è stata utilizzata acqua distillata deionizzata. Vetreria e altri materiali sono stati immersi in acido nitrico al 10%, risciacquati con acqua bidistillata e asciugati prima dell’uso. Al momento dell’analisi, il nostro laboratorio ha partecipato al programma di test di competenza per il piombo nel sangue condotto dai Centers for Disease Control and Prevention (CDC).
Valutazione dello stato nutrizionale e socioeconomico
Altezza e peso per età, come indici di denutrizione cronica, sono stati calcolati utilizzando tabelle di riferimento del National Center for Health Statistics (NCHS) statunitense 23 . Gli Z-score sono stati calcolati con il programma Epi Info (Centers for Disease Control and Prevention, Atlanta, Stati Uniti). Come indicatore dello stato del ferro, la percentuale di saturazione della transferrina è stata calcolata dividendo la concentrazione di ferro sierico (SI) per la capacità totale di legare il ferro (TIBC) e moltiplicando per 100. SI e TIBC sono stati misurati con un kit diagnostico colorimetrico Bayer (Serapack, Bayer). Per il controllo di qualità, sono stati analizzati campioni di siero Seracheck (Serapack, Bayer). L’accuratezza per SI e TIBC è stata rispettivamente del 95±5% e del 92±4%.
Lo status socioeconomico è stato calcolato secondo l’indice Bronfman. Le variabili predittive erano: materiale di pavimentazione della casa, affollamento, disponibilità di acqua potabile, sistema di drenaggio e livello di istruzione del padre24 . Ulteriori informazioni sul tipo di acqua utilizzata per cucinare (del rubinetto o in bottiglia), condizioni di salute, ecc. sono state raccolte tramite questionario.
Analisi statistica
Questo studio ha testato l’ipotesi di un’associazione tra l’esposizione a F e As (misurata nelle urine e nell’acqua) e i punteggi di QI (Performance, Verbale e Completo). È stata condotta un’analisi bivariata per analizzare le differenze nelle medie o nelle proporzioni tra le tre comunità al fine di confrontare esposizioni e covariate potenzialmente correlate all’effetto di interesse (ANOVA seguita da test pos hoc, quando necessario, e test del chi-quadrato). Inizialmente, abbiamo modellato regressioni lineari semplici per F o As nelle urine o nell’acqua. Successivamente, abbiamo modellato regressioni lineari multiple includendo le seguenti variabili: F o As nelle urine o nell’acqua (da sole e interazione F-As), Pb nel sangue, istruzione della madre, stato socioeconomico, punteggio z altezza per età e saturazione della transferrina. Le variabili di esposizione sono state trattate come continue e tutti i dati (n = 132) sono stati inclusi nei modelli di regressione. La logica di questa procedura è stata la seguente: all’inizio dello studio, abbiamo selezionato le tre comunità in base alle loro concentrazioni di F e As nell’acqua potabile. Tuttavia, analizzando i valori di F e As nelle urine, abbiamo osservato che i bambini della comunità del 5 febbraio (con la più alta esposizione) presentavano livelli di F o As nelle urine persino inferiori a quelli dei bambini di Salitral (con esposizione media). Questa osservazione è spiegata dall’accesso ad acqua in bottiglia con livelli inferiori di F o As nella comunità del 5 febbraio. Alcune persone in questa popolazione utilizzavano l’acqua del rubinetto per cucinare e l’acqua in bottiglia per bere, una pratica che contribuiva a ridurre l’esposizione. Poiché i livelli di F e As nelle urine sono indicatori migliori di esposizione (perché integrano tutte le fonti) e i dati di F e As nelle urine delle tre comunità seguivano una distribuzione unimodale, abbiamo previsto che gli esiti di interesse, data la variabile di esposizione (F o As nelle urine), sarebbero stati continui per l’intera popolazione. Il livello di significatività è stato fissato a 0,05. Tutte le analisi sono state eseguite con SPSS versione 12.0 (SPSS Inc., Chicago, Stati Uniti).
Risultati
Le caratteristiche sociodemografiche dei bambini delle tre comunità sono presentate inTabella 1. Confrontando le concentrazioni medie di F e As nell’acqua, sono state osservate differenze statisticamente significative tra Moctezuma e Salitral e 5 de Febrero (p < 0,001). I livelli medi di F nell’acqua erano rispettivamente quasi 3,5 e 6 volte superiori ai limiti OMS in Salitral e 5 de Febrero. I livelli medi di As nell’acqua erano rispettivamente 17 e 19 volte superiori ai limiti OMS in Salitral e 5 de Febrero. Non sono state osservate differenze statisticamente significative nell’età dei partecipanti, nel livello di istruzione della madre, nella proporzione di genere o nei punteggi z (peso per età e altezza per età) tra le tre comunità. Tuttavia, vi erano differenze statisticamente significative (p < 0,01) nello stato socioeconomico e nella proporzione di bambini con saturazione della transferrina inferiore al 20%.
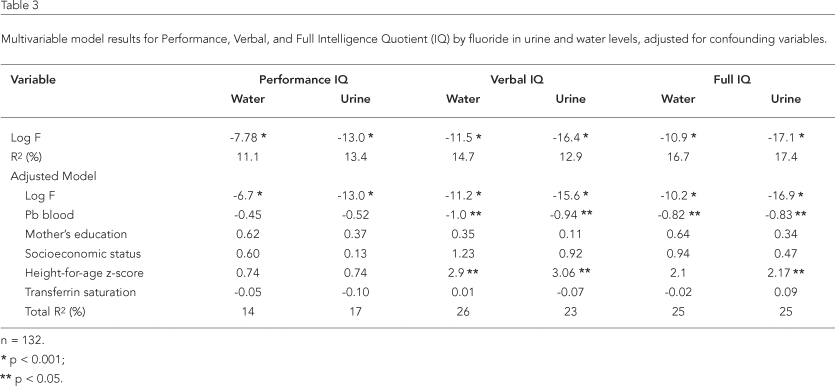
Per testare l’associazione tra F nelle urine o F nell’acqua e punteggi di QI (Prestazioni, Verbale e Completo), sono stati calcolati modelli di regressione multipla. I risultati sono mostrati in
Tabella 3. Per F nelle urine, i coefficienti (valori b) per i punteggi di Performance, Verbale e QI completo, aggiustati per Pb nel sangue, stato socioeconomico, istruzione della madre, punteggio z altezza per età e saturazione della transferrina, erano rispettivamente -13,0, -15,6 e -16,9 (tutti i valori p < 0,001). Per F nell’acqua, i coefficienti (valori b), anch’essi aggiustati per gli stessi fattori confondenti menzionati sopra, erano rispettivamente -6,7, -11,2 e -10,2 (tutti i valori p < 0,001).
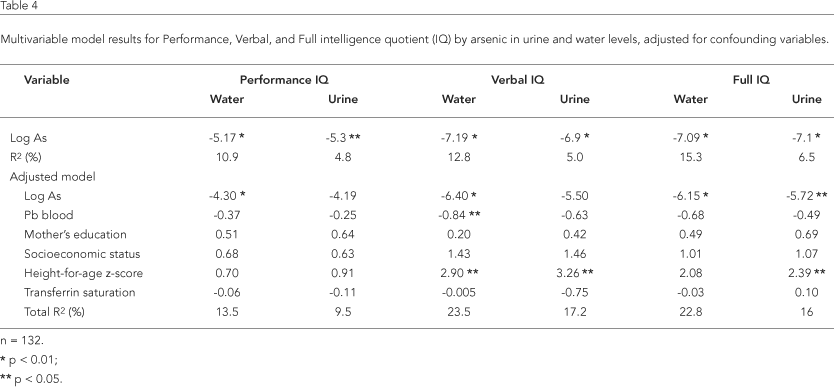
Poiché i dati di esposizione sono mostrati in
Tabella 4. Dopo aver corretto per i fattori confondenti (Pb nel sangue, stato socioeconomico, istruzione della madre, punteggio z altezza per età e saturazione della transferrina), l’As nelle urine è risultato inversamente associato ai punteggi del QI completo (b = -5,72, p = 0,003). Abbiamo anche osservato relazioni inverse per i punteggi del QI di prestazione e verbale, tuttavia non erano così significative (b = -4,19, p = 0,08; b = -5,50, p = 0,06, rispettivamente). Dopo aver corretto per i fattori confondenti, l’As in acqua ha mostrato associazioni inverse con i punteggi del QI di prestazione, verbale e completo (valori b = -4,30, -6,40 e -6,15, rispettivamente; tutti i valori p < 0,001).
Abbiamo scoperto che l’esposizione a F nelle urine era associata a una riduzione dei punteggi di Performance, Verbale e QI completo prima e dopo la correzione per i fattori confondenti (valori b = rispettivamente -13,0, -15,6 e -16,9; tutti i valori p < 0,001). Lo stesso andamento è stato osservato nei modelli con F in acqua come variabile di esposizione (valori b = rispettivamente -6,7, -11,2 e -10,2; tutti i valori p < 0,001).
L’impatto del F sul QI è stato riportato in diversi studi da ricercatori cinesi. In uno studio condotto nel 1995, i punteggi medi del QI sono stati confrontati tra bambini che vivevano in aree con diversa prevalenza di fluorosi dentale. Il punteggio medio del QI dei residenti nell’area con fluorosi grave (F urinario medio di 2,69 mg/L e indice di fluorosi dentale di 3,2) era di 80,3 punti, mentre nell’area con fluorosi bassa (F urinario medio di 1,02 mg/L e indice di fluorosi dentale < 0,4) era di 89,9 punti. La differenza tra i gruppi era statisticamente significativa 9 . Un altro studio ha confrontato i punteggi del QI di bambini che vivevano in due villaggi con diversi livelli medi di F nell’acqua (4,12 mg/L contro 0,91 mg/L). Sebbene gli autori non abbiano controllato i fattori confondenti e non abbiano misurato F nelle urine, riferiscono che il QI medio dei bambini nell’area ad alto contenuto di fluoro (97,69 punti) era significativamente inferiore rispetto all’area a basso contenuto di fluoro (105,21 punti) 10 . I due studi appena menzionati hanno utilizzato il test di Rui Wen per misurare il QI. Nel 2000, un altro rapporto ha confrontato i punteggi del QI di bambini provenienti da due aree in Cina (F nell’acqua potabile 3,15 mg/L contro 0,37 mg/L). Hanno anche misurato la concentrazione di F nelle urine (F urinario medio di 4,99 mg/L contro 1,43 mg/L). Il punteggio medio del QI per i bambini nell’area più esposta (92,2 punti) era inferiore rispetto ai bambini che vivevano nell’area meno esposta (103,05 punti) 11 . Infine, un altro studio cinese ha valutato 118 bambini di due villaggi. Il punteggio medio del QI per l’area ad alto contenuto di fluoro (92,02 punti; F in acqua 2,47 mg/L) era significativamente inferiore rispetto all’area a basso contenuto di fluoro (100,41 punti; F in acqua 0,36 mg/L). In questo studio, è stata riportata una lieve associazione inversa tra F nelle urine e punteggi del QI (r = -0,17, p = 0,003). Non è stato effettuato alcun aggiustamento per i fattori confondenti 12 . Nonostante diverse carenze (mancanza di aggiustamento per i fattori confondenti, assenza di marcatori biologici, nessuna quantificazione di altri potenziali inquinanti neurotossici, ecc.), tutti questi studi suggeriscono che F ha un impatto negativo sui punteggi del QI, con riduzioni osservate del QI che vanno da 8 a 11 punti tra bambini esposti e non esposti.
I livelli di esposizione dei bambini al F nel presente studio erano più elevati rispetto agli studi cinesi. Il F nell’acqua potabile era 3,5 e 6 volte superiore ai valori di riferimento dell’OMS per due delle comunità. In media, il valore di F nelle urine era di 6,6 mg/g crt. Inoltre, oltre il 50% dei bambini nelle due aree ad alta esposizione presentava As nelle urine superiore al valore di riferimento del CDC di 50 µg/g crt. L’effetto individuale del F nelle urine indicava che per ogni mg di aumento di F nelle urine ci si poteva aspettare una diminuzione di 1,7 punti nel QI completo. La percentuale attribuibile al solo F nelle urine era superiore del 17% rispetto al contributo di altri fattori misurati. La varianza nel QI completo spiegata nel modello aggiustato era del 25%. Per quanto riguarda l’As nelle urine, abbiamo osservato un’associazione inversa con i punteggi del QI completo (b = -5,72, p = 0,003). Abbiamo anche osservato una relazione inversa tra i punteggi di Performance e QI verbale, sebbene con minore significatività (rispettivamente b = -4,19, p = 0,08; b = -5,50, p = 0,06). Abbiamo inoltre scoperto che l’As in acqua era inversamente correlato con i punteggi di Performance, QI verbale e QI completo (valori b = -4,30, -6,40 e -6,15; tutti i valori p < 0,001). Rispetto a F, l’effetto attribuibile all’As era minore.
Esistono anche dati in letteratura a supporto del possibile ruolo dell’As nella riduzione del QI. In uno studio condotto dal nostro gruppo, è stata osservata un’associazione negativa tra As urinario (media = 62,9 µg/g crt) e punteggi di QI verbale (r = -0,43, p = 0,008) e completo (r = -0,33, p = 0,04), dopo aggiustamento per fattori confondenti, in bambini che vivono intorno a un complesso di fonderia 15 . Un altro studio condotto in Bangladesh ha riportato un’associazione inversa tra As nell’acqua e punteggi di QI di prestazione e completo (valori b = -1,45 e -1,64, rispettivamente; p < 0,001 in entrambi i casi) 13 .
Gli effetti avversi di F e As sul sistema nervoso centrale umano sono supportati da dati sperimentali. Quando F attraversa la barriera ematoencefalica, la barriera ematoencefalica, si accumula nel cervello, inducendo alterazioni strutturali e cognitive nel sistema nervoso centrale 17,25 . I ratti esposti a F nell’acqua potabile allo svezzamento presentavano livelli elevati di fluoro in 6 su 7 regioni cerebrali e livelli di fluoro plasmatico da 7 a 42 volte superiori a quelli riscontrati negli animali di controllo. Questi elevati livelli di F nel plasma e nel cervello erano associati ad alterazioni comportamentali, come deficit cognitivi 17 . Sono stati segnalati deficit di apprendimento in un compito di alternanza ritardata e alterazioni in un compito di apprendimento spaziale per i gruppi esposti ad As rispetto ai gruppi di controllo 18,26,27 .
Il disegno del presente studio ha precluso la verifica statistica dell’interazione tra F e As. Tuttavia, in uno studio precedente condotto dal nostro gruppo di ricerca nella città di San Luis Potosí, i punteggi del QI sono stati valutati utilizzando WISC-RM in una popolazione di bambini esposti a F nell’acqua potabile (valori compresi tra 1,5 e 3 mg/L). I livelli medi di F e As nelle urine erano rispettivamente di 4,3±1,5 mg/g crt e 41±1,5 µg/g crt. Questo studio non ha dimostrato alcun effetto sui punteggi del QI, ma ha mostrato una relazione positiva tra F nelle urine e tempo di reazione (r = 0,28, p = 0,04) e una relazione inversa tra F nelle urine e punteggi di organizzazione visuo-spaziale (r = -0,27, p = 0,05) 16 . Questi dati possono supportare l’ipotesi che l’esposizione a entrambe le sostanze tossiche possa peggiorare le prestazioni dei bambini nei test neuropsicologici e indicano quindi la necessità di ulteriori indagini.
I nostri risultati relativi al Pb nel sangue indicano che i deficit osservati nei punteggi di QI non possono essere attribuiti all’esposizione al Pb. Quando il Pb nel sangue è stato incluso nel modello aggiustato per F nelle urine, la correlazione è rimasta significativa con solo un piccolo contributo alla varianza, mentre nel modello aggiustato per As nelle urine non è stata significativa.
Sebbene si tratti di uno studio trasversale e i livelli di F e As nelle urine siano biomarcatori di esposizione recente, disponiamo di dati sulle esposizioni passate per due delle comunità incluse nello studio. A 5 de Febrero, i livelli di F nell’acqua riportati dal 1997 al 2004 variavano da 8,7 mg/L a 10,2 mg/L. I valori di As nello stesso periodo variavano da 130 µg/L a 215 µg/L. I livelli di entrambi gli inquinanti nell’acqua erano superiori agli standard OMS. I dati relativi a Salitral del 2002 e del 2003 mostrano che i livelli di F erano in media di 5,3 mg/L e quelli di As variavano da 141 µg/L a 150 µg/L. Sebbene non disponiamo di dati storici sui livelli di F nell’acqua di Moctezuma, possiamo supporre che fossero simili ai nostri risultati poiché nessuno dei bambini presentava fluorosi dentale, un indicatore di esposizione cronica a F. Sulla base di queste informazioni e poiché F e As nell’acqua erano altamente correlati (r = 0,86, p < 0,001), supponiamo che lo scenario di esposizione non sia cambiato nel tempo e che l’esposizione attuale a F o As nell’acqua potabile possa essere utilizzata come indicatore dell’esposizione passata. Alcuni degli effetti sulle disfunzioni cerebrali sono stati osservati anni dopo l’esposizione. I bambini nel campione dello studio sono stati esposti dalla nascita e sono rimasti esposti fino alla raccolta dei dati dello studio. I livelli biologici di F e As sono chiaramente indicatori migliori dell’esposizione effettiva perché integrano tutte le fonti e le variazioni di esposizione. Il 53% delle persone del 5 de Febrero ha dichiarato di utilizzare acqua in bottiglia per bere ma non per cucinare, mentre questa percentuale era del 27% per la comunità di Salitral.
In conclusione, i dati di questa ricerca supportano la conclusione che F e As presenti nell’acqua potabile abbiano un potenziale effetto neurotossico nei bambini. È urgente attuare misure di sanità pubblica per ridurre i livelli di esposizione. Milioni di persone in tutto il mondo sono esposte a questi inquinanti e sono quindi potenzialmente a rischio di effetti negativi sull’intelligenza. Questo rischio può aumentare in presenza di altri fattori che influenzano lo sviluppo del sistema nervoso centrale, come la malnutrizione e la povertà. Il rischio è particolarmente elevato per i bambini, il cui cervello è particolarmente sensibile alle tossine ambientali. Inoltre, sarebbe opportuno riesaminare i benefici del F, dati i rischi per la salute documentati.
Collaboratori
D. Rocha-Amador ha partecipato al campionamento di urine e acqua, alla somministrazione del questionario, alla quantificazione del fluoro in acqua e urina, alla quantificazione della creatinina nelle urine, alla quantificazione dei livelli di ferro nel sangue, allo sviluppo del database e all’analisi dei dati. L. Carrizales ha partecipato al campionamento del sangue, alla quantificazione del piombo nel sangue e dell’arsenico in urina e acqua, e alla somministrazione del questionario. ME Navarro e R. Morales hanno contribuito all’applicazione e alla valutazione dei test neuropsicologici. J. Calderón è stato responsabile della progettazione del progetto, dell’approvvigionamento delle risorse finanziarie, dell’analisi statistica dei dati e della stesura finale dell’articolo.
Ringraziamenti
Questo lavoro è stato sostenuto dal Consejo Nacional de Ciencia y Tecnología – CONACYT (Proyect J 37584-M). Siamo grati al Dr. Díaz-Barriga per gli utili commenti sul manoscritto.
Inviato il 02/05/2006
Versione finale ripresentata l’11/09/2006
Approvato il 10/10/2006
GUARDA LA NOSTRA BIO E EFFETTUA UNA DONAZIONE…
Riferimenti
- 1. Organizzazione Mondiale della Sanità. Linee guida per la qualità dell’acqua potabile. v. 1: raccomandazioni. http://www.who.int/water_sanitation_health/dwq/gdwq3/en/ (consultato il 03/09/2006).
- 2. Messico. Modifica alla Norma Ufficiale Messicana NOM-127-SSA1-1994. Salud ambiental, agua para uso y consumo humano. Limiti di qualità e trattamenti consentiti affinché sia necessario sommergere l’acqua per la potabilizzazione. Diario Ufficiale 2000; Prima sezione, pag. 48-54.
- 3. Smedley PL, Kinninburg DG. Una revisione della fonte, del comportamento e della distribuzione dell’arsenico nelle acque naturali. Applied Geochemistry 2002; 17:517-68.
- 4. Méndez M, Armienta MA. Distribuzione della fase dell’arsenico negli sterili della miniera di Zimapán, Messico. Geofísica Internacional 2003; 42:131-40.
- 5. Trejo R, Alarcón MT, Martínez Y, Romero P, Salvador J. Niveles de fluoruros en el agua de los pozos de la ciudad de Durango. Ingeniería Hidráulica en México 1997; 12:51-7.
- 6. Díaz-Barriga F, Leyva R, Quistián J, Loyola-Rodríguez JP, Pozos A, Grimaldo M. Fluorosi endemica a San Luis Potosi, Messico. IV. Fonti di esposizione al fluoro. Fluoruro 1997; 30:219-22.
- 7. Centers for Disease Control and Prevention. Rassegna di “benefici e rischi” del fluoro. Washington DC: Dipartimento della Salute e dei Servizi Umani degli Stati Uniti; 1991.
- 8. Yoshida T, Hiroshi Y, Fan Sun G. Effetti cronici sulla salute nelle persone esposte all’arsenico tramite l’acqua potabile: relazione dose-risposta in una revisione. Toxicol Appl Pharmacol 2004; 198:243-52.
- 9. Li XS, Zhi JL, Gao RO. Effetto dell’esposizione al fluoro sull’intelligenza nei bambini. Fluoride 1995; 28:189-92.
- 10. Zhao LB, Liang GH, Zhang DN, Wu XR. Effetto di un’alimentazione idrica ad alto contenuto di fluoro sull’intelligenza dei bambini. Fluoride 1996; 29:190-2.
- 11. Lu Y, Sun ZR, Wu LN, Wang X, Lu W, Liu SS. Effetti dell’acqua ad alto contenuto di fluoro sull’intelligenza nei bambini. Fluoride 2000; 33:74-8.
- 12. Xiang Q, Liang Y, Chen L, Wang C, Chen B, Zhou M. Effetti del fluoro nell’acqua potabile sull’intelligenza dei bambini. Fluoride 2003; 36:84-94.
- 13. Wasserman GA, Liu X, Parvez F, Ahsan H, Factor-Litvak P, van Geen A, et al. Esposizione all’arsenico nell’acqua e funzione intellettiva dei bambini ad Araihazar, Bangladesh. Environ Health Perspect 2004; 112:1329-33.
- 14. Tsai SY, Chou HY, The HW, Chen CM, Chen CJ. Gli effetti dell’esposizione cronica all’arsenico presente nell’acqua potabile sullo sviluppo neurocomportamentale nell’adolescenza. Neurotoxicology 2003; 24:747-53.
- 15. Calderón J, Navarro ME, Jiménez-Capdeville ME, Santos-Díaz MA, Golden A, Rodríguez-Leyva I, et al. Esposizione all’arsenico e al piombo e sviluppo neuropsicologico nei bambini messicani. Ricerca sull’ambiente 2001; 85:69-76.
- 16. Calderón J, Machado B, Navarro ME, Carrizales L, Díaz-Barriga F. Influenza del fluoro sul tempo di reazione e sull’organizzazione visuospaziale nei bambini. Epidemiologia 2001; 11:S153.
- 17. Mullenix JP, Denbesten PK, Schunior A, Kernan WJ. Neurotossicità del fluoruro di sodio nei ratti. Neurotoxicol Teratol 1995; 17:169-77.
- 18. Rodriguez VM, Jímenez-Capdville ME, Giordano M. Gli effetti dell’esposizione all’arsenico sul sistema nervoso. Toxicol Lett 2003; 145:1-18.
- 19. Gómez-Palacio M, Padilla E, Roll S. Escala de Inteligencia revisada para el nivel escolar (WISC-RM): manuale di applicazione adattato e standardizzato in Messico. Messico DF: Manuale Editoriale Moderno; 1993.
- 20. Istituto Nazionale per la Sicurezza e la Salute sul Lavoro. Manuale di metodi analitici. 3a edizione . Atlanta: Centers for Disease Control and Prevention; 1984.
- 21. Cox DH. Metodo di assorbimento atomico elettrotermico con evoluzione dell’arsina per la determinazione di livelli in nanogrammi di arsenico totale in urine e acqua. J Anal Toxicol 1980; 4:207-11.
- 22. Subramain KS. Determinazione del piombo nel sangue: confronto di due metodi GFAAS. Atom Spectrosc 1987; 8:7-14.
- 23. Dibley MJ, Goldsby JB, Staehling NW, Trowbridge FL. Sviluppo di curve normalizzate per il riferimento di crescita internazionale: considerazioni storiche e tecniche. Am J Clin Nutr 1987; 46:736-48.
- 24. Bronfman MG, Castro H, Gutiérrez G. Medición de la desigualdad: una strategia metodológica, análisis de las características socioeconómicas de la muestra. Arch Invest Med (Messico) 1998; 19:351-60.
- 25. Varner JA, Karl F, Horvarth JW, Issacson RL. Somministrazione cronica di fluoruro di alluminio o fluoruro di sodio a ratti in acqua potabile: alterazioni dell’integrità neuronale e cerebrovascolare. Brain Res 1998; 784:284-98.
- 26. Rodriguez VM, Carrizales L, Jimenez-Capdeville ME, Dufour L, Giordano M. Effetti dell’esposizione all’arsenito di sodio sui parametri comportamentali nel ratto. Brain Res Bull 2001; 55:301-8.
- 27. Rodriguez VM, Carrizales L, Mendoza MS, Fajardo OR, Giordano M. Effetti dell’esposizione all’arsenito di sodio sullo sviluppo e sul comportamento nel ratto. Neurotoxicol Teratol 2002; 24:743-50.