Studio di Stanford trova la prova biologica che il “vaccino” Covid causa miocardite
Una nuova analisi di Stanford ha identificato biomarcatori cardiaci elevati negli individui vaccinati — risultati coerenti con la miocardite subclinica. I dati suggeriscono che il coinvolgimento del cuore può verificarsi senza sintomi immediati, sollecitando richieste di sorveglianza a lungo termine e revisione indipendente.
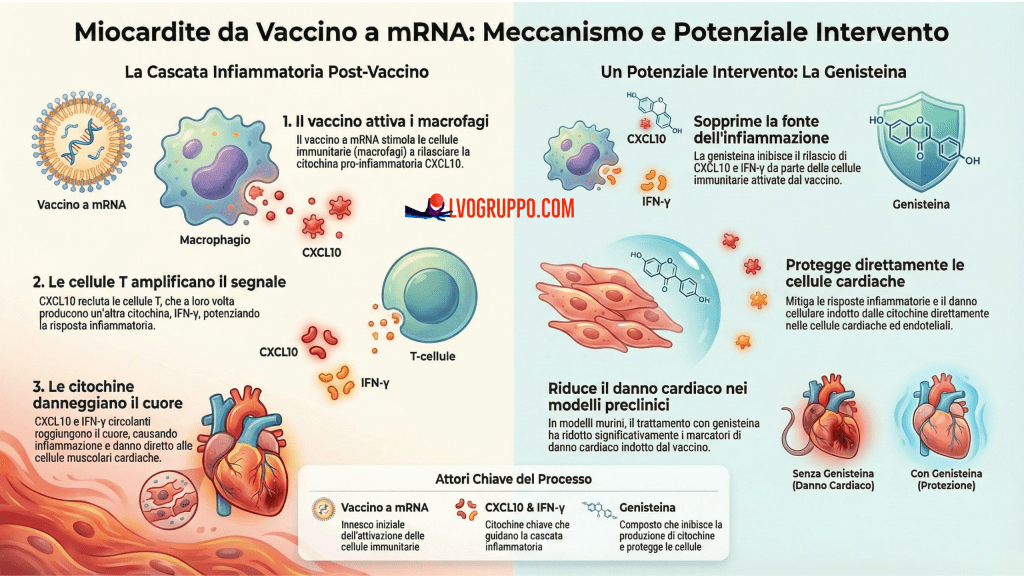
Articolo originale : Inhibition of CXCL10 and IFN-γ ameliorates myocarditis in preclinical models of SARS-CoV-2 mRNA vaccination
Introduzione
Il dibattito pubblico sui vaccini a mRNA contro il SARS-CoV-2 è stato spesso accompagnato da preoccupazioni riguardo ad un effetto collaterale: la miocardite, un’infiammazione del muscolo cardiaco.
La mancanza di una chiara spiegazione biologica ha alimentato dubbi e incertezze. Fino ad ora.
Un nuovo e rivoluzionario studio scientifico ha finalmente fatto luce sul preciso meccanismo cellulare che può portare a questa condizione.
Con un approccio da veri detective, i ricercatori hanno svelato una complessa reazione a catena che coinvolge specifiche cellule immunitarie e le proteine infiammatorie che esse producono. Non si tratta di un’azione diretta del vaccino sul cuore, ma di un effetto indiretto mediato da una cascata di eventi biologici ben definita.
In questo articolo, analizzeremo i risultati più sorprendenti e di maggiore impatto di questa ricerca, scomponendo il processo di scoperta in punti chiari e comprensibili per capire esattamente cosa accade nel corpo e come questa conoscenza potrebbe rendere i futuri vaccini ancora più sicuri.
1. Il problema è riconducibile a due segnali specifici: le citochine CXCL10 e IFN-γ
L’indagine scientifica è partita da un’intuizione brillante: riesaminare e confrontare dati già esistenti provenienti da due studi umani completamente indipendenti. Il primo dataset mostrava quali citochine (proteine-segnale del sistema immunitario) aumentano normalmente nel sangue di individui sani dopo la vaccinazione. Il secondo, invece, confrontava i livelli di citochine tra pazienti che avevano sviluppato miocardite e persone vaccinate che non avevano avuto problemi.
Mettendo insieme questi due pezzi del puzzle, è emerso un dato inequivocabile. Tra decine di molecole analizzate, solo due si distinguevano nettamente in entrambi gli scenari: la CXCL10 e l’interferone-gamma (IFN-γ). Queste due citochine non solo fanno parte della normale risposta immunitaria al vaccino, ma i loro livelli erano sproporzionatamente più alti proprio negli individui che avevano sviluppato miocardite.
Questa convergenza di prove è stata la svolta. Invece di parlare genericamente di “infiammazione”, la scienza è ora in grado di puntare il dito su un percorso biologico estremamente specifico, guidato da due precisi colpevoli molecolari. Questo ha permesso di focalizzare la ricerca non più su un fenomeno vago, ma su un meccanismo preciso e misurabile.
2. L’effetto domino: come si scatena la reazione immunitaria
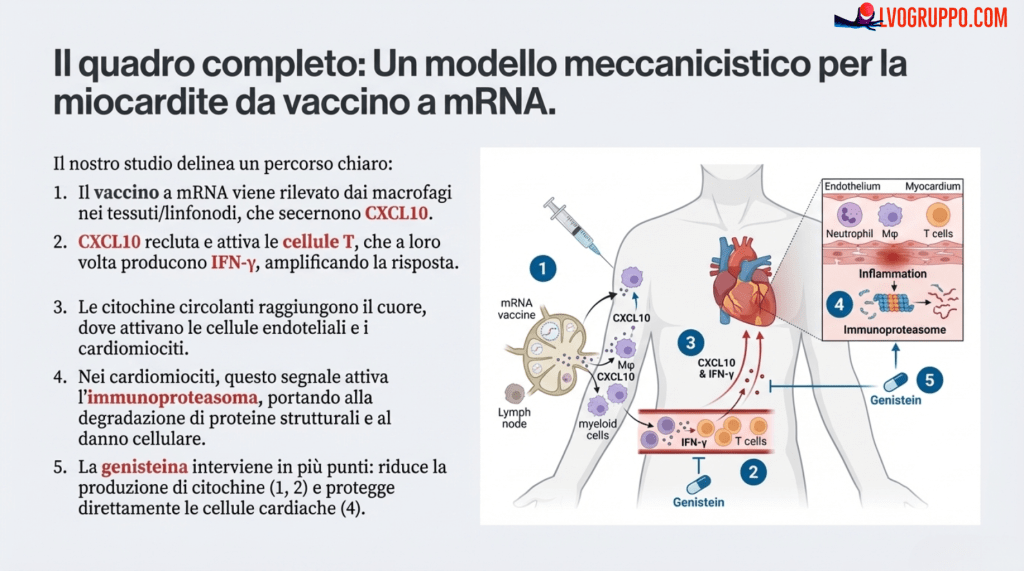
Il danno al cuore non è un effetto diretto del vaccino, ma la conseguenza di una sequenza di eventi, un vero e proprio effetto domino che coinvolge diverse cellule del sistema immunitario. Il modello elaborato dai ricercatori descrive questa catena di reazioni passo dopo passo.
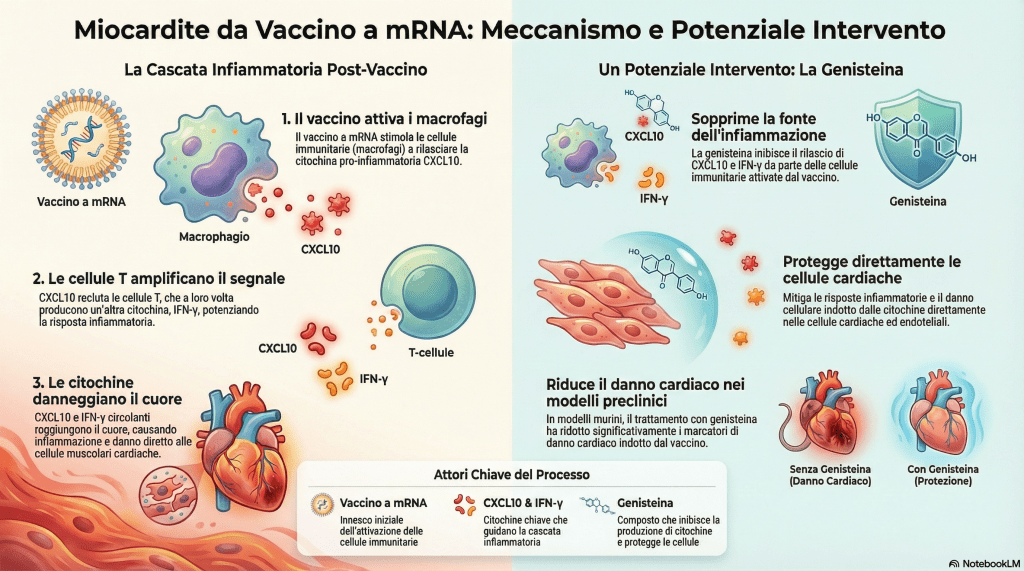
Passo 1: Dopo la somministrazione del vaccino, le prime cellule immunitarie a reagire all’mRNA sono i macrofagi. Questi “spazzini” del sistema immunitario, una volta attivati, iniziano a produrre il primo segnale: la citochina CXCL10.
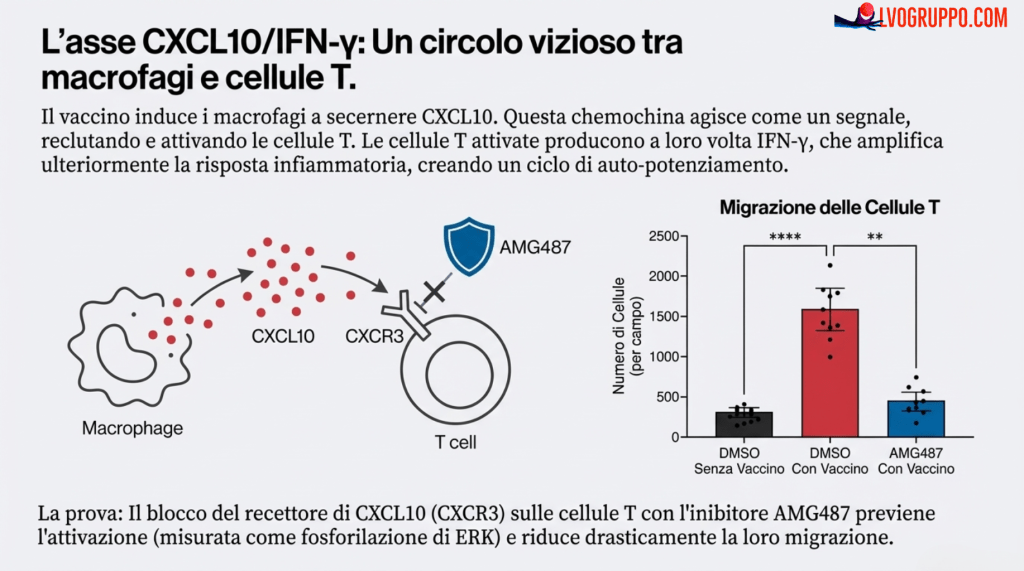
Passo 2: La CXCL10 agisce come un segnale di richiamo, una sorta di sirena che attira sul posto altre cellule immunitarie specializzate, i linfociti T.
Passo 3: Una volta reclutati e attivati, questi linfociti T producono a loro volta il secondo, potentissimo segnale: l’IFN-γ. Questa seconda ondata di segnali crea un circolo vizioso che amplifica ulteriormente la risposta infiammatoria.
In sintesi, la miocardite non è causata dal vaccino che “attacca” il cuore, ma è una conseguenza indiretta di questa specifica interazione a più stadi tra macrofagi e linfociti T, che genera un eccesso di segnali infiammatori circolanti.
3. L’obiettivo: in che modo l’infiammazione colpisce le cellule cardiache
Una volta che le citochine CXCL10 e IFN-γ vengono prodotte in grandi quantità ed entrano in circolo, cosa succede quando raggiungono il cuore? Lo studio ha rivelato anche questo passaggio cruciale. Queste molecole attivano un meccanismo specializzato all’interno delle stesse cellule del muscolo cardiaco (i cardiomiociti).
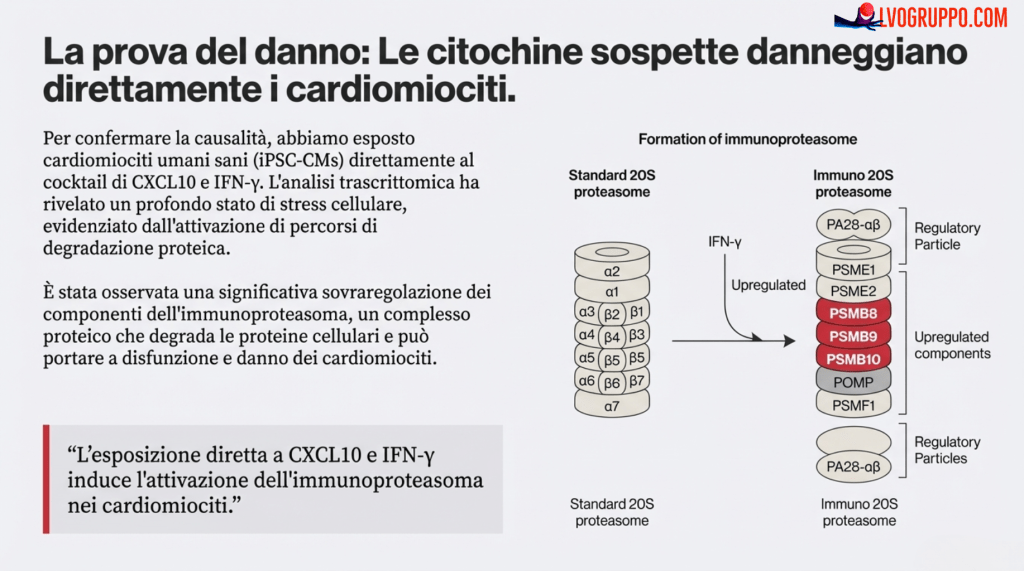
Questo meccanismo è noto come immunoproteasoma. Per comprenderlo, pensiamo al proteasoma standard come al “centro di riciclaggio” di una cellula, che scompone le proteine vecchie o danneggiate. L’immunoproteasoma è una sua versione ad alta potenza, che si attiva durante una forte risposta immunitaria. In questo caso, le citochine lo spingono in un tale stato di iperattività che inizia a distruggere anche le proteine strutturali essenziali, indebolendo di fatto il muscolo cardiaco.
Questo processo causa uno stress significativo e un danno diretto ai cardiomiociti. Come riassunto nel modello di lavoro dello studio:
Queste citochine circolano fino al cuore, dove attivano l’immunoproteasoma, promuovono la degradazione delle proteine strutturali e causano un danno ai cardiomiociti.
4. Una potenziale soluzione: la possibilità di bloccare il meccanismo
Comprendere un meccanismo in modo così dettagliato non serve solo a spiegare un problema, ma anche a trovare una soluzione. Nello studio, i ricercatori hanno testato un composto chiamato Genisteina per verificare se fosse in grado di interrompere questa cascata infiammatoria.
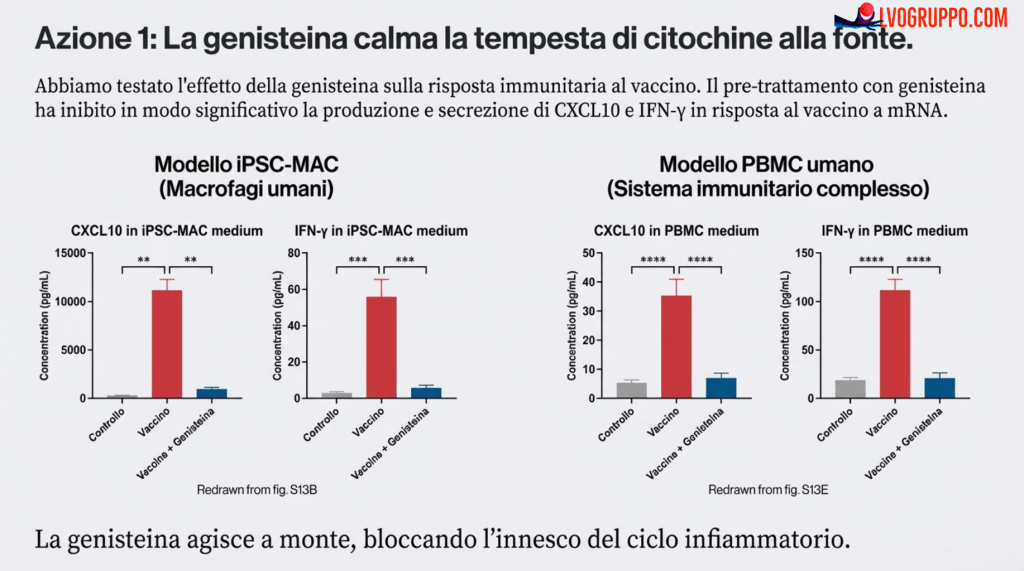
I risultati hanno mostrato che la Genisteina esercita una potente duplice azione, intervenendo sul problema con un attacco su due fronti. Agisce sia alla sorgente del problema, calmando le cellule immunitarie iperattive, sia sul bersaglio, proteggendo direttamente il tessuto cardiaco. In particolare, è stato dimostrato che la Genisteina:
Riduce la produzione stessa delle citochine “colpevoli” (CXCL10 e IFN-γ) da parte delle cellule immunitarie.
Sembra proteggere direttamente le cellule cardiache dal danno indotto dall’attivazione dell’immunoproteasoma.
È importante sottolineare che questo non significa che la Genisteina sia un trattamento pronto all’uso. Il vero punto di svolta è la dimostrazione che, conoscendo il percorso molecolare esatto, gli scienziati possono testare interventi mirati per bloccarlo. Questa conoscenza apre la strada allo sviluppo di strategie per rendere i vaccini di prossima generazione ancora più sicuri, neutralizzando questo raro effetto collaterale senza comprometterne l’efficacia.
Questa ricerca trasforma un’area di incertezza in una narrazione scientifica chiara e definita. Ora sappiamo che il raro evento di miocardite post-vaccino a mRNA è il risultato di una catena di eventi ben precisa: i macrofagi, stimolati dal vaccino, producono CXCL10; questa richiama i linfociti T, che rilasciano IFN-γ; infine, queste due citochine attivano l’immunoproteasoma nelle cellule cardiache, causando un danno.
Questa scoperta non solo rassicura sulla natura indiretta e immunomediata del fenomeno, ma fornisce anche un bersaglio preciso per future ottimizzazioni. La domanda che sorge spontanea è: in che modo questo livello di comprensione molecolare potrà plasmare il futuro dello sviluppo dei vaccini e aprire le porte a una medicina sempre più personalizzata, in grado di prevedere e prevenire anche le reazioni più rare?
La Risposta Immunitaria alla Vaccinazione a mRNA: Un Percorso Guidato
1. L’Innesco: La Prima Reazione Immunitaria
1.1 L’arrivo del vaccino e la risposta dei macrofagi
Il primo passo della risposta immunitaria dopo la somministrazione di un vaccino a mRNA avviene a livello locale, nel tessuto in cui viene effettuata l’iniezione. Le prime cellule a reagire sono le sentinelle del sistema immunitario residenti in quell’area, in particolare i macrofagi. Come illustrato nel modello di lavoro in fig. S16, queste cellule “percepiscono” la presenza dell’mRNA del vaccino, riconoscendolo come un segnale che richiede una reazione immediata e dando così il via a una cascata di eventi difensivi.
1.2 Il primo segnale d’allarme: la citochina CXCL10
Per coordinare la difesa, le cellule immunitarie comunicano attraverso “messaggeri chimici” chiamati citochine. In risposta al vaccino a mRNA, i macrofagi rilasciano una citochina chiave: la CXCL10. Questo segnale agisce come un “richiamo alle armi”, la cui funzione primaria, come descritto in fig. S16, è quella di reclutare altre cellule immunitarie specializzate, in particolare i linfociti T, attirandole verso il sito di iniezione. L’importanza di questo segnale è confermata dai dati in fig. S1 E, che mostrano come la CXCL10 sia una delle citochine i cui livelli aumentano in modo più significativo nel sangue dopo la vaccinazione.
Questo primo allarme, tuttavia, è solo l’inizio. Il segnale lanciato da CXCL10 innesca una reazione a catena che amplifica la risposta, chiamando in causa altri attori fondamentali del sistema immunitario.
2. L’Amplificazione: L’intervento dei Linfociti T
2.1 La chiamata dei rinforzi: reclutamento e migrazione dei linfociti T
La citochina CXCL10, rilasciata dai macrofagi, non si limita ad attirare i linfociti T, ma li attiva anche. L’esperimento mostrato in fig. S5 dimostra che il mezzo di coltura prelevato dai macrofagi esposti al vaccino è in grado di attivare i linfociti T, causando un aumento del marcatore di attivazione P-ERK. Ma come sappiamo che è proprio CXCL10 il mediatore chiave? La prova decisiva arriva bloccando il suo recettore specifico (CXCR3) con un inibitore chimico, l’AMG487. Tale blocco riduce significativamente sia l’attivazione dei linfociti T (fig. S5 C) sia la loro capacità di migrare verso la fonte del segnale (fig. S5 E), confermando in modo inequivocabile il ruolo centrale di CXCL10 in questa fase di reclutamento.
2.2 Il secondo segnale potente: il rilascio di IFN-γ
Una volta attivati e giunti sul posto, i linfociti T contribuiscono in modo decisivo all’amplificazione della risposta immunitaria rilasciando un’altra citochina estremamente potente: l’Interferone-gamma (IFN-γ). Come illustrato nel modello di fig. S16, l’IFN-γ agisce potenziando ulteriormente la risposta infiammatoria. Anche in questo caso, i dati clinici di fig. S1 E confermano che l’IFN-γ è, insieme a CXCL10, una delle citochine più significativamente aumentate nel circolo sanguigno in seguito alla vaccinazione.
2.3 Il circolo vizioso infiammatorio: un meccanismo di feedback
La combinazione di queste due citochine crea un potente ciclo di feedback che auto-amplifica la risposta infiammatoria. Il processo, sintetizzato in fig. S16, funziona in questo modo:
I macrofagi, stimolati dal vaccino, producono CXCL10.
CXCL10 attira e attiva i linfociti T.
I linfociti T attivati producono IFN-γ.
L’IFN-γ, a sua volta, stimola un’ulteriore e più massiccia produzione di CXCL10, creando un circolo virtuoso (o vizioso, a seconda del contesto) che si auto-alimenta, dove ogni passaggio potenzia il precedente, portando a un’esplosione controllata della risposta infiammatoria.
Queste potenti citochine non agiscono solo localmente. Circolando nel corpo, possono raggiungere organi distanti come il cuore e innescare cambiamenti specifici a livello cellulare, introducendo il prossimo protagonista della nostra storia: l’immunoproteasoma.
**3. L’Effetto a Valle: L’Attivazione dell’**Immunoproteasoma
3.1 Un “interruttore” molecolare nelle cellule cardiache
Ogni cellula possiede un sofisticato macchinario molecolare chiamato proteasoma, che funziona come un “sistema di riciclaggio” per le proteine vecchie o danneggiate, mantenendo l’ordine e la funzionalità cellulare. In condizioni normali, questo macchinario esiste in una forma “standard”. Tuttavia, le citochine infiammatorie come l’IFN-γ possono agire da interruttore, inducendo le cellule a modificare il proteasoma per adattarlo a esigenze di tipo immunitario.
**3.2 Dal Proteasoma Standard all’**Immunoproteasoma
Quando le cellule cardiache (cardiomiociti) sono esposte a segnali come l’IFN-γ, il proteasoma standard viene convertito nella sua forma specializzata, l’immunoproteasoma, attraverso la sostituzione di alcune delle sue subunità.
| Caratteristica | Proteasoma Standard | Immunoproteasoma |
|---|---|---|
| Stato di attivazione | Sempre attivo (funzione di base) | Indotto da segnali immunitari (es. IFN-γ) |
| Funzione primaria | Riciclaggio di proteine vecchie o danneggiate | Elaborazione di peptidi per la presentazione al sistema immunitario e la risposta infiammatoria |
| Composizione | Contiene subunità standard (β1, β2, β5) | Le subunità standard sono sostituite da subunità specializzate (PSMB9, PSMB10, PSMB8) |
Le prove sperimentali dimostrano che il trattamento delle cellule cardiache con CXCL10 e IFN-γ innesca questa conversione. L’analisi trascrittomica (fig. S10 I) mostra un netto aumento della trascrizione genica per le subunità specializzate PSMB8, PSMB9 e PSMB10. Questo aumento a livello di geni si traduce poi in un effettivo incremento dell’abbondanza proteica di queste componenti, come confermato dall’analisi proteomica in fig. S11 A, completando di fatto la trasformazione del macchinario nella sua forma immunitaria.
3.3 La funzione dell’Immunoproteasoma: degradazione proteica e infiammazione
La conversione in immunoproteasoma ha una conseguenza funzionale precisa. Questo macchinario modificato accelera la degradazione delle proteine all’interno della cellula. Nelle cellule cardiache, come suggerito dal modello in fig. S16 e dal processo biologico “proteasomal protein catabolic process” evidenziato in fig. S10 H, questo si traduce in un’aumentata scomposizione di proteine strutturali. Tale processo contribuisce attivamente all’infiammazione locale e al potenziale danno cellulare nel tessuto cardiaco.
In questo modo, un segnale immunitario sistemico, rappresentato dalle citochine circolanti, si traduce in un cambiamento meccanicistico specifico all’interno delle cellule di un organo, collegando la risposta al vaccino a un effetto cellulare a distanza.
4. Conclusione: La Cascata Immunitaria in Sintesi
4.1 Riepilogo del percorso
L’intera sequenza di eventi può essere riassunta in una cascata logica e consequenziale, che illustra il percorso dalla vaccinazione all’effetto cellulare.
Innesco: Il vaccino a mRNA attiva i macrofagi residenti nei tessuti, che rilasciano la citochina CXCL10.
Amplificazione: CXCL10 recluta i linfociti T, che a loro volta producono la citochina IFN-γ, creando un ciclo di feedback che amplifica l’infiammazione sistemica.
Azione a distanza: Le citochine circolanti raggiungono il cuore e attivano un interruttore molecolare nelle cellule cardiache, convertendo il proteasoma standard in immunoproteasoma.
Effetto cellulare: L’immunoproteasoma aumenta la degradazione delle proteine strutturali, contribuendo alla risposta infiammatoria locale nel tessuto cardiaco.
4.2 L’insegnamento chiave
Questo percorso biologico illustra in modo esemplare come il sistema immunitario utilizzi una serie di segnali a cascata, altamente coordinati e potenti, per orchestrare una difesa efficace. Dimostra come una risposta immunitaria iniziata localmente possa avere effetti sistemici, mediati da messaggeri chimici che viaggiano attraverso il corpo. Infine, evidenzia come meccanismi cellulari specifici e finemente regolati, come l’attivazione dell’immunoproteasoma, siano fondamentali in questo processo, rivelando la complessità e l’eleganza della biologia immunitaria.
Relazione Tecnica: Protocolli Standardizzati per la Differenziazione di iPSC e la Generazione di Sferoidi Cardiaci 3D
1.0 Introduzione e Scopo del Documento
La capacità di indirizzare la differenziazione di cellule staminali pluripotenti indotte (iPSC) verso lignaggi cellulari specifici rappresenta una pietra miliare per la modellizzazione delle malattie umane e per lo sviluppo di nuove terapie nel campo della medicina rigenerativa. La disponibilità di protocolli standardizzati e riproducibili è un requisito strategico fondamentale per garantire la coerenza e l’affidabilità dei risultati sperimentali. Questa relazione tecnica ha lo scopo di sintetizzare, in modo chiaro e sequenziale, le metodologie per la generazione di cardiomiociti, macrofagi e cellule endoteliali a partire da iPSC. Inoltre, viene descritta la procedura per l’assemblaggio di questi tipi cellulari in sferoidi cardiaci 3D, un modello in vitro avanzato. Tutte le procedure qui riportate sono una sintesi dei metodi descritti nella sezione Supplementary* *Materials della pubblicazione di Cao et al., Sci. Transl. Med. 17, eadq0143 (2025). Prima di procedere con i protocolli di differenziazione, è essenziale definire le condizioni di base per la coltura e il mantenimento delle iPSC indifferenziate.
2.0 Condizioni di Coltura di Base e Mantenimento delle **iPSC
Il mantenimento della pluripotenza e della vitalità delle linee di iPSC di partenza è un prerequisito critico per il successo dei successivi protocolli di differenziazione. Qualsiasi deviazione dalle condizioni ottimali può compromettere la capacità delle cellule di rispondere in modo efficiente e omogeneo agli stimoli differenziativi. Questa sezione delinea il protocollo essenziale per la coltura e l’espansione delle iPSC in uno stato indifferenziato.
**2.1 Protocollo di Mantenimento delle **iPSC
Le condizioni standard per la coltura di iPSC umane sono riassunte di seguito:
Terreno di coltura: Le cellule devono essere coltivate in terreno Essential 8.
Supporto alla vitalità: Per migliorare la sopravvivenza cellulare dopo il passaggio delle cellule, è necessario aggiungere al terreno l’inibitore della chinasi ROCK, Y27632, alla concentrazione di 10 μM per le prime 24 ore.
Frequenza di ricambio: Il terreno di coltura deve essere sostituito quotidianamente per garantire un apporto costante di nutrienti e rimuovere i metaboliti di scarto.
Ambiente di incubazione: Le colture devono essere mantenute in un incubatore umidificato a una temperatura di 37°C e con una concentrazione di CO₂ del 5%.
Una volta ottenuta un’espansione sufficiente di cellule staminali sane e pluripotenti, è possibile procedere con i protocolli specifici per la loro differenziazione guidata verso i lignaggi desiderati.
3.0 Protocolli di Differenziazione Guidata da **iPSC
I protocolli descritti di seguito si basano sull’applicazione precisa e temporalmente regolata di fattori di crescita e piccole molecole per indirizzare in modo efficiente la differenziazione delle iPSC verso tre distinti lignaggi cellulari: macrofagi (iPSC-MAC), cardiomiociti (iPSC-CM) e cellule endoteliali (iPSC-EC).
3.1 Differenziazione in Macrofagi (iPSC-MAC)
La generazione di macrofagi maturi da iPSC è un processo multifase che si estende per oltre 20 giorni. Il protocollo prevede una serie di trattamenti sequenziali volti a guidare le cellule attraverso stadi intermedi di progenitori ematopoietici fino a ottenere monociti purificati, che vengono infine maturati in macrofagi. I passaggi chiave sono riassunti nella seguente tabella.
| Fase/Giorni | Componenti del Mezzo | Note Operative |
|---|---|---|
| Giorno 0-2 | Mezzo IF9S + 50 ng/mL BMP4, 15 ng/mL Activin A, 1.5 µM CHIR99021 | Inizio dell’induzione |
| Giorno 2-5 | Mezzo IF9S + 50 ng/mL VEGF, 50 ng/mL bFGF, 50 ng/mL SCF, 10 µM SB431542 | Transizione verso il lignaggio ematopoietico (durata: 3 giorni) |
| Giorno 5-9 | Mezzo IF9S + 50 ng/mL VEGF, 50 ng/mL bFGF, 50 ng/mL SCF, 50 ng/mL IL-6, 50 ng/mL TPO, 10 ng/mL IL-3 | Espansione dei progenitori (durata: 4 giorni) |
| Giorno 9-15 | Mezzo IF9S + 50 ng/mL IL-6, 10 ng/mL IL-3, 80 ng/mL M-CSF | Differenziazione verso monociti (durata: 6 giorni) |
| Giorno 15 | – | Selezione dei monociti CD14+ tramite biglie magnetiche |
| Post-Giorno 15 (6 giorni) | Mezzo IF9S + 80 ng/mL M-CSF | Maturazione finale in macrofagi |
3.2 Differenziazione in Cardiomiociti (iPSC-CM)
La differenziazione in cardiomiociti contrattili (beating iPSC-CMs) si basa su un protocollo di modulazione chimica della via di segnalazione Wnt. La procedura prevede l’attivazione seguita dall’inibizione di questa via per mimare i segnali dello sviluppo cardiaco embrionale. Un passaggio cruciale è la purificazione metabolica, basata sulla selezione delle cellule in un terreno privo di D-glucosio per eliminare le popolazioni cellulari non-cardiomiocitiche.
| Giorno | Mezzo e Supplementi | Azione/Scopo |
|---|---|---|
| 0 | RPMI + B27 (senza insulina) + 7 µM CHIR99021 | Attivazione della via di Wnt |
| 2 | RPMI + B27 (senza insulina) | Ricambio del terreno |
| 3 | RPMI + B27 (senza insulina) + 5 µM IWR-1 | Inibizione della via di Wnt |
| 5 | RPMI + B27 (senza insulina) | Ricambio del terreno |
| 7 | RPMI + B27 | Ricambio con terreno completo |
| 9 | RPMI + B27 (senza D-glucosio) | Purificazione dei cardiomiociti (3 giorni) |
| 12 | RPMI + B27 | Ricambio con terreno completo |
| 13 | RPMI + B27 + 3 µM CHIR99021 | Re-piastramento ed espansione (6 giorni) |
| Post-espansione | RPMI + B27 | Mantenimento fino al Giorno 30 |
3.3 Differenziazione in Cellule Endoteliali (iPSC-EC)
Questo protocollo guida la differenziazione delle iPSC verso il lignaggio endoteliale, fondamentale per la vascolarizzazione e la funzione tissutale. La procedura si conclude con l’isolamento di una popolazione pura di cellule endoteliali tramite selezione immunomagnetica basata sull’espressione del marcatore di superficie CD144.
| Giorno | Trattamento (Mezzo e Reagenti) |
|---|---|
| 0 | Terreno BPEL + 8 µM CHIR99021 |
| 3, 6, 9 | Ricambio con terreno BPEL + 50 ng/mL VEGF, 10 µM SB431542 |
| 10 | Isolamento delle cellule iPSC-EC con biglie magnetiche CD144 |
| Post-10 | Mantenimento in terreno EGM2 (usare prima del passaggio 3) |
La generazione efficiente di questi tre tipi cellulari apre la strada alla loro integrazione in modelli tissutali 3D più complessi e funzionali, come gli sferoidi cardiaci.
4.0 Generazione di Sferoidi Cardiaci 3D
Gli sferoidi cardiaci 3D rappresentano modelli in vitro superiori rispetto alle colture bidimensionali (2D) grazie alla loro capacità di ricapitolare in modo più fedele l’architettura cellulare, le interazioni cellula-cellula e la fisiologia a livello tissutale del miocardio. Questa sezione descrive il protocollo di co-coltura per l’assemblaggio di queste strutture tridimensionali auto-organizzanti.
4.1 Protocollo di Assemblaggio degli Sferoidi
La generazione di sferoidi cardiaci stabili e funzionali richiede la combinazione di tipi cellulari specifici a stadi di maturazione definiti e in rapporti precisi.
Tipi cellulari e stato richiesto:
Cardiomiociti** (iPSC-CMs):** Utilizzati al giorno 30 del protocollo di differenziazione.
Cellule Endoteliali (iPSC-ECs): Utilizzate al passaggio 1 (P1).
Macrofagi (iPSC-MACs): Utilizzati prima del giorno 30 di maturazione.
Rapporto cellulare: Il rapporto di combinazione è 7:2:1 (iPSC-CM : iPSC-EC : iPSC-MAC).
Procedura di assemblaggio:
Preparazione Cellulare: Tutti e tre i tipi cellulari vengono dissociati in sospensioni di singole cellule. Successivamente, vengono mescolati secondo il rapporto stabilito e risospesi nel terreno completo (70% RPMI, 30% EGM2, 50 ng/mL VEGF) a una concentrazione finale di 1.5 milioni di cellule/mL.
Aggregazione: 1 mL della miscela cellulare viene seminato in ciascun pozzetto di una piastra AggreWellTM800 24-well Plate. La geometria di questi pozzetti facilita la sedimentazione e l’aggregazione cellulare per formare sferoidi di dimensioni uniformi.
Mantenimento in Coltura: Per sostenere la vitalità e la maturazione degli sferoidi, metà del volume del terreno di coltura viene sostituita con terreno fresco nei giorni 2 e 4 dopo la semina.
Pronto per l’Uso: A partire dal giorno 5, gli sferoidi sono considerati formati e pronti per essere utilizzati negli esperimenti successivi.
5.0 Considerazioni Finali
I protocolli qui sintetizzati forniscono un quadro metodologico standardizzato per derivare cardiomiociti, macrofagi e cellule endoteliali da linee di iPSC e per assemblarli in costrutti cardiaci 3D. Queste procedure costituiscono la base per la creazione di modelli cellulari e tissutali avanzati, garantendo un’elevata riproducibilità essenziale per lo studio di patologie cardiache a base infiammatoria, lo screening di farmaci e l’analisi dei meccanismi di cardiotossicità.
PARTE 2 : Svelare il Mistero: Come la Scienza Studia la Miocardite da Vaccino a mRNA
Introduzione: La Domanda Guida della Ricerca
Benvenuto in questo viaggio nel cuore del metodo scientifico. Da quando sono stati introdotti i vaccini a mRNA contro il SARS-CoV-2, è emersa una rara, ma importante, associazione con la miocardite, un’infiammazione del muscolo cardiaco. Di fronte a questa osservazione, la comunità scientifica si è posta una domanda cruciale: non solo se esista un legame, ma perché e come avviene a livello delle nostre cellule e molecole.
Questo studio non si è fermato alla superficie. I ricercatori hanno messo in campo un arsenale di tecniche all’avanguardia per smontare il problema pezzo per pezzo e poi ricomporre il puzzle. In questa panoramica, ti guideremo passo dopo passo attraverso l’ingegnoso modello sperimentale che hanno costruito, mostrandoti come la scienza moderna possa trasformare un dubbio in una chiara comprensione biologica.
1. Capitolo 1: Alla Ricerca di Indizi nei Dati Umani
Ogni buona indagine scientifica inizia raccogliendo gli indizi disponibili. In questo caso, i ricercatori hanno iniziato la loro “caccia” analizzando i dati già esistenti, raccolti da migliaia di persone, per passare da un’osservazione su larga scala a un’ipotesi specifica e verificabile.
1.1. L’Analisi dei Dati Esistenti
Il primo passo è stato quello di guardare al quadro generale. I ricercatori hanno esaminato i database pubblici, come il VAERS (Vaccine Adverse Event Reporting System), per avere una misura quantitativa dei casi di miocardite segnalati dopo la vaccinazione.
Successivamente, hanno compiuto un passo più profondo, rianalizzando i dati di studi precedenti (come quelli di Arunachalam* et al.* e Barmada* et al.*) che avevano misurato i livelli di decine di proteine infiammatorie, chiamate citochine, nel sangue di persone vaccinate. Questo equivaleva a “interrogare” il sangue dei pazienti alla ricerca di molecole sospette.
1.2. L’Identificazione dei Sospetti Principali: CXCL10 e IFN-γ
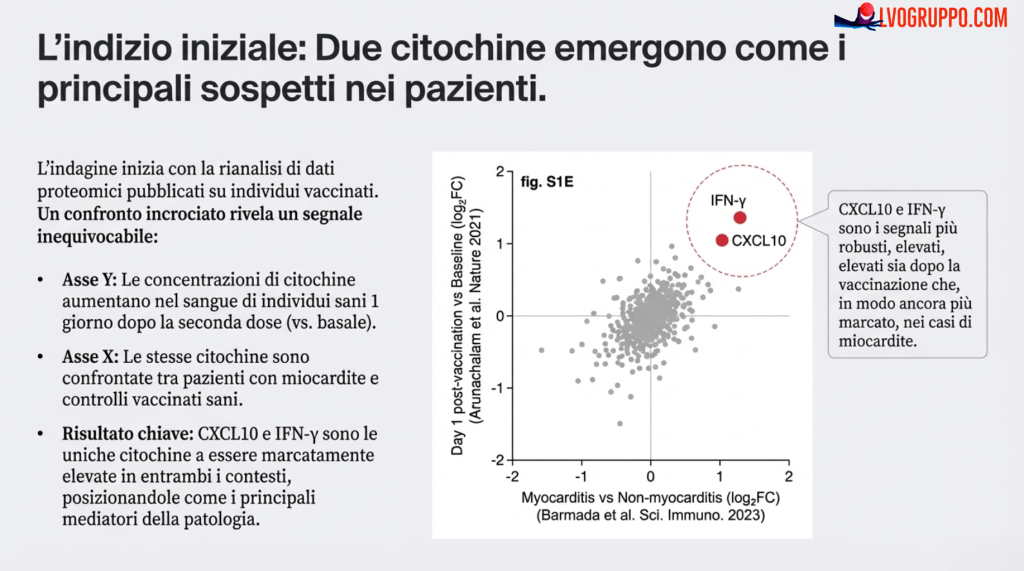
Dalla rianalisi di questi dati proteomici (come mostrato nel grafico di fig. S1E), sono emerse due molecole chiave che si distinguevano nettamente dalle altre: CXCL10 e IFN-γ.
Questa scoperta è stata l’indizio fondamentale. I dati mostravano che queste due citochine infiammatorie erano significativamente elevate:
Nelle persone sane, subito dopo la seconda dose di vaccino.
In modo ancora più marcato, nei pazienti che avevano effettivamente sviluppato la miocardite.
Questo suggeriva un meccanismo ‘dose-dipendente’: una normale risposta infiammatoria al vaccino (livelli moderati di citochine) che, in alcuni rari individui, poteva superare una soglia critica, portando al danno cardiaco (livelli molto elevati).
I dati umani hanno puntato i riflettori su due molecole specifiche, CXCL10 e IFN-γ, suggerendo che potessero essere i principali responsabili della reazione infiammatoria che porta al danno cardiaco.
1.3. Transizione al Capitolo Successivo
Con questi due “sospetti” molecolari in mano, la sfida successiva per i ricercatori è stata quella di ricreare l’intero processo in laboratorio per studiarlo da vicino.
2. Capitolo 2: Ricostruire il Cuore in Laboratorio (Modelli In Vitro)
Per capire come le molecole sospette agissero a livello cellulare, i ricercatori hanno utilizzato tecnologie avanzate per costruire modelli del cuore umano in una piastra di laboratorio (in vitro), permettendo loro di osservare ogni interazione passo dopo passo.
2.1. La Magia delle Cellule Staminali Pluripotenti Indotte (iPSC)
La base di questo approccio è una tecnica rivoluzionaria nota come iPSC** (induced Pluripotent Stem Cells)**. Questa tecnologia permette di prendere cellule adulte comuni, come quelle prelevate da un campione di sangue, e “riprogrammarle” geneticamente per farle tornare a uno stato primordiale, simile a quello delle cellule staminali embrionali. Da qui, i ricercatori possono “guidarle” a specializzarsi e diventare qualsiasi tipo di cellula del corpo. Questa tecnologia è fondamentale perché permette di studiare gli effetti su cellule umane—specificamente quelle del cuore e del sistema immunitario—senza dover prelevare tessuti direttamente dai pazienti, un’operazione che sarebbe invasiva e impraticabile.
Per questo studio, hanno creato i tre tipi di cellule fondamentali per ricostruire le interazioni chiave nel cuore:
Cardiomiociti** (iPSC-CMs):** Le cellule muscolari del cuore, quelle che si contraggono per pompare il sangue.
Cellule Endoteliali (iPSC-ECs): Le cellule che formano il rivestimento interno dei vasi sanguigni del cuore.
Macrofagi (iPSC-MACs): Un tipo di cellula immunitaria “sentinella”, sempre in allerta per rilevare potenziali minacce.
2.2. L’Esperimento Chiave: Una Catena di Eventi
Con queste cellule a disposizione, i ricercatori hanno meticolosamente ricostruito la catena di eventi causa-effetto che sospettavano portasse al danno cardiaco.
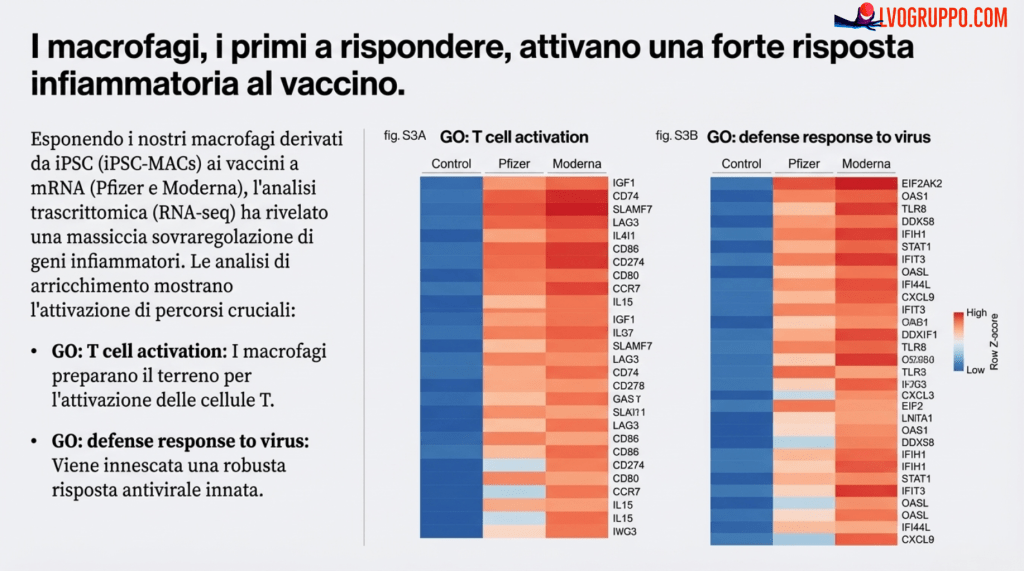
Passo 1: La Reazione Immunitaria Iniziale. Per prima cosa, hanno esposto i macrofagi (iPSC-MACs) ai vaccini Pfizer e Moderna. Il risultato è stato immediato e chiaro: i macrofagi hanno reagito producendo grandi quantità della prima molecola sospetta, CXCL10 (risultato confermato sia a livello proteico in fig. S2 che a livello genico in fig. S3).
Passo 2: Il Dialogo tra Cellule Immunitarie. Successivamente, hanno simulato l’interazione tra diverse cellule immunitarie. Hanno preso il “brodo di coltura” dei macrofagi attivati dal vaccino (ricco di CXCL10) e lo hanno usato per stimolare i linfociti T. Hanno scoperto che il CXCL10 prodotto dai macrofagi agiva come un potente segnale chimico (una chemochina) che “chiamava a raccolta” e attivava i linfociti T, spingendoli a muoversi. Questo passaggio è cruciale, perché dimostra come una reazione immunitaria locale possa iniziare a reclutare i soldati specializzati (i linfociti T) che, una volta attivati, sono la fonte della seconda molecola sospetta: l’IFN-γ (esperimento di attivazione e migrazione in fig. S5).
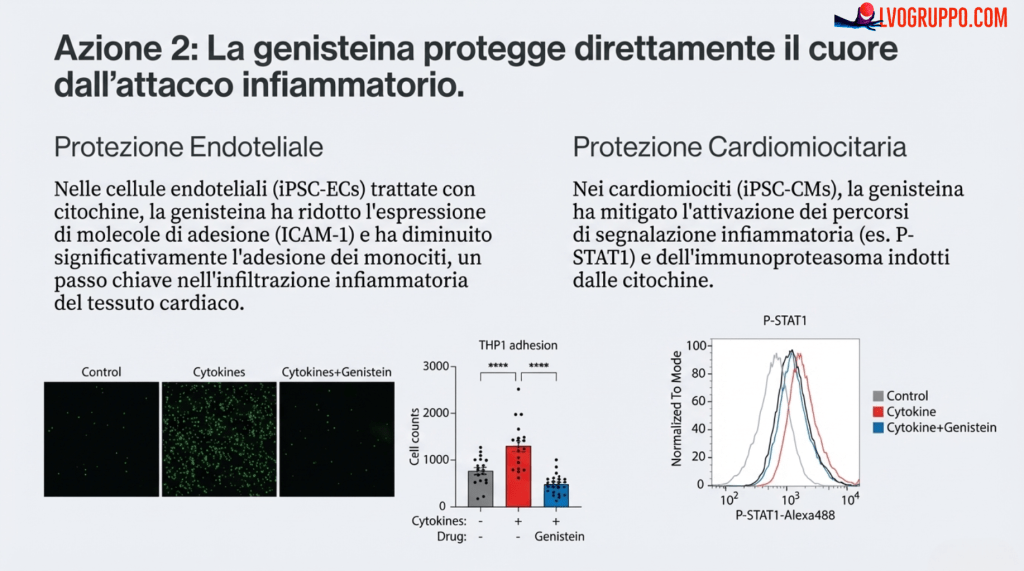
Passo 3: L’Infiammazione dei Vasi Sanguigni. A questo punto, i ricercatori avevano il “cocktail” infiammatorio completo (CXCL10 + IFN-γ). Lo hanno aggiunto alle cellule endoteliali (iPSC-ECs). Come previsto, le cellule che rivestono i vasi sanguigni si sono “infiammate”, iniziando a esprimere sulla loro superficie delle molecole di adesione, come delle bandierine che attirano altre cellule immunitarie, preparando il terreno per l’invasione del tessuto.
Passo 4: Il Danno Diretto al Muscolo Cardiaco. Infine, hanno trattato direttamente i cardiomiociti (iPSC-CMs) con il cocktail di CXCL10 e IFN-γ. I risultati hanno mostrato chiari segni di stress e danno cellulare (fig. S9, S10). Andando ancora più a fondo, hanno identificato il meccanismo molecolare preciso del danno: l’**attivazione dell’**immunoproteasoma, una sorta di “macchinario di riciclaggio” cellulare che, in condizioni di forte infiammazione, può andare in iper-attività e iniziare a degradare proteine strutturali essenziali per la cellula cardiaca. I ricercatori hanno confermato questo non solo tramite analisi genetiche (fig. S10), ma anche misurando direttamente un aumento dell’attività di questo macchinario nelle cellule cardiache esposte alle citochine (fig. S11).
2.3. Transizione al Capitolo Successivo
Dopo aver meticolosamente ricostruito la catena di eventi in una piastra di laboratorio, era il momento di verificare se questo stesso meccanismo si verificasse anche in un organismo complesso e vivente.
3. Capitolo 3: La Prova Finale (Modelli In Vivo)
Le scoperte fatte in laboratorio sono fondamentali, ma per avere la conferma definitiva è necessario osservare il fenomeno in un sistema biologico completo. Per questo, i ricercatori si sono rivolti a modelli animali (in vivo).
3.1. Perché Usare i Topi?
I modelli animali, in questo caso topi delle linee BALB/c e C57BL/6NCr, sono essenziali nella ricerca biomedica. Permettono di studiare gli effetti sistemici di un trattamento (cioè come influisce sull’intero organismo) e di confermare che i meccanismi scoperti nelle cellule isolate (in vitro) sono validi anche nel complesso contesto di un corpo vivente, dove organi e sistemi interagiscono tra loro.
3.2. Gli Esperimenti di Conferma
Per verificare le loro ipotesi, i ricercatori hanno condotto tre esperimenti cruciali sui topi, riassunti nella tabella seguente.
| Esperimento | Domanda a cui Risponde | Risultato Chiave |
|---|---|---|
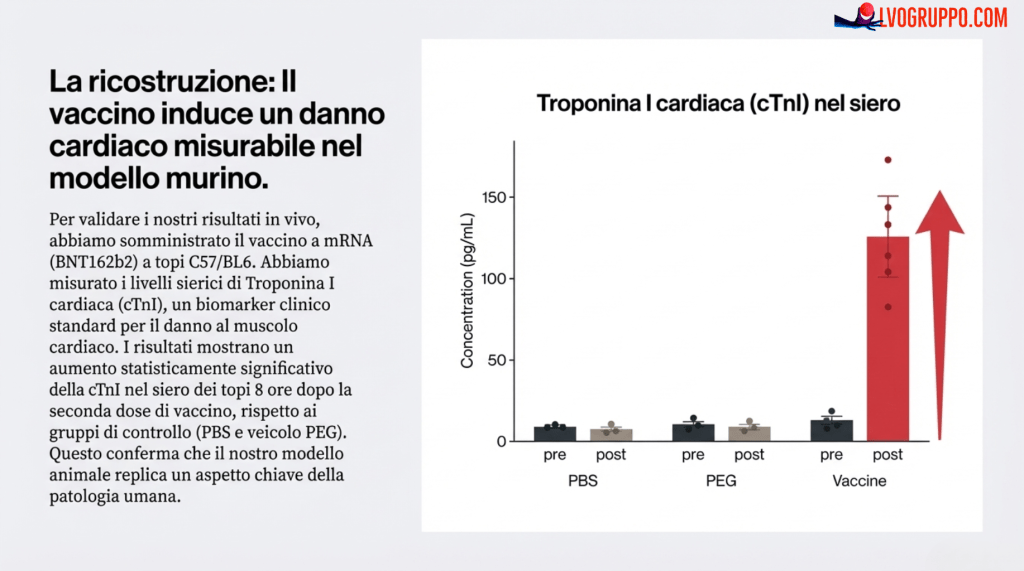
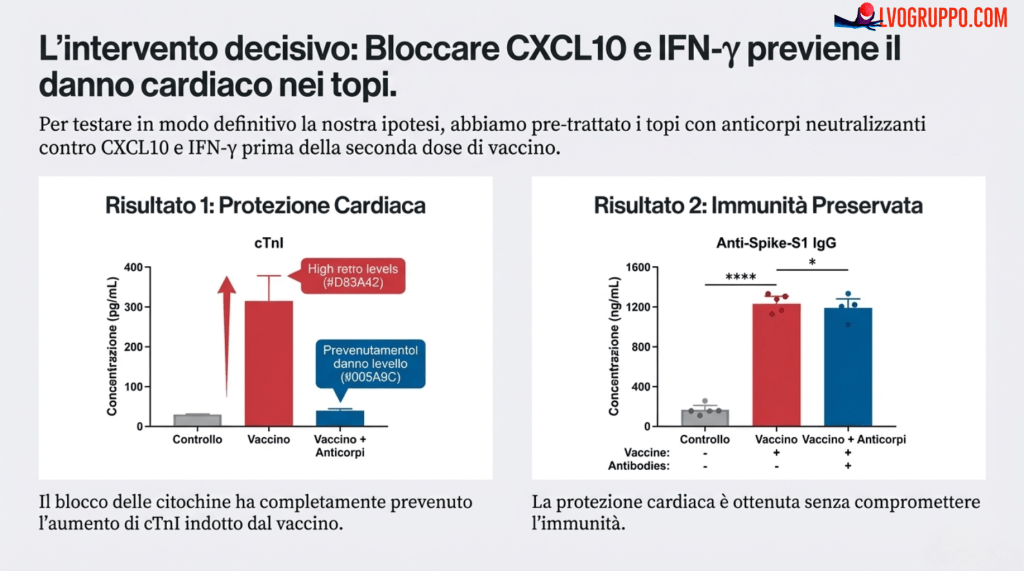
| Somministrazione del Vaccino | La vaccinazione nei topi causa un danno cardiaco misurabile? | Sì. I topi vaccinati mostravano un aumento dei marcatori di danno cardiaco (cTnI) nel sangue (fig. S6). |
| Blocco delle Citochine | Se blocchiamo CXCL10 e IFN-γ con degli anticorpi, possiamo prevenire il danno? | Sì. I topi trattati con anticorpi specifici hanno mostrato una riduzione significativa del danno cardiaco e dell’infiltrazione di cellule immunitarie nel cuore (fig. S7). Questa è stata la prova diretta del loro ruolo causale. |
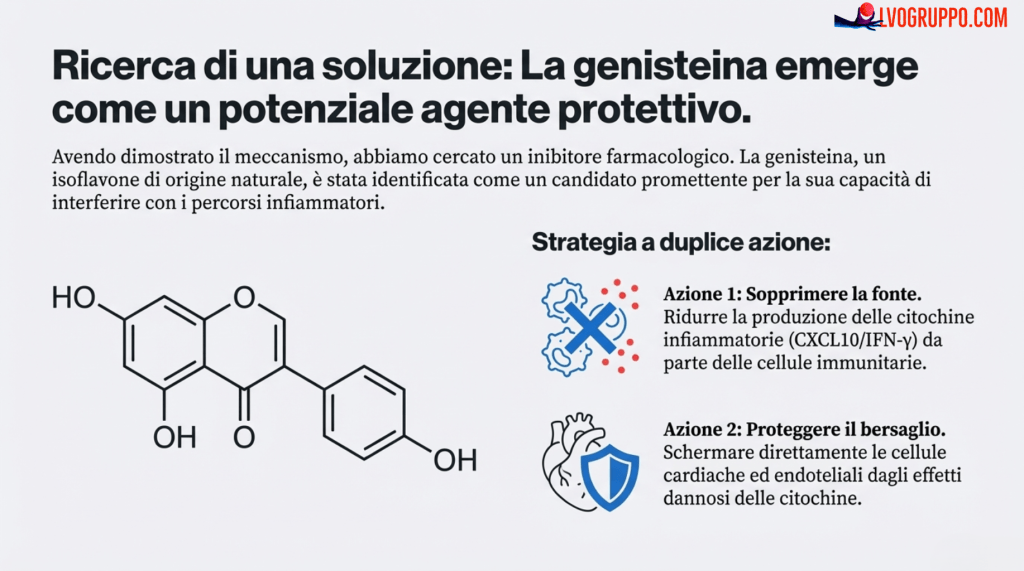
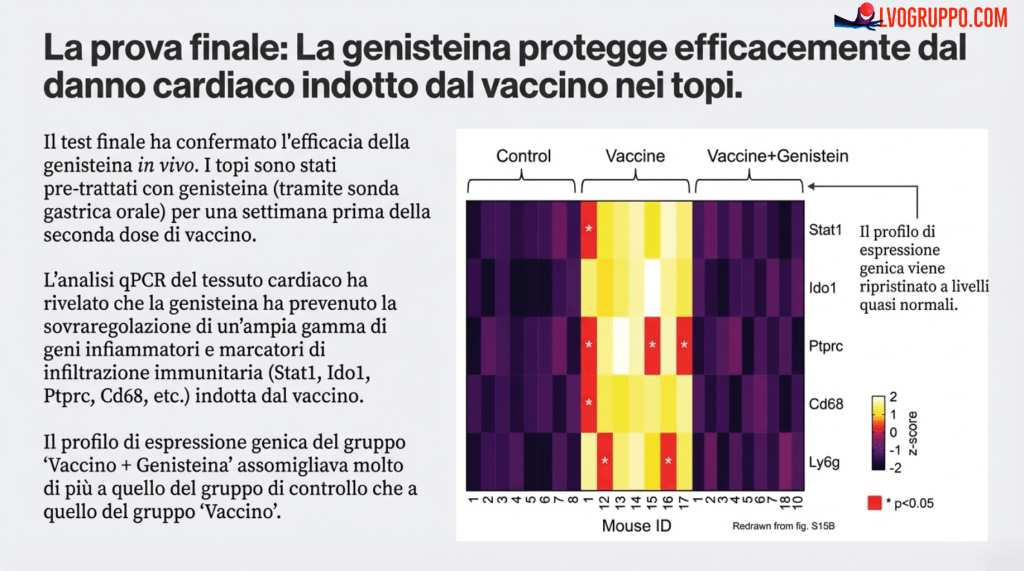
| Test di un Agente Terapeutico (Genisteina) | Esiste una sostanza in grado di mitigare questa reazione infiammatoria? | Sì. La Genisteina ha ridotto la produzione di citochine dalle cellule immunitarie (fig. S13) e ha protetto il cuore dal danno sia nei modelli cellulari (fig. S11, S12) che nei topi (fig. S15). |
3.3. Transizione al Capitolo Successivo
Mettendo insieme i pezzi del puzzle provenienti dai dati umani, dagli esperimenti cellulari e dai test sugli animali, i ricercatori sono stati finalmente in grado di disegnare un quadro completo del fenomeno.
4. Capitolo 4: Il Quadro Completo – Un Modello Unificato
Combinando tutte le prove raccolte, lo studio propone un modello di lavoro chiaro e unificato (rappresentato schematicamente in fig. S16) che spiega la sequenza di eventi biologici dalla puntura nel braccio fino al potenziale danno cardiaco.
4.1. La Sequenza degli Eventi: Dal Braccio al Cuore
Ecco la catena di eventi, passo dopo passo:
Iniezione: Il vaccino a mRNA viene somministrato nel muscolo del braccio.
Prima Risposta: Le cellule immunitarie “sentinella” presenti nel sito di iniezione, come i macrofagi, riconoscono il vaccino e vengono attivate, iniziando a produrre la prima citochina chiave: CXCL10.
Amplificazione: Il CXCL10 agisce come un segnale di richiamo per altre cellule immunitarie, i linfociti T. Una volta attivati, questi ultimi iniziano a produrre la seconda citochina fondamentale: l’IFN-γ.
Circolazione: Questo duo di citochine infiammatorie, CXCL10 e IFN-γ, entra nel flusso sanguigno e viene trasportato in tutto il corpo, raggiungendo anche il cuore.
Un Attacco su Due Fronti nel Cuore: Una volta giunte nel cuore, le citochine scatenano una reazione a catena:
Attivano le cellule che rivestono i piccoli vasi sanguigni (l’endotelio), rendendoli “appiccicosi” e favorendo l’infiltrazione di altre cellule immunitarie.
A concentrazioni più alte, danneggiano direttamente le cellule muscolari cardiache (i cardiomiociti) attivando in modo anomalo l’immunoproteasoma, che inizia a degradare componenti cellulari vitali.
Potenziale Intervento: Il modello identifica anche dei punti deboli in questa catena. Composti come la Genisteina hanno dimostrato di poter agire in più punti, sia riducendo la produzione iniziale di citochine da parte delle cellule immunitarie, sia proteggendo direttamente le cellule cardiache dal loro effetto dannoso.
4.2. Conclusione e Messaggio Finale
Questo studio è un esempio brillante di come funziona il metodo scientifico. Partendo da un’osservazione clinica (un raro effetto avverso), i ricercatori hanno utilizzato un approccio metodico e multi-livello—dai big data umani, ai modelli cellulari avanzati, fino alla validazione in organismi viventi—per trasformare un’associazione statistica in una profonda comprensione biologica.
Questo tipo di ricerca non solo chiarisce i meccanismi alla base di un fenomeno, ma apre anche la strada a potenziali interventi mirati per rendere terapie già estremamente efficaci e sicure, ancora più sicure per tutti. È una testimonianza del potere della scienza di illuminare l’ignoto e migliorare costantemente la salute umana.
Metodologie di Raccolta e Analisi dei Dati
1.0 Introduzione alle Metodologie dello Studio
Questo documento fornisce una descrizione tecnica dettagliata e rigorosa dell’architettura metodologica impiegata in questo studio per investigare i meccanismi molecolari e cellulari alla base della miocardite post-vaccinazione a mRNA. La strategia di ricerca è stata costruita su un approccio multi-livello, progettato per integrare sinergicamente diverse piattaforme analitiche. L’integrazione di approcci computazionali, modelli cellulari in vitro derivati da cellule staminali, analisi multi-omiche ad alta processività e validazione funzionale in modelli animali in vivo è stata fondamentale per formulare, testare e validare le ipotesi scientifiche. Partendo da un’analisi esplorativa di dati clinici e dataset pubblicamente disponibili, lo studio ha progressivamente focalizzato l’indagine su specifici mediatori e pathway molecolari, culminando in test preclinici di interventi terapeutici. Le sezioni seguenti illustrano in dettaglio ogni fase di questo processo, iniziando dall’analisi dei dati clinici e dei dataset pubblicati che ha posto le fondamenta dell’intera indagine.
2.0 Analisi di Dati Clinici e Dataset Pubblicati
L’approccio strategico iniziale dello studio si è basato sull’analisi di dati clinici e multi-omici già esistenti per generare ipotesi robuste e data-driven. L’interrogazione di database di farmacovigilanza, come il Vaccine Adverse Event Reporting System (VAERS), ha permesso di contestualizzare il fenomeno clinico. Parallelamente, la rianalisi mirata di dataset proteomici e trascrittomici pubblicati ha consentito di identificare segnali molecolari chiave associati sia alla risposta fisiologica alla vaccinazione sia alla condizione patologica della miocardite. Questa fase esplorativa è stata cruciale per formulare l’ipotesi centrale dello studio, ovvero il potenziale ruolo causale delle citochine CXCL10 e IFN-γ.
2.1 Interrogazione del Database VAERS (Vaccine Adverse Event Reporting System)
Per esplorare la natura e la frequenza dei report di miocardite a seguito della vaccinazione COVID-19 negli Stati Uniti, è stato interrogato il database VAERS attraverso il sistema CDC WONDER. I dati sono stati estratti applicando filtri specifici e rigorosi per isolare il set di dati di interesse.
I parametri di ricerca utilizzati sono stati i seguenti:
Sintomi: 10028606 (MYOCARDITIS)
Caratteristiche del vaccino: COVID-19 (COVID-19 VACCINE)
Produttore: MODERNA e PFIZER/BIONTECH
Dose: 1 dose e 2 dose
Stato/Territorio: The United States
I dati utilizzati per le analisi sono stati recuperati in data 28 dicembre 2023.
2.2 Rianalisi di Dati Proteomici Umani Post-Vaccinazione
È stata condotta una rianalisi dei dati proteomici plasmatici provenienti da due studi precedentemente pubblicati (Arunachalam et al., 2021 e Barmada et al., 2023) per identificare le citochine differenzialmente espresse sia in individui sani vaccinati sia in pazienti con miocardite. È stata eseguita una duplice analisi comparativa:
Soggetti sani: Sono state confrontate le concentrazioni medie di citochine plasmatiche misurate 1 giorno dopo la somministrazione della seconda dose di vaccino Pfizer rispetto ai livelli basali pre-vaccinazione. I risultati di questo confronto sono stati visualizzati come log2 fold change sull’asse Y della figura S1E.
Pazienti con miocardite: Sono state confrontate le concentrazioni medie di citochine plasmatiche in pazienti con miocardite post-vaccinazione con quelle di controlli vaccinati sani. I risultati di questo confronto sono stati visualizzati come log2 fold change sull’asse X della figura S1E.
**2.3 Rianalisi di Dataset **Trascrittomici
Sono stati rianalizzati due dataset trascrittomici a singola cellula per investigare le alterazioni dell’espressione genica nei monociti a seguito della vaccinazione.
Dataset** CITE-seq (GSE171964)** Il workflow computazionale ha previsto il processamento dei dati grezzi di CITE-seq, relativi a cellule mononucleate del sangue periferico (PBMCs) di individui sani prima e dopo la seconda dose di vaccino, scaricati dal database NCBI GEO. L’analisi ha seguito i seguenti passaggi: processamento dei dati con il pacchetto R Seurat 4.4.0; estrazione della popolazione cellulare di interesse, ovvero le cellule C8 CD14+/BDCA1+/PD-L1+; correzione degli effetti batch tra campioni utilizzando l’algoritmo Harmony 0.1.1; clustering cellulare tramite l’algoritmo di Louvain per identificare sottopopolazioni; e infine, identificazione dei geni differenzialmente espressi (DEG) tra il sottocluster di monociti C8 emerso dopo la vaccinazione e i monociti classici C3 presenti prima della vaccinazione.
Dataset** scRNA-seq (GSE230227)** Sono stati analizzati i dati grezzi di scRNA-seq di PBMCs ottenuti da individui sani e da pazienti con miocardite post-vaccinazione. Per l’analisi, i cluster identificati come monociti classici (I-VI) sono stati aggregati in un unico gruppo. Successivamente, i geni differenzialmente espressi tra gli individui sani e quelli con miocardite sono stati identificati utilizzando la funzione FindMarkers con i parametri min.pct = 0.1 e logfc.threshold = 0.1. Infine, è stata eseguita un’analisi di arricchimento Gene Ontology (GO) sui DEG identificati utilizzando il pacchetto Clusterprofiler.
Le scoperte emerse da queste analisi computazionali hanno non solo corroborato il ruolo centrale di CXCL10 e IFN-γ identificato a livello proteomico, ma hanno anche rivelato una complessa firma trascrittomica infiammatoria, caratterizzata dall’iperattivazione di pathway legati all’interferone e alla chemiotassi dei monociti. Questa convergenza di evidenze ha reso imperativa la validazione funzionale di questi meccanismi in modelli sperimentali controllati.
**3.0 Generazione e Coltura di Modelli Cellulari **In Vitro
Per studiare le interazioni cellulari e i meccanismi molecolari in un ambiente controllato e fisiologicamente rilevante, sono stati impiegati modelli cellulari avanzati derivati sia da cellule staminali pluripotenti indotte (iPSC) umane sia da cellule immunitarie primarie. L’utilizzo di cellule derivate da iPSC, come cardiomiociti, macrofagi e cellule endoteliali, ha permesso di ricreare le componenti cellulari chiave del cuore. L’integrazione con cellule immunitarie primarie ha consentito di modellare in modo più accurato le risposte immunitarie sistemiche e locali.
**3.1 Derivazione di Lignaggi Cellulari da **iPSC
I principali tipi cellulari cardiaci e immunitari sono stati differenziati da linee di iPSC umane utilizzando protocolli consolidati e specifici, come riassunto nella tabella seguente.
| Tipo Cellulare | Fattori e Condizioni Chiave di Differenziazione |
|---|---|
| Cardiomiociti (iPSC-CMs) | Protocollo di modulazione di Wnt con CHIR99021 e IWR-1. Purificazione metabolica in terreno privo di glucosio. Espansione con CHIR99021 prima dell’uso al giorno 30. |
| Macrofagi (iPSC-MACs) | Trattamento sequenziale con BMP4, Activin A, CHIR99021, seguito da VEGF, bFGF, SCF, SB431542, e poi citochine come IL-6, TPO, IL-3, e M-CSF. Selezione di monociti CD14+ al giorno 15 e maturazione finale con M-CSF. |
| Cellule Endoteliali (iPSC-ECs) | Differenziazione in terreno BPEL con CHIR99021, seguita da VEGF e SB431542. Isolamento di cellule CD144+ al giorno 10 e mantenimento in terreno EGM2. |
3.2 Generazione di Sferoidi Cardiaci 3D
Per simulare l’architettura tridimensionale e le interazioni cellulari del tessuto cardiaco, sono stati generati sferoidi cardiaci in co-coltura. Il protocollo prevedeva la dissociazione dei tre lignaggi cellulari derivati da iPSC (cardiomiociti, cellule endoteliali e macrofagi) e la loro successiva aggregazione in un rapporto definito di 7:2:1 (iPSC-CM : iPSC-EC : iPSC-MAC). Le cellule sono state seminate in piastre AggreWellTM800 in un terreno di coltura completo contenente 70% RPMI, 30% EGM2 e 50 ng/mL VEGF per promuovere la formazione di aggregati tridimensionali auto-assemblati.
3.3 Derivazione e Coltura di Cellule Immunitarie Primarie
Per complementare i modelli basati su iPSC, sono state utilizzate cellule immunitarie primarie ottenute da PBMCs umane.
Macrofagi: I monociti CD14+ sono stati isolati da PBMCs tramite selezione magnetica e coltivati per 6 giorni in presenza di M-CSF per promuovere la differenziazione in macrofagi maturi.
Linfociti T CD3+: Le cellule T CD3+ crioconservate sono state scongelate e coltivate in terreno di espansione ImmunoCult-XF supplementato con IL-2. Per evitare interferenze nei saggi successivi, l’IL-2 è stato rimosso dal terreno di coltura 48 ore prima dell’inizio degli esperimenti.
Questi sofisticati modelli cellulari sono stati successivamente sottoposti a una vasta gamma di tecniche analitiche per caratterizzare le risposte molecolari e funzionali agli stimoli indagati.
4.0 Analisi Trascrittomica e Proteomica di Massa
Per ottenere una visione globale e imparziale delle alterazioni molecolari indotte dal vaccino e dalle citochine nei modelli cellulari, sono state impiegate tecnologie “omiche” ad alta processività. L’analisi trascrittomica (Bulk RNA-seq) ha permesso di quantificare le variazioni nell’espressione genica a livello dell’intero genoma, mentre l’analisi proteomica basata su spettrometria di massa ha fornito una mappatura completa delle alterazioni a livello proteico, offrendo una visione complementare dei meccanismi biologici attivati.
4.1 Analisi Trascrittomica (Bulk RNA-seq)
Il flusso di lavoro per l’analisi trascrittomica è stato standardizzato per campioni sia umani che murini e ha compreso i seguenti passaggi chiave:
Isolamento dell’RNA: L’RNA totale è stato estratto dai campioni cellulari o tissutali utilizzando il kit Direct-zol RNA Microprep.
Sequenziamento: Le librerie di cDNA sono state sequenziate sulla piattaforma NovaSeq PE150 per generare letture paired-end.
Processamento** dei Dati:** Le letture grezze sono state sottoposte a trimming degli adattatori con Trim Galore. Successivamente, le letture sono state mappate sui genomi di riferimento (GRCh38 per l’uomo, mm10 per il topo) utilizzando l’allineatore STAR versione 2.7.10a per la quantificazione dei trascritti genici.
Normalizzazione e Correzione: I geni con un numero di letture inferiore a 5 in ≥90% dei campioni sono stati esclusi. I conteggi rimanenti sono stati normalizzati per tenere conto dei bias legati alla lunghezza genica e al contenuto di GC, utilizzando il pacchetto cqn. Gli effetti batch sono stati corretti con la funzione ComBat del pacchetto SVA.
Analisi Differenziale: I geni differenzialmente espressi (DEG) sono stati identificati applicando un modello lineare generalizzato implementato nel pacchetto edgeR. I valori di p sono stati corretti utilizzando la procedura di Benjamini-Hochberg, e una soglia di False Discovery Rate (FDR) ≤ 0.05 è stata considerata statisticamente significativa.
Analisi a Valle: Per interpretare il significato biologico dei DEG, sono state eseguite analisi di arricchimento di pathway KEGG e Gene Ontology (GO) utilizzando clusterProfiler per i dati umani e GAGE per i dati murini.
4.2 Spettrometria di Massa (LC-MS/MS) e Analisi Proteomica
La caratterizzazione del proteoma è stata eseguita mediante cromatografia liquida accoppiata a spettrometria di massa tandem (LC-MS/MS). Il processo è stato articolato in tre fasi principali.
Preparazione del Campione: I pellet cellulari sono stati lisati e le proteine estratte. I lisati proteici sono stati sottoposti a riduzione con DTT e alchilazione con acrilammide. Successivamente, le proteine sono state digerite enzimaticamente con **Tripsina/**LysC su colonne S-Trap micro spin per generare peptidi. I peptidi sono stati quindi eluiti e quantificati.
Acquisizione Dati (LC-MS/MS): I campioni di peptidi sono stati analizzati accoppiando un sistema di cromatografia liquida ad altissima pressione (UPLC Acquity M-Class) con uno spettrometro di massa Orbitrap Exploris 480. I peptidi sono stati separati su una colonna a fase inversa utilizzando un gradiente di 80 minuti e frammentati tramite dissociazione indotta da collisione ad alta energia (HCD).
Analisi dei Dati: I dati grezzi sono stati analizzati con la suite software Byonic per l’identificazione di peptidi e proteine, utilizzando un database Uniprot Homo sapiens. I parametri di ricerca includevano una tolleranza di 12 ppm sia per i precursori che per i frammenti, modifiche fisse (propionamide sulla cisteina) e variabili (es. ossidazione della metionina). Il tasso di falsa scoperta (FDR) è stato controllato all’1%. Un totale di 1.030 proteine identificate con almeno 50 conteggi totali in tutti i 12 campioni è stato utilizzato per le analisi a valle. L’analisi dell’espressione differenziale delle proteine è stata infine eseguita con il pacchetto limma, considerando significative le proteine con un valore di p.adjust < 0.05.
Le scoperte ottenute da queste analisi omiche sono state successivamente approfondite e validate attraverso saggi mirati a specifiche vie molecolari e funzioni cellulari.
5.0 Saggi Molecolari, Cellulari e Immunitari
Per validare le scoperte derivate dalle analisi omiche e per dissezionare meccanismi biologici specifici, è stata impiegata una suite di saggi mirati. Il passaggio strategico da approcci “omici” ad alta processività, volti a generare ipotesi, a saggi funzionali a bassa processività, progettati per testare tali ipotesi, è stato fondamentale. Questi test sono stati essenziali per quantificare l’attivazione di vie di segnalazione, misurare la secrezione di citochine, valutare l’espressione di marcatori di superficie e analizzare le interazioni funzionali tra popolazioni cellulari, fornendo prove meccanicistiche a supporto dello studio.
5.1 Quantificazione di Proteine e Citochine
Diverse tecniche sono state utilizzate per la quantificazione accurata di proteine e citochine specifiche in campioni biologici, come riassunto nella tabella sottostante.
| Tecnica | Descrizione e Applicazione |
|---|---|
| ELISA | Misurazione di NT-proBNP umano nei surnatanti cellulari, Troponina I cardiaca (cTnI) e IgG anti-Spike nel siero murino utilizzando kit commerciali. |
| Multiplex Cytokine Array | Analisi simultanea di un pannello di citochine nei surnatanti cellulari e nel siero murino tramite i pannelli Legendplex Human/Mouse Anti-Virus Response. |
| Western Blotting | Rilevamento e quantificazione di proteine specifiche (es. P-ERK, ERK, NF-κB) per analizzare l’attivazione delle vie di segnalazione. I segnali sono stati normalizzati su controlli di caricamento come GAPDH o β-actina. |
5.2 Analisi di Citometria a Flusso e Cell Sorting (FACS)
La citometria a flusso è stata impiegata per l’analisi quantitativa dell’espressione di proteine a livello di singola cellula. In particolare, è stata utilizzata per misurare l’espressione di marcatori di attivazione su iPSC-CMs (es. la fosforilazione di STAT1, P-STAT1) e di molecole di adesione su iPSC-ECs (es. ICAM-1, VCAM-1).
Inoltre, la tecnica di Fluorescence-Activated Cell Sorting (FACS) è stata utilizzata per separare fisicamente le diverse popolazioni cellulari (CD14+/CD144- MACs, CD14-/CD144+ ECs, CD14-/CD144- CMs) a partire da sferoidi cardiaci dissociati, per successive analisi trascrittomiche (RNA-seq) specifiche per ciascun tipo cellulare.
5.3 Saggi Funzionali Immunitari
Per studiare le interazioni dinamiche tra cellule immunitarie ed endoteliali, sono stati implementati specifici saggi funzionali in vitro.
Saggio di Adesione Cellulare: È stata quantificata l’adesione di cellule immunitarie (linee cellulari THP-1 e Jurkat), preventivamente marcate con il tracciante fluorescente CFSE, a un monostrato di cellule endoteliali (iPSC-EC) pre-trattate con citochine o medium condizionato.
Saggio di Transmigrazione dei Linfociti T: Utilizzando inserti di coltura Millicell con membrane porose, è stata misurata la migrazione di linfociti T (marcati con CFSE) dalla camera superiore verso la camera inferiore, contenente macrofagi precedentemente trattati con il vaccino, simulando il processo di chemiotassi.
5.4 Tecniche di Imaging e Espressione Genica
Immunofluorescenza: Questa tecnica è stata applicata per visualizzare la localizzazione di proteine specifiche all’interno di sferoidi cardiaci e sezioni di tessuto cardiaco murino. Il protocollo prevedeva la fissazione, permeabilizzazione, incubazione con anticorpi primari e secondari fluorescenti e montaggio con DAPI per la visualizzazione dei nuclei. Le immagini sono state acquisite con un microscopio confocale ZEISS LSM 880 tramite acquisizione di Z-stack per ottenere una risoluzione tridimensionale.
qRT-PCR: La reazione a catena della polimerasi quantitativa in tempo reale è stata utilizzata per misurare l’espressione relativa di geni specifici. Utilizzando la chimica SYBR Green, l’espressione genica è stata calcolata con il metodo del delta-delta Ct (2<sup>-ΔΔCt</sup>) e normalizzata sull’espressione di geni housekeeping stabili (RPL37A per i campioni umani, Rplp0 per quelli murini).
Il passo successivo è stato integrare queste scoperte molecolari con una valutazione diretta della funzionalità cardiaca, per comprendere l’impatto fisiologico dei meccanismi identificati.
**6.0 Valutazioni Funzionali e Fisiologiche Cardiache **In Vitro
Per determinare l’impatto funzionale diretto degli stimoli infiammatori sui cardiomiociti, è stato essenziale misurare parametri fisiologicamente rilevanti come la contrattilità e l’attività elettrica. Questi saggi forniscono endpoint quantitativi del danno cellulare e della disfunzione cardiaca, collegando le alterazioni molecolari a conseguenze a livello cellulare.
6.1 Saggi di Contrazione Basati su Video
La funzionalità contrattile è stata valutata utilizzando un sistema di imaging ad alta velocità.
Strumentazione: Una telecamera CMOS ad alta velocità (KP-FM400WCL) montata su un microscopio invertito è stata utilizzata per registrare video dei movimenti cellulari. L’analisi dei filmati è stata eseguita con il software dedicato SI8000C Analyzer.
Applicazioni:
Monostrati** di iPSC-CMs:** Sono stati registrati filmati del movimento sincrono del monostrato cellulare a una frequenza di 75 fotogrammi al secondo (fps).
Sferoidi Cardiaci: È stata registrata la contrazione dell’intero sferoide. Per l’analisi, il campo visivo è stato suddiviso in 9 Regioni di Interesse (ROI) per ottenere una misurazione robusta della contrattilità complessiva.
6.2 Registrazioni del Potenziale di Campo (MEA – Multielectrode Array)
L’attività elettrofisiologica dei cardiomiociti è stata misurata utilizzando la piattaforma Maestro MEA (Axion Biosystems), che rileva i potenziali di campo extracellulari generati da popolazioni di cellule cardiache. I parametri chiave misurati e analizzati tramite il Cardiac Analysis Tool includevano:
Potenziale di Campo: Durata del potenziale di campo (FPD), corretta per la frequenza di battito tramite la correzione di Fridericia (cFPD), e periodo del battito (BP).
Contrattilità: Registrata simultaneamente tramite misurazioni basate sull’impedenza.
Eventi Aritmici: Identificati e categorizzati manualmente sulla base delle registrazioni.
I dati sono stati presentati come variazione delle registrazioni post-trattamento rispetto al basale, e successivamente normalizzati sul gruppo di controllo (veicolo) per quantificare l’effetto specifico dei trattamenti.
Sebbene i saggi in vitro abbiano dimostrato una disfunzione a livello cellulare, non potevano catturare la complessità di una risposta immunitaria sistemica integrata o l’impatto sul tessuto cardiaco nel contesto di un organismo completo. Pertanto, la traslazione di queste scoperte in modelli murini in vivo è stata un passo indispensabile per validarne la rilevanza fisiopatologica.
7.0 Modelli Murini In Vivo e Analisi Correlate
Il ruolo dei modelli animali è stato cruciale per validare i meccanismi identificati in vitro in un contesto sistemico complesso. I modelli murini hanno permesso di valutare la risposta immunitaria integrata, il danno tissutale cardiaco e l’efficacia di potenziali interventi terapeutici in un organismo completo, conferendo così una maggiore rilevanza traslazionale ai risultati dello studio.
7.1 Modelli di Danno Miocardico
Sono stati impiegati due distinti modelli murini per investigare il danno miocardico.
Indotto da Vaccino mRNA: A topi maschi BALB/c o C57BL/6NCr è stato somministrato il vaccino BNT162b2 per via intramuscolare. Il protocollo prevedeva un regime a due dosi (Giorno 0 e Giorno 21). Su questo modello sono stati condotti studi di intervento, tra cui il blocco delle citochine tramite somministrazione di anticorpi neutralizzanti (anti-CXCL10, Bio X Cell BE0440; anti-IFN-γ, Bio X Cell BE0055) o dei rispettivi controlli isotipici, e il trattamento con genisteina.
Indotto da Citochine: Per studiare direttamente gli effetti acuti delle citochine, i topi hanno ricevuto un’iniezione endovenosa singola di un cocktail di CXCL10 e IFN-γ ricombinanti (0.1 mg/kg ciascuna). Questo modello è stato utilizzato per caratterizzare la cinetica del danno acuto (con il punto temporale di 4 ore scelto in quanto corrispondente al picco del danno) e per testare l’effetto protettivo della genisteina.
7.2 Analisi Istologica dei Tessuti Cardiaci
I cuori prelevati dai topi sono stati analizzati con tecniche istologiche standard per valutare l’infiltrazione immunitaria e le alterazioni tissutali.
| Tecnica Istologica | Dettagli Metodologici |
|---|---|
| Immunoistochimica (IHC) | Fissazione in paraformaldeide e inclusione in paraffina. Utilizzo del kit STAT Universal Animal IHC Kit. La procedura includeva recupero dell’antigene, blocco e incubazione con anticorpi primari (es. Ly6G, CD68, CD3). Quantificazione del numero di cellule positive per mm² analizzando dieci campi visivi casuali per sezione utilizzando ImageJ. |
| Immunofluorescenza (IF) | Fissazione in paraformaldeide e inclusione in OCT per il criosezionamento. Le sezioni sono state incubate con anticorpi primari e secondari fluorescenti e montate con DAPI per la visualizzazione dei nuclei. |
Queste analisi in vivo sono state supportate da un rigoroso approccio statistico, essenziale per garantire la validità e l’affidabilità di tutte le conclusioni tratte.
8.0 Analisi Statistica
L’approccio statistico generale dello studio è stato definito per garantire la robustezza e la riproducibilità dei risultati. Tutti i dati quantitativi sono stati derivati da un minimo di tre esperimenti indipendenti e sono presentati come media ± errore standard della media (SEM). L’analisi statistica è stata eseguita utilizzando il software Prism 9.
Per il confronto tra due gruppi è stato utilizzato il **t-test di **Student (a due code). Per i confronti tra più gruppi, è stata impiegata l’analisi della varianza a una via (ANOVA), seguita da test post-hoc appropriati per le comparazioni multiple, come il **test di **Dunn o il **test di **Holm-Sidak.


Lasciate il vostro commento