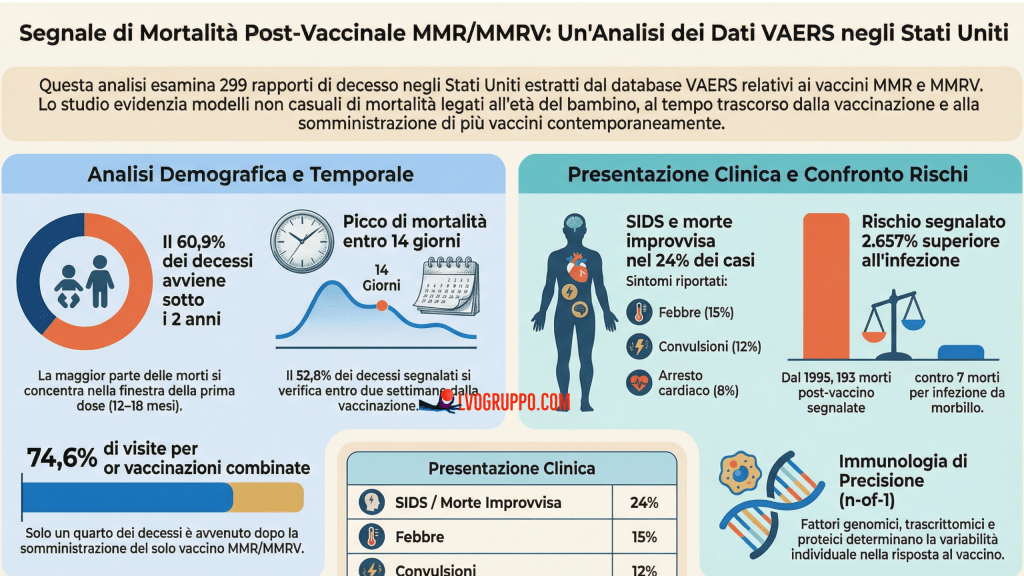
Un’analisi approfondita dello studio Cosgrove et al. (2025) sui decessi segnalati al VAERS dopo la vaccinazione contro morbillo, parotite e rosolia negli Stati Uniti
I risultati mostrano una concentrazione non casuale di morti tra bambini sotto i due anni, con un picco nella fascia 12–18 mesi — la finestra della prima dose raccomandata — e una forte addensamento temporale nelle prime due settimane post-vaccinali. Lo studio non stabilisce causalità, ma identifica un segnale di sicurezza che gli autori ritengono richieda indagini indipendenti e urgenti: sorveglianza attiva, studi autoptici con test virologici molecolari, e una revisione del consenso informato. Il presente articolo analizza criticamente questi dati, il loro contesto scientifico, i limiti metodologici e le implicazioni per la pratica clinica e la salute pubblica.
ACQUISTA LA TRADUZIONE IN ITALIANO DELLO STUDIO E SOSTIENI IL NOSTRO LAVORO
1. Il paradosso della sorveglianza passiva: guardare senza vedere
I vaccini contro morbillo, parotite e rosolia — nella doppia formulazione MMR (trivalente) e MMRV (quadrivalente, con varicella) — rappresentano uno degli interventi di salute pubblica più capillari al mondo. Negli Stati Uniti vengono somministrati sistematicamente a partire dai 12–15 mesi di età, con una seconda dose raccomandata tra i 4 e i 6 anni. L’efficacia immunologica di questi preparati nel prevenire epidemie è ben documentata e consolidata: il morbillo, prima dell’introduzione del vaccino, causava negli Stati Uniti tra 3 e 4 milioni di casi ogni anno, con migliaia di ricoveri ospedalieri e centinaia di decessi.
Tuttavia, nessuna efficacia — per quanto consolidata — può esimere le autorità sanitarie dall’obbligo di una sorveglianza post-marketing continua, rigorosa e intellettualmente onesta. È in questo quadro che si inserisce lo studio pubblicato nel 2025 da Kirstin Cosgrove e colleghi: una revisione sistematica di tutte le segnalazioni di decesso seguenti alla vaccinazione MMR/MMRV presenti nel database VAERS (Vaccine Adverse Event Reporting System) dalla sua istituzione, nel 1990, fino all’agosto 2025.
Il VAERS, gestito congiuntamente dai Centers for Disease Control and Prevention (CDC) e dalla Food and Drug Administration (FDA), funziona attraverso la segnalazione spontanea da parte di operatori sanitari, genitori e produttori di vaccini. Questo meccanismo di sorveglianza passiva presenta un vantaggio cruciale: intercettare segnali precoci di sicurezza in modo relativamente rapido, senza i costi logistici degli studi di coorte. Incorpora però anche un limite strutturale enorme: il sottosegnalamento cronico e sistematico degli eventi avversi. Un’indagine finanziata dagli stessi CDC, condotta da Lazarus et al. per l’Agenzia per la Ricerca e la Qualità in Sanità (AHRQ), ha stimato che meno dell’1% degli eventi avversi gravi viene segnalato ai sistemi nazionali di farmacovigilanza vaccinale.
Questo significa che i dati del VAERS non fotografano la realtà nella sua interezza, ma ne intercettano una frazione molto piccola e probabilmente non rappresentativa in modo uniforme.
Eppure, nonostante questa limitazione intrinseca e ben nota, i dati emersi dallo studio di Cosgrove et al. mostrano pattern di tale coerenza e sistematicità da imporre una riflessione seria.
Non è il numero assoluto delle segnalazioni a preoccupare in modo isolato, ma la loro distribuzione: per età, per intervallo temporale dalla vaccinazione, per presentazione clinica. Una distribuzione che, come vedremo, ha la forma di un segnale — non di un rumore.
Il VAERS è progettato per rilevare segnali di allerta precoci, non per stabilire causalità. Tuttavia, ignorare sistematicamente i segnali rilevati — senza procedere con indagini indipendenti e rigorose — equivale ad abdicare alla responsabilità fondamentale della farmacovigilanza. (Cosgrove et al., 2025)
Un segnale di sicurezza, in epidemiologia, non è una prova. È un’ipotesi che merita di essere testata con strumenti adeguati. Il problema non è che il VAERS generi un segnale — è che, troppo spesso, quel segnale non produce la risposta scientifica che dovrebbe.
2. La ricerca: chi, cosa, come
2.1 Gli autori e il contesto istituzionale
Lo studio, intitolato “Deaths Following MMR and MMRV Vaccination in the United States”, è firmato da un gruppo di ricercatori affiliati alla McCullough Foundation di Dallas, all’Advanced Biological Research Group di Jacksonville (Florida), a Neo7Bioscience e ad altri enti indipendenti. Gli autori dichiarano esplicitamente l’assenza di fondi esterni, affiliazioni industriali o conflitti di interesse — un elemento non marginale in un campo dove i finanziamenti possono orientare le priorità di ricerca e influenzare le conclusioni.
2.2 La metodologia
Il database VAERS è stato interrogato attraverso l’interfaccia pubblica MedAlerts.org, senza restrizioni di data iniziale, includendo tutte le segnalazioni di decesso associate a MMR o MMRV fino al 29 agosto 2025. La ricerca ha identificato globalmente 536 decessi associati a questi vaccini in tutto il mondo; di questi, 299 esplicitamente attribuiti agli Stati Uniti hanno costituito il campione analitico principale dello studio.
Le variabili analizzate comprendono: l’età al momento del decesso, l’intervallo temporale tra vaccinazione e morte (time-to-death), il sesso, la presenza di vaccini somministrati in concomitanza, le presentazioni cliniche riportate, e l’utilizzo dei servizi sanitari di emergenza (accesso al Pronto Soccorso, ricovero ospedaliero). I risultati sono presentati in modo puramente descrittivo, attraverso statistiche di sintesi: nessun tasso di incidenza è stato calcolato, nessun confronto è stato effettuato correggendo per la mortalità di base nella stessa fascia d’età, nessuna inferenza causale è stata formulata.
Questo approccio metodologico è onesto e scientificamente corretto. Il VAERS non è progettato per determinare la causalità, e presentare i suoi dati come tali sarebbe scorrecto. È invece progettato per identificare pattern che richiedono ulteriori indagini con strumenti epidemiologici più potenti: studi di coorte, record-linkage, sorveglianza attiva basata su cartelle cliniche elettroniche.
| Studio | Deaths Following MMR and MMRV Vaccination in the United States |
| Autori principali | Cosgrove K., Hulscher N., McCullough P.A. et al. |
| Anno di pubblicazione | 2025 |
| Fonte dati | VAERS (MedAlerts.org), dati estratti al 29 agosto 2025 |
| Campione analitico | 299 segnalazioni di decesso negli Stati Uniti |
| Campione globale | 536 decessi totali nel database VAERS mondiale |
| Tipo di analisi | Descrittiva — nessuna inferenza causale |
| Finanziamenti esterni | Nessuno dichiarato |
3. I dati: cosa dicono le 299 segnalazioni
3.1 Il profilo demografico: la prima infanzia al centro del segnale
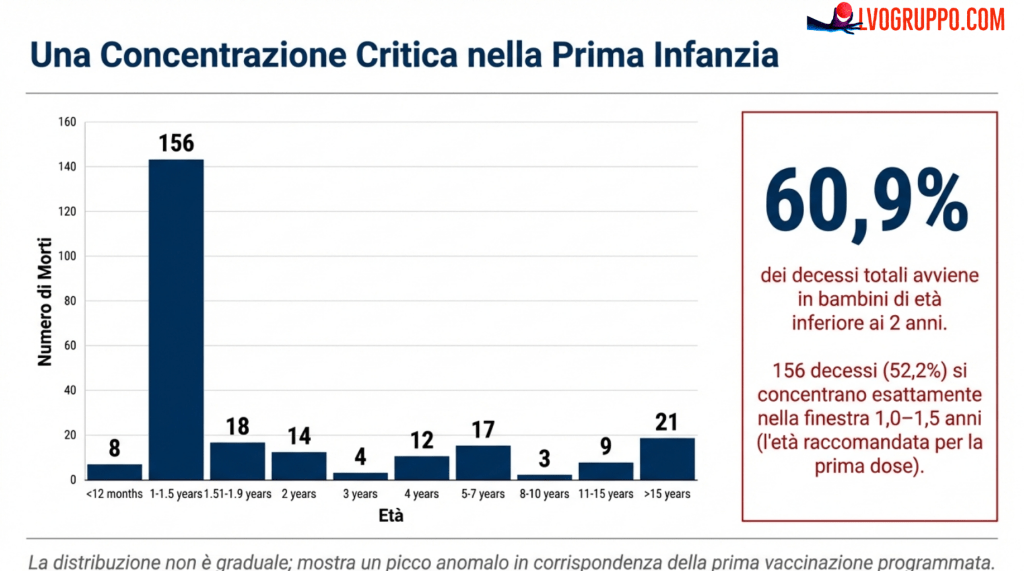
Il dato demografico più rilevante emerso dall’analisi è la concentrazione estrema dei decessi nella primissima infanzia. Su 299 segnalazioni statunitensi, 182 — il 60,9% del totale — riguardano bambini di età inferiore ai due anni. La fascia più colpita è quella tra 1,0 e 1,5 anni, con 156 decessi (il 52,2% dell’intero campione). Questa è esattamente la finestra temporale raccomandata per la somministrazione della prima dose di MMR.
Non stiamo parlando di una distribuzione casuale su tutte le fasce d’età pediatriche, ma di una concentrazione acuta attorno a un momento preciso del calendario vaccinale. Rispetto alle fasce successive, il distacco è netto: solo 14 decessi si registrano all’età di 2 anni, 4 a 3 anni, 12 a 4 anni, 17 tra 5 e 7 anni. Il picco drammatico attorno ai 12–18 mesi non ha un equivalente nelle altre fasi dello sviluppo infantile.
Si osserva inoltre una modesta prevalenza maschile (52,8% maschi contro 41,1% femmine, con il 6% di dati mancanti). La differenza di genere nella risposta immunologica innata è un campo di ricerca ancora largamente inesplorato nell’immunologia pediatrica — i meccanismi molecolari che potrebbero spiegare questa disparità meriterebbero indagini dedicate.
3.2 La distribuzione temporale: una concentrazione anomala nelle prime due settimane
Il secondo elemento di rilievo è la distribuzione temporale dei decessi rispetto alla data di vaccinazione. I risultati mostrano quello che in epidemiologia si chiama una distribuzione front-loaded: la grande maggioranza degli eventi si addensa nelle ore e nei giorni immediatamente successivi all’esposizione, anziché distribuirsi uniformemente nel tempo o decrescere progressivamente su mesi.
I dati specifici parlano in modo chiaro:
- 18 decessi si sono verificati nel giorno stesso della vaccinazione (Giorno 0) — compatibili con reazioni acute immediate, potenzialmente anafilattiche o da collasso sistemico rapido.
- 102 decessi nei giorni 1–7 successivi alla somministrazione, per un totale di 120 (il 40,1% del campione) nella prima settimana.
- 38 decessi tra l’ottavo e il quattordicesimo giorno, portando il totale delle prime due settimane a 158 decessi — il 52,8% del campione totale.
- 68,6% dei decessi avvenuti nella prima settimana, tra quelli con dati anagrafici disponibili, riguardava bambini nella fascia 1,0–1,5 anni.
Dopo i 14 giorni, i numeri calano in modo marcato: 28 decessi tra il giorno 15 e il 30, 21 tra il giorno 31 e il 90, 26 oltre il giorno 90. Sessantasei segnalazioni non disponevano di date sufficienti per calcolare l’intervallo temporale.
Una distribuzione così fortemente concentrata nelle prime settimane è incompatibile con l’andamento atteso se i decessi fossero eventi puramente casuali non correlati alla vaccinazione. Se i decessi fossero coincidenziali — dovuti cioè a cause indipendenti che si manifestano per caso subito dopo la vaccinazione — ci aspetteremmo una distribuzione più uniforme nel tempo, coerente con le cause di morte naturale in quella fascia d’età. Il fatto che oltre la metà si concentri nelle prime due settimane, con un picco acuto nelle prime 24 ore, rappresenta un pattern che in qualunque altro ambito della farmacologia clinica avrebbe già innescato protocolli di indagine urgente.
“La distribuzione temporale osservata è fortemente front-loaded, con la più alta concentrazione di decessi segnalati verificatasi subito dopo la vaccinazione. Questo pattern temporale riflette una mortalità non casuale, la cui sincronizzazione con l’età della prima dose e le presentazioni cliniche ricorrenti configura un segnale di sicurezza che richiede valutazione rigorosa, trasparente e pienamente indipendente.” (Cosgrove et al., 2025)
3.3 Il ruolo dei vaccini concomitanti: il peso del calendario multi-vaccinale
Un terzo elemento di notevole rilevanza riguarda la pratica comune di somministrare più vaccini nella stessa visita pediatrica — una pratica che semplifica la gestione del calendario, riduce il numero di accessi ambulatoriali e aumenta la copertura complessiva, ma che introduce variabili immunologiche complesse e ancora insufficientemente studiate.
Lo studio rileva che il 74,6% dei decessi segnalati (223 casi su 299) si è verificato in un contesto di vaccinazione combinata, dove MMR o MMRV erano somministrati insieme ad altri vaccini. Solo il 25,4% (76 casi) ha fatto seguito alla sola somministrazione di MMR/MMRV.
La distribuzione in base al numero di vaccini concomitanti mostra:
- 68 decessi (22,7%) con MMR/MMRV più un vaccino aggiuntivo
- 67 decessi (22,4%) con MMR/MMRV più due vaccini aggiuntivi
- 51 decessi (17,1%) con MMR/MMRV più tre vaccini aggiuntivi
- 27 decessi (9,0%) con MMR/MMRV più quattro vaccini aggiuntivi
- 7 decessi (2,3%) con MMR/MMRV più cinque vaccini aggiuntivi
- 3 decessi (1,0%) con MMR/MMRV più sei vaccini aggiuntivi
Questi dati sollevano interrogativi legittimi sulle interazioni immunologiche tra vaccini somministrati simultaneamente, sul carico antigenico cumulativo e sullo stress fisiologico imposto a un sistema immunitario in fase di maturazione. La sicurezza delle combinazioni multi-vaccinali — non dei singoli vaccini, ma delle loro interazioni quando somministrati insieme — è un settore che la letteratura scientifica ha finora esplorato in modo limitato. Non esistono studi clinici randomizzati di grandi dimensioni che valutino sistematicamente la sicurezza di combinazioni specifiche di sei o sette vaccini somministrati simultaneamente a bambini di 12–15 mesi.
Questo non significa che tali combinazioni siano necessariamente pericolose per la maggioranza dei bambini. Significa che esiste un vuoto di conoscenza che i dati presentati da Cosgrove et al. rendono urgente colmare, soprattutto per i sottogruppi di bambini che potrebbero presentare vulnerabilità immunogenetiche preesistenti.
3.4 Le presentazioni cliniche: un fenotipo che si ripete
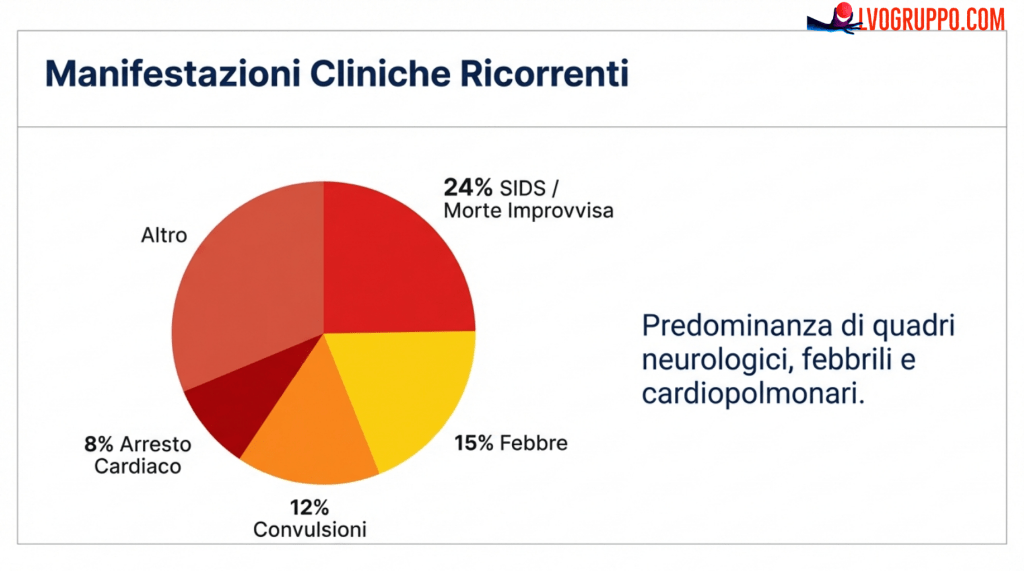
Le manifestazioni cliniche precedenti il decesso, pur eterogenee nei dettagli, mostrano pattern ricorrenti e clinicamente coerenti che non lasciano indifferenti. La categoria più frequentemente riportata è quella della Sudden Infant Death Syndrome (SIDS) o morte improvvisa inspiegata, presente nel 24% dei casi (72 segnalazioni). Cruciale è l’osservazione che il 68% di questi casi di SIDS (49 su 72) si è concentrato proprio nella fascia 1,0–1,5 anni, coincidendo in modo preciso con la finestra della prima dose.
Le altre presentazioni cliniche documentate: febbre nel 15% dei casi (45 bambini), convulsioni nel 12% (35 bambini), arresto cardiaco nell’8% (24 bambini), distress respiratorio nel 7% (20 bambini), encefalite nel 3% (10 bambini). Nel 23,7% delle segnalazioni era documentato un accesso al Pronto Soccorso; nel 25,4% un ricovero ospedaliero.
Questi numeri ci dicono qualcosa di importante: i decessi avvenivano spesso dopo una crisi acuta riconosciuta clinicamente, non come eventi silenti e improvvisi. Il tasso elevato di accessi al pronto soccorso e di ricoveri indica che qualcosa di osservabile clinicamente stava accadendo — convulsioni, difficoltà respiratorie, arresti cardiaci — prima del decesso. Non si trattava di bambini apparentemente sani che morivano nel sonno senza alcun segnale premonitore.
La predominanza di presentazioni neurologiche (convulsioni, encefalite) e cardiopolmonari (arresto cardiaco, distress respiratorio), unite all’elevata proporzione di SIDS nella fascia d’età della prima dose, configura quello che gli autori definiscono un «fenotipo fisiologico» ricorrente. Non un insieme eterogeneo di cause indipendenti e casuali, ma un pattern sistemico coerente con l’ipotesi di un’attivazione immunitaria intensa e mal regolata in un sottogruppo vulnerabile di bambini.
4. Il confronto più discusso: decessi da vaccino e decessi da morbillo
Il dato statistico che ha generato il maggiore dibattito — e che richiede la più attenta contestualizzazione — riguarda il confronto tra i decessi segnalati dopo la vaccinazione e quelli documentati per l’infezione naturale da morbillo nello stesso arco temporale.
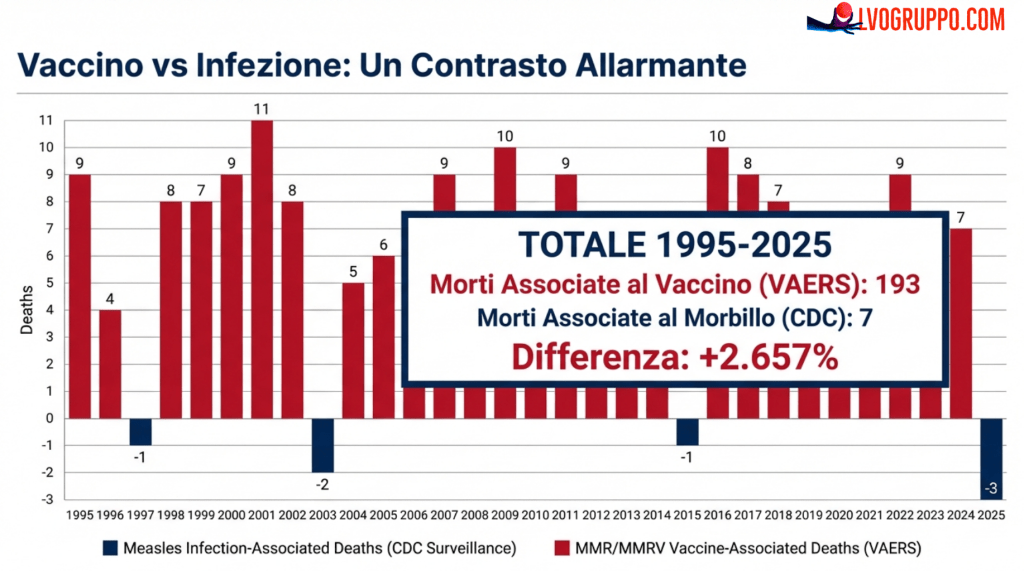
Dal 1995, il VAERS registra 193 decessi post-vaccinali MMR/MMRV con data di morte identificabile. Nello stesso arco temporale — trent’anni — la sorveglianza CDC documenta 7 decessi associati all’infezione naturale da morbillo: uno nel 1996, due nel 2003, uno nel 2015, e tre nel 2025. Lo studio calcola che si tratta del 2.657% in più di decessi segnalati dopo il vaccino rispetto all’infezione naturale.
4.1 Perché questo confronto va interpretato con estrema cautela
Prima di qualunque conclusione, è indispensabile chiarire che cosa questo dato non significa, e non può significare. Le 193 segnalazioni VAERS sono morti segnalate temporalmente in prossimità della vaccinazione, non morti causate dalla vaccinazione. Il VAERS, per sua natura e definizione, registra qualsiasi decesso avvenga dopo la somministrazione di un vaccino, indipendentemente dall’esistenza di un nesso causale accertato. Un bambino che muore per una causa completamente non correlata al vaccino — un’infezione intercorrente, un’anomalia cardiaca congenita non diagnosticata, un incidente — ma che era stato vaccinato pochi giorni prima, può finire nel database.
Al contrario, i 7 decessi per infezione naturale da morbillo sono stati oggetto di analisi clinica diretta e sono stati attribuiti al morbillo dopo accertamento diagnostico. Non si tratta quindi di una comparazione simmetrica: si confrontano segnalazioni non verificate con decessi confermati. Questo è un limite metodologico fondamentale che va tenuto presente in ogni lettura del dato.
Detto questo — e questa premessa è irrinunciabile — rimane il fatto che un segnale di questa entità non può essere liquidato senza indagine. Quasi 200 segnalazioni di decesso a fronte di 7 morti accertate da malattia in trent’anni è una disparità che richiede spiegazione. O queste segnalazioni sono in larga parte coincidenze statistiche, nel qual caso dovrebbe essere possibile dimostrarlo con studi di mortalità di background; oppure alcune di esse riflettono un legame causale reale, nel qual caso identificarle e quantificarle è un dovere etico oltre che scientifico.
4.2 Il fattore di sottosegnalamento
Gli autori applicano un Underreporting Factor (URF) conservativo di 31 volte, derivato dalle stime di Rose et al., per proiettare l’impatto reale del segnale. Applicando questo moltiplicatore ai 193 decessi segnalati si ottiene una stima di circa 5.983 eventi potenzialmente non segnalati nello stesso periodo. Il confronto con i 7 decessi da morbillo porta a una disparità proiettata dell’85.371%.
L’URF è uno strumento metodologico legittimo nell’epidemiologia della farmacovigilanza, utilizzato per stimare l’ordine di grandezza del sottosegnalamento nei sistemi passivi. Va però usato con consapevolezza critica: le proiezioni derivate da un URF rimangono stime ipotetiche con ampi margini di incertezza, non misure empiriche. Il valore di 31 utilizzato nello studio è definito dagli autori stessi come «conservativo»: alcune stime, come quella dell’indagine Lazarus dell’AHRQ, suggeriscono che il sottosegnalamento potrebbe essere ancora maggiore (inferiore all’1% degli eventi effettivi segnalati).
In ogni caso, le proiezioni URF andrebbero presentate esplicitamente come stime di scenario, utili per orientare la priorità della ricerca e delle risorse di sorveglianza, non come quantificazioni precise di un rischio accertato. L’articolo che state leggendo li presenta in questo spirito.
5. Il contesto epidemiologico del 2025: morbillo in ripresa
Il 2025 ha registrato negli Stati Uniti il numero più alto di casi di morbillo del XXI secolo: 2.255 casi confermati e 3 decessi, tutti documentati in soggetti non vaccinati. Questo dato è reale, significativo e non va minimizzato. La capacità del virus del morbillo di propagarsi rapidamente in popolazioni con copertura vaccinale insufficiente è scientificamente accertata. La comparsa di focolai in comunità con bassi tassi di vaccinazione è un fenomeno prevedibile e prevenibile.
In questo contesto, la discussione sulla sicurezza del vaccino MMR non avviene nel vuoto, ma in un momento in cui la percezione del rischio da morbillo è tornata concretamente attuale. Occorre quindi ragionare con precisione sulla bilancia rischi-benefici, senza cadere né nell’errore di ignorare i segnali di sicurezza né in quello opposto di amplificarli oltre la loro reale portata.
Lo studio di Cosgrove et al. solleva peraltro una questione metodologica specifica e legittima riguardo alla sorveglianza delle epidemie di morbillo: nelle comunicazioni pubbliche del CDC sui focolai, non viene sistematicamente operata una distinzione tra soggetti esplicitamente non vaccinati e soggetti con stato vaccinale ignoto o non documentato. Queste due categorie vengono spesso aggregate, il che può portare a una sovrastima della proporzione di non vaccinati tra i casi, distorcendo la percezione del rischio relativo tra vaccinati e non vaccinati. Per una corretta interpretazione epidemiologica, l’accertamento dello stato vaccinale in ogni singolo caso è un requisito metodologico di base, non un capriccio.
5.1 Il problema del morbillo da ceppo vaccinale
Un aspetto tecnico ma di notevole rilevanza clinica riguarda la natura viva attenuata del componente anti-morbillo presente nell’MMR. Questo tipo di preparazione vaccinale permette al virus attenuato di replicarsi in modo limitato nell’organismo, producendo una risposta immunitaria efficace. Un effetto collaterale di questa caratteristica è che il virus vaccinale può essere rilevato mediante test molecolare nei campioni respiratori per un periodo fino a 29–30 giorni dalla vaccinazione.
Le implicazioni pratiche sono rilevanti: le presentazioni cliniche del cosiddetto Vaccine-Associated Measles (VAM) — il morbillo da ceppo vaccinale — sono clinicamente indistinguibili da quelle del morbillo selvatico. La differenziazione richiede quindi l’uso del test molecolare MeVA RT-qPCR (Measles Virus Genotype A RT-qPCR), che il CDC stesso raccomanda come esame di conferma in presenza di positività sierologica nei 21 giorni successivi alla vaccinazione e in contesti di potenziale esposizione al virus selvatico.
Questo ha implicazioni sia per la sorveglianza delle epidemie — alcune «reinfezioni» in vaccinati potrebbero in realtà essere morbillo da ceppo vaccinale, non da ceppo selvaggio — sia per le indagini autoptiche sui decessi nel periodo post-vaccinale, dove il test molecolare dovrebbe essere sistematicamente incluso per distinguere la causa virale del decesso.
6. La variabilità biologica individuale: non tutti i bambini reagiscono ugualmente
Una delle dimensioni più scientificamente fertili dello studio — e forse la più ricca di implicazioni per la medicina del futuro — riguarda il riconoscimento che la risposta al vaccino MMR non è biologicamente uniforme tra gli individui. Il paradigma «n-of-all» — una dose standard, un protocollo uguale per tutti, un rischio identico per tutta la popolazione — ignora la realtà della diversità molecolare individuale, che la scienza post-genomica ha reso sempre più comprensibile e misurabile.
La letteratura scientifica sulla vaccinomics e adversomics — le discipline che studiano rispettivamente le basi genomiche della risposta immunitaria ai vaccini e i meccanismi molecolari degli eventi avversi — documenta come la risposta ai vaccini vivi attenuati sia determinata da una complessa architettura molecolare multi-omica. Tre livelli di analisi si intrecciano:
6.1 Determinanti genomici
Le varianti genetiche individuali costituiscono il substrato di base della risposta immunitaria. Polimorfismi nei loci HLA di classe I e II influenzano l’efficienza della presentazione dell’antigene al sistema immunitario adattativo: in parole semplici, determinano se il sistema immunitario di un bambino «riconoscerà» efficacemente il virus attenuato come un segnale di pericolo da cui produrre anticorpi protettivi.
Varianti nei geni delle citochine — come IL2, IL10RA, TNF — e nei sensori dell’immunità innata — TLR4, TLR7, DDX58 — modulano l’ampiezza e la qualità della risposta infiammatoria. In soggetti con specifiche combinazioni sfavorevoli di polimorfismi, lo stesso stimolo vaccinale che in un bambino genera protezione immunologica ottimale può innescare cascate infiammatorie disregolate e potenzialmente pericolose in un altro. La differenza non è nella forza del vaccino, ma nella biologia dell’ospite che lo riceve.
6.2 Determinanti trascrittomici
Oltre al DNA statico, la qualità della risposta dipende da come le istruzioni genetiche vengono eseguite in tempo reale. Processi come lo splicing alternativo e la ritenzione di introni nei geni STAT1 e STAT2 — entrambi fondamentali per la trasduzione del segnale dell’interferone — possono produrre proteine tronche o non funzionali. Il risultato è un fallimento nello stabilire il cosiddetto «stato antivirale», che in condizioni normali limita la replicazione del ceppo vaccinale attenuato e mantiene l’infezione vaccinale entro i confini di sicurezza per i quali il preparato è stato progettato.
In soggetti con queste vulnerabilità trascrittomiche, il virus vaccinale può replicarsi in modo meno controllato del previsto, con potenziali conseguenze che vanno dall’infezione persistente alle complicanze neuro-immuni. Studi di trascrittomica comparativa in coorti vaccinali potrebbero identificare questi pattern prima della somministrazione.
6.3 Determinanti proteomici ed evasione virale
Il terzo livello di analisi riguarda le proteine — i prodotti finali dell’espressione genica — e i meccanismi con cui il virus attenuato interagisce con il sistema immunitario dell’ospite. Il virus del morbillo attenuato non è biologicamente inerte: conserva meccanismi attivi di evasione immunitaria, inclusa la capacità di inibire la segnalazione dell’interferone di tipo I e di modulare l’attività del fattore di trascrizione NF-κB, uno dei regolatori centrali della risposta infiammatoria.
Questo può indurre una soppressione linfoide transitoria — un effetto immuno-depressivo temporaneo — che in soggetti con vulnerabilità preesistenti crea una finestra di opportunità per la replicazione virale incontrollata, con potenziali conseguenze sistemiche gravi. Le complicanze più severe documentate in questa categoria includono la Measles Inclusion-Body Encephalitis (MIBE) nei soggetti immunocompromessi — già riconosciuta come evento avverso nel foglietto illustrativo del vaccino — e considerazioni sulla Panencefalite Subacuta Sclerosante (SSPE) in relazione al ceppo vaccinale.
“Le prove provenienti dalla vaccinomics e dalla adversomics dimostrano che le risposte al vaccino MMR sono altamente eterogenee e plasmate dalla variazione inter-individuale a livello genomico, trascrittomico e proteomico. Questi dati evidenziano i limiti dei paradigmi di vaccinazione n-of-all e supportano un passaggio verso una precision immunology n-of-1 che incorpori la profilazione immunogenetica, la valutazione della via dell’interferone e una sorveglianza molecolare longitudinale.” (Cosgrove et al., 2025)
Il passaggio dall’immunologia di massa all’immunologia di precisione non è uno slogan anti-vaccinale, né una prospettiva irrealizzabile. È il naturale sviluppo scientifico di una medicina sempre più capace di stratificare i rischi individuali prima dell’intervento terapeutico. Analogamente a quanto accade in oncologia — dove la profilazione genomica del tumore determina la scelta del farmaco biologico più appropriato — la vaccinomics mira a identificare, prima della somministrazione, i bambini che presentano vulnerabilità molecolari specifiche che li pongono a rischio di reazioni gravi. Le basi scientifiche per questo approccio esistono già. Manca la volontà politica e le risorse per tradurle in protocolli clinici di screening routinario.
7. Il consenso informato: una lacuna che non possiamo ignorare
Forse l’aspetto più direttamente rilevante per la pratica clinica quotidiana — e più critico dal punto di vista della bioetica — riguarda il consenso informato. Lo studio di Cosgrove et al. solleva una questione precisa e documentabile: il foglietto illustrativo approvato dalla FDA per il vaccino M-M-R® II (la versione di Merck autorizzata negli Stati Uniti) elenca l’encefalite tra gli eventi avversi nella sezione dedicata all’esperienza post-marketing, ma non specifica che tali eventi possono avere esito fatale.
Il decesso è menzionato altrove nel documento, ma senza indicare che può verificarsi nel giro di giorni dalla somministrazione, e senza mettere in relazione questa possibilità con la finestra temporale in cui la grande maggioranza dei decessi segnalati al VAERS si concentra. Un genitore che legge il foglietto illustrativo prima di acconsentire alla vaccinazione del proprio figlio non riceve queste informazioni in modo esplicito e comprensibile.
Questo è un problema concreto di trasparenza, non di ideologia anti-vaccinale. Il consenso informato — principio fondamentale dell’etica medica codificato in tutti gli ordinamenti giuridici moderni e sancito dalla Convenzione di Oviedo sui diritti dell’uomo e la biomedicina — richiede che il paziente (o il suo rappresentante legale, nel caso di minori) sia informato dei rischi noti in modo sufficiente da permettere una decisione consapevole. La temporalità di un rischio — il fatto che un evento avverso grave possa manifestarsi entro ore o giorni dalla somministrazione, non solo settimane o mesi dopo — è un’informazione clinicamente rilevante che incide sulla capacità del genitore di riconoscere precocemente segnali di allarme.
Gli autori raccomandano esplicitamente che il foglietto illustrativo venga aggiornato per includere informazioni più precise sulla tempistica degli eventi avversi gravi segnalati al VAERS, con particolare riferimento alla finestra delle prime due settimane. Questa richiesta non è radicale: è conforme agli standard della farmacovigilanza moderna e dovrebbe trovare il sostegno di chiunque creda che la fiducia pubblica nella vaccinazione si costruisca sulla trasparenza, non sul silenzio o sulla minimizzazione.
Informare i genitori non significa spaventarli. Significa rispettarli come protagonisti delle decisioni sanitarie che riguardano i loro figli. La fiducia pubblica nelle istituzioni sanitarie si costruisce sulla coerenza tra i dati di sorveglianza e le informazioni rese accessibili al pubblico.
8. Cosa non dice lo studio — e perché è importante dirlo
Una corretta informazione richiede di precisare con altrettanta chiarezza ciò che questo studio non afferma, non può affermare, e non ha la pretesa di affermare:
- Lo studio non prova che il vaccino MMR/MMRV causa morti. Il VAERS è un sistema di segnalazione di associazioni temporali, non uno strumento di determinazione causale. Per stabilire la causalità sono necessari studi di coorte con controlli adeguati, analisi di mortalità di background corrette per età e stagione, studi di record-linkage su larga scala, e autopsie sistematiche con test virologici specifici. Nulla di tutto ciò è presente in questo studio.
- Lo studio non afferma che i vaccini MMR/MMRV debbano essere sospesi o ritirati. Gli autori richiedono indagini indipendenti, un aggiornamento del consenso informato e il passaggio a sistemi di sorveglianza attiva — non la cancellazione di un intervento di salute pubblica con oltre cinquant’anni di storia.
- Il confronto 2.657% non è una misura del rischio relativo reale. Mette a confronto segnalazioni non verificate (VAERS) con decessi clinicamente accertati (CDC), una comparazione strutturalmente asimmetrica che non può essere interpretata come stima del rischio.
- Le proiezioni derivate dall’applicazione dell’URF sono stime ipotetiche. Hanno valore per orientare la priorità della ricerca e delle risorse di sorveglianza, non per quantificare con precisione un rischio causale.
- Lo studio proviene da autori con posizioni note nel dibattito pubblico sui vaccini. Questo non ne invalida i dati, che provengono da fonti pubbliche verificabili (VAERS e CDC), ma impone una lettura critica della metodologia e dell’interpretazione, come per qualsiasi studio scientifico.
Queste precisazioni non sminuiscono la rilevanza del segnale — lo contestualizzano. E contestualizzare correttamente è il presupposto di qualunque risposta scientifica e politica adeguata. Il problema non è il segnale in sé: è la mancanza di risposte istituzionali proporzionate alla sua entità.
9. Cosa serve adesso: le raccomandazioni degli autori
Gli autori dello studio formulano raccomandazioni specifiche e metodologicamente fondate, che meritano di essere prese in considerazione indipendentemente dal giudizio che si ha sui singoli autori:
9.1 Transizione alla sorveglianza attiva
Il superamento della dipendenza dai sistemi di sorveglianza passiva come il VAERS — che, per definizione, non consentono di calcolare tassi di incidenza corretti per la popolazione di base — è una priorità riconosciuta dalla letteratura scientifica internazionale da oltre un decennio. I sistemi di sorveglianza attiva basati su record-linkage — che collegano le cartelle vaccinali ai registri di mortalità e ospedalizzazione — permettono di calcolare tassi di mortalità corretti per età e di confrontarli con la mortalità di background nella stessa fascia d’età, distinguendo le morti che avvengono casualmente nel periodo post-vaccinale dagli eventuali eccessi di mortalità causalmente associati alla vaccinazione.
Sistemi di questo tipo esistono già in alcuni contesti nazionali (in particolare in Danimarca, Finlandia e altri paesi scandinavi), e hanno consentito di identificare sia segnali di sicurezza reali sia coincidenze statistiche infondate. Investire nella loro implementazione su scala più ampia è una scelta di sanità pubblica responsabile.
9.2 Autopsie sistematiche con test virologici molecolari
Per ogni decesso in soggetti vaccinati con MMR/MMRV entro 30 giorni dalla somministrazione, gli autori raccomandano la conduzione di autopsie con test MeVA RT-qPCR, per distinguere il ceppo vaccinale dal virus selvatico e determinare se il morbillo — o un ceppo derivato dalla vaccinazione — abbia avuto un ruolo nella causa del decesso. Questo protocollo, ad oggi non sistematico nella pratica corrente, fornirebbe dati autoptici empirici piuttosto che classificazioni per esclusione come SIDS — una diagnosi che, per definizione, descrive l’assenza di una causa identificata, non la presenza di una causa specifica.
9.3 Aggiornamento del foglietto illustrativo
Il foglietto illustrativo del vaccino M-M-R® II dovrebbe essere aggiornato per riflettere in modo più accurato e completo il profilo di sicurezza emerso dalla sorveglianza post-marketing, includendo informazioni esplicite sulla temporalità degli eventi avversi gravi segnalati e sulla loro possibile evoluzione fatale. Questo non è un atto di pubblicità negativa verso il vaccino: è un requisito minimo di correttezza informativa verso i genitori che firmano il consenso alla vaccinazione.
9.4 Ricerca sulla stratificazione del rischio individuale
Investire nella ricerca sulla vaccinomics e adversomics per sviluppare strumenti di profilazione immunogenetica pre-vaccinale non è una proposta futuristica. Il sequenziamento dell’esoma — la porzione funzionale del genoma — è diventato tecnicamente accessibile e progressivamente più economico. Identificare le varianti genetiche associate a rischio elevato di reazioni severe prima della somministrazione permetterebbe di modulare il protocollo vaccinale per i soggetti a rischio: ritardare la somministrazione, adottare misure di monitoraggio post-vaccinale più intensive, o esplorare alternative immunizzanti per casi specifici.
10. Un sistema di sorveglianza all’altezza delle sue promesse
Ogni sistema di farmacovigilanza vale quanto la sua capacità di rispondere ai segnali che genera. Il VAERS è stato creato nel 1990 con un obiettivo preciso: intercettare precocemente segnali di sicurezza che potrebbero non essere visibili negli studi pre-approvazione, necessariamente limitati nella dimensione campionaria e nella durata del follow-up. Questo obiettivo rimane valido e prezioso.
Ma un sistema di sorveglianza passiva che genera segnali senza che questi producano risposte investigative proporzionate è un sistema che ha perso la sua funzione principale. Lo studio di Cosgrove et al. — che può essere discusso, criticato, integrato, ma non ignorato — pone questa domanda in modo diretto: i segnali di mortalità emersi dal VAERS nella fascia d’età 12–18 mesi sono stati oggetto di indagini indipendenti adeguate? Se sì, dove sono i risultati di tali indagini? Se no, perché no?
Sono domande legittime. Sono domande a cui la comunità scientifica e le autorità sanitarie hanno il dovere di rispondere in modo trasparente, con dati — non con rassicurazioni generiche.
Il morbillo rimane una malattia pericolosa, soprattutto per i più vulnerabili: bambini piccoli nei primi mesi di vita, soggetti immunocompromessi, donne in gravidanza. La vaccinazione di massa ha contribuito in modo determinante a ridurne la prevalenza e la mortalità. Nulla di quanto presentato in questo articolo intende mettere in discussione questa realtà.
Ma la coesistenza di questi fatti con la necessità di indagare i segnali di sicurezza non è una contraddizione: è la normalità della scienza medica matura. I migliori vaccini della storia — il salk per la poliomielite, il morbillo monovalente degli anni Sessanta, molti altri — hanno subito revisioni, aggiornamenti, modifiche di formulazione e di calendario nel corso del tempo, sulla base dei dati di sorveglianza post-marketing. Non perché fossero pericolosi in assoluto, ma perché la scienza si aggiorna.
11. Riflessione finale: fiducia, trasparenza e responsabilità
La fiducia pubblica nella vaccinazione — in qualsiasi vaccinazione — non può essere edificata sul silenzio riguardo ai rischi, né sulla sistematica minimizzazione dei segnali scomodi. Non si costruisce nemmeno attraverso l’esposizione strumentale e decontestualizzata di dati grezzi di sorveglianza passiva. Si costruisce sulla trasparenza, sulla volontà di indagare con rigore scientifico ogni segnale di sicurezza, e sulla capacità di comunicare onestamente sia i benefici documentati che i rischi ancora da chiarire.
Lo studio di Cosgrove et al. non è un manifesto anti-vaccinale. È un’analisi descrittiva di dati di sorveglianza pubblica che identificano pattern meritevoli di indagine urgente. Gli autori lo dicono esplicitamente nelle loro conclusioni: senza indagine indipendente, i dati non possono stabilire la causalità. Ma la mancanza di causalità accertata non è una ragione per non cercarla.
I genitori che portano i loro figli a vaccinarsi esercitano uno degli atti di cura più importanti che un genitore possa compiere in una società moderna. Hanno il diritto di farlo in modo pienamente informato, con la consapevolezza di ciò che il vaccino protegge e di ciò che, in una piccola frazione di casi, potrebbe non andare come previsto. I medici hanno il dovere di essere il tramite di questa informazione completa. Le autorità sanitarie hanno la responsabilità di garantire che i dati di sorveglianza siano investigati, che il consenso informato rifletta la realtà aggiornata, e che la fiducia pubblica sia rispettata con la stessa cura con cui si rispetta la salute pubblica.
Perché alla fine le due cose sono inseparabili.
La scienza non teme l’indagine. Non teme le domande difficili, né i dati scomodi. Ciò che la scienza non può permettersi — e che nessun sistema sanitario che si rispetti dovrebbe permettere — è il silenzio di fronte a un segnale che chiede di essere spiegato.
Nota metodologica dell’articolo: Questo articolo si basa principalmente sullo studio originale di Cosgrove et al. (2025), del quale riporta fedelmente i dati e le conclusioni. Le statistiche VAERS presentate sono dati descrittivi di segnalazioni, non misure di rischio causale. Il confronto con i decessi da morbillo e le proiezioni derivate dall’URF sono presentati con il loro preciso contesto metodologico. L’articolo non raccomanda la sospensione delle vaccinazioni MMR/MMRV e non costituisce parere medico.

Riferimenti bibliografici
Tutte le fonti sono quelle citate nello studio originale di Cosgrove et al. (2025). I collegamenti consentono l’accesso diretto alle pubblicazioni originali.
1. Hendriks J, Blume S. — La vaccinazione contro il morbillo prima dell’introduzione del vaccino combinato MMR. American Journal of Public Health, 2013; 103(8): 1393–1401. → Leggi la fonte
2. Centers for Disease Control and Prevention — Vaccini contro il morbillo: panoramica, indicazioni e raccomandazioni per i professionisti sanitari. → Leggi la fonte
3. Centers for Disease Control and Prevention — Sicurezza del vaccino MMR: effetti collaterali noti, monitoraggio post-marketing e raccomandazioni cliniche. → Leggi la fonte
4. Marin M, Broder KR, Temte JL, Snider DE, Seward JF et al. — Raccomandazioni dell’Advisory Committee on Immunization Practices (ACIP) per l’uso del vaccino combinato morbillo-parotite-rosolia-varicella. MMWR Recomm Rep, 2010; 59(RR-3): 1–12. → Leggi la fonte
5. Vaccine Adverse Event Reporting System (VAERS) — Informazioni istituzionali. U.S. Department of Health & Human Services; Centers for Disease Control and Prevention; Food and Drug Administration. → Leggi la fonte
6. Lazarus R. — Supporto elettronico per la sanità pubblica nel sistema di segnalazione eventi avversi da vaccini (ESP:VAERS): rapporto finale. Harvard Pilgrim Health Care, Inc., Grant R18 HS017045; Rockville, MD: Agency for Healthcare Research and Quality (AHRQ); 2010. → Leggi la fonte
7. National Vaccine Information Center — MedAlerts: interfaccia pubblica di ricerca nel database VAERS, con funzioni avanzate di filtro e analisi. → Leggi la fonte
8. Mathis AD, Raines K, Filardo TD et al. — Aggiornamento sul morbillo negli Stati Uniti, 1 gennaio–17 aprile 2025. MMWR Morb Mortal Wkly Rep, 2025; 74(14): 232–238. → Leggi la fonte
9. Gindler J, Tinker S, Markowitz L et al. — Mortalità acuta da morbillo negli Stati Uniti, 1987–2002. Journal of Infectious Diseases, 2004; 189 Suppl 1: S69–S77. → Leggi la fonte
10. Miller NZ. — Vaccini e morte improvvisa del lattante: un’analisi del database VAERS 1990–2019 e revisione della letteratura medica. Toxicology Reports, 2021; 8: 1324–1335. → Leggi la fonte
11. Hooker BS, Jablonowski C. — Aumento della mortalità associato alle vaccinazioni somministrate a lattanti di due mesi. Zenodo, 2026. (Preprint) → Leggi la fonte
12. Merck Sharp & Dohme LLC — Foglietto illustrativo approvato dalla FDA: vaccino vivo contro morbillo, parotite e rosolia (M-M-R® II). Revisione novembre 2025. → Leggi la fonte
13. Rose J. — Valutazione critica della farmacovigilanza VAERS: il sistema americano di segnalazione degli eventi avversi da vaccini è un sistema funzionante? Science, Public Health Policy and Law, 2021; 3: 100–129. → Leggi la fonte
14. Centers for Disease Control and Prevention — Casi di morbillo e focolai epidemici negli Stati Uniti: dati aggiornati 2025–2026. → Leggi la fonte
15. Washam MC, Leber AL, Oyeniran SJ, Everhart K, Wang H. — Dispersione (shedding) dell’RNA del vaccino contro il morbillo nei bambini dopo la vaccinazione MMR. Journal of Clinical Virology, 2024; 173: 105696. → Leggi la fonte
16. Centers for Disease Control and Prevention — Test MeVA RT-qPCR per il genotipo A del virus del morbillo: indicazioni cliniche e laboratoristiche. → Leggi la fonte
17. Montroy J, Yan C, Khan F et al. — Profilassi post-esposizione per la prevenzione del morbillo: una revisione sistematica. Vaccine, 2025; 47: 126706. → Leggi la fonte
18. Centers for Disease Control and Prevention — Panoramica del trattamento del morbillo: guida per i professionisti sanitari. Maggio 2025. → Leggi la fonte
19. Omeršel J, Karas Kuželički N. — Vaccinomics e adversomics nell’era della medicina di precisione. Journal of Clinical Medicine, 2020; 9(11): 3561. → Leggi la fonte
20. Whitaker JA, Ovsyannikova IG, Poland GA. — Adversomics: un nuovo paradigma per la sicurezza e la progettazione dei vaccini. Expert Review of Vaccines, 2015; 14(7): 935–947. → Leggi la fonte
21. Ovsyannikova IG, Haralambieva IH, Vierkant RA et al. — Aplotipi estesi dei geni LTA, TNF, LST1 e HLA e loro associazione con l’immunità indotta dal vaccino contro la rosolia. PLoS ONE, 2010; 5(7): e11806. → Leggi la fonte
22. Tanaka T, Narazaki M, Kishimoto T. — IL-6 nell’infiammazione, nell’immunità e nella malattia. Cold Spring Harbor Perspectives in Biology, 2014; 6: a016295. → Leggi la fonte
23. Ni T et al. — Regolazione genica mediata dalla ritenzione globale di introni durante l’attivazione delle cellule T CD4+. Nucleic Acids Research, 2016; 44: 6817–6829. → Leggi la fonte
24. Wendorf KA et al. — Panencefalite subacuta sclerosante: epidemiologia aggiornata. Clinical Infectious Diseases, 2017; 65(2): 226–232. → Leggi la fonte

Lasciate il vostro commento