Efficacia transitoria, rischi cardiaci documentati e un rapporto rischio-beneficio problematico nei bambini 5-11 anni: cosa rivela realmente lo studio su oltre 800.000 giovani inglesi
1. Introduzione: la vaccinazione pediatrica sotto la lente dei dati
La vaccinazione anti-COVID-19 nei bambini e adolescenti ha rappresentato uno degli aspetti più controversi della campagna vaccinale globale.

A differenza degli adulti e degli anziani, per i quali il rapporto rischio-beneficio appariva più favorevole, la popolazione pediatrica presentava fin dall’inizio caratteristiche epidemiologiche peculiari: un rischio bassissimo di forme gravi di COVID-19, tassi di ospedalizzazione marginali e mortalità praticamente assente.
In questo contesto, lo studio pubblicato dalla collaborazione OpenSAFELY sulla rivista Epidemiology (Volume 37, Numero 1, Gennaio 2026) assume un’importanza fondamentale: si tratta di uno degli studi osservazionali più ampi mai condotti sull’efficacia e la sicurezza del vaccino Pfizer-BioNTech (BNT162b2) nella fascia d’età 5-15 anni, basato sui dati sanitari di oltre 820.000 adolescenti e 140.000 bambini in Inghilterra.
SCARICA LA TRADUZIONE IN ITALIANO DELLO STUDIO
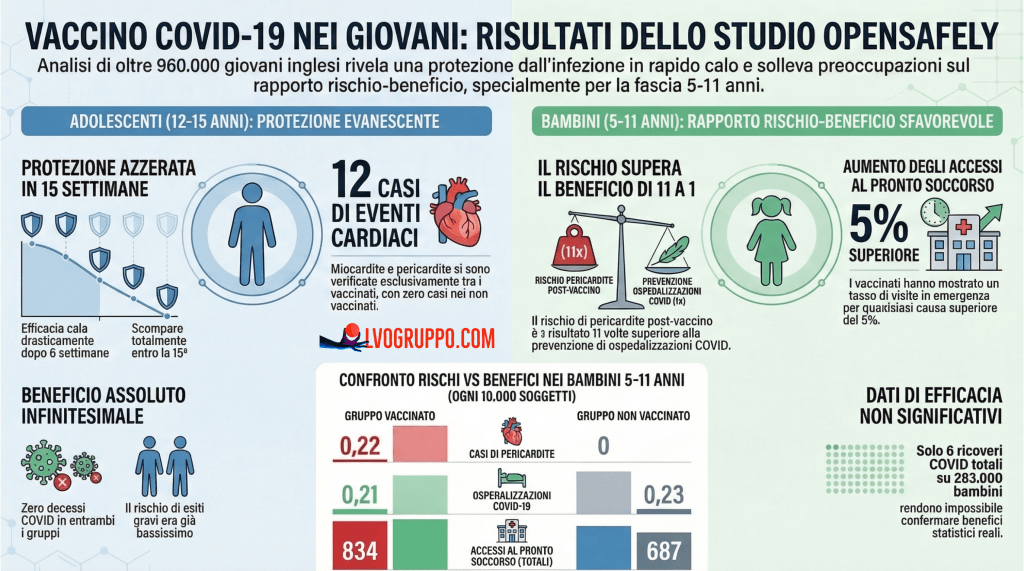
L’analisi dettagliata di questo studio rivela un quadro ben più articolato di quanto suggerito dalle conclusioni ufficiali. Se da un lato i ricercatori confermano alcuni benefici della vaccinazione negli adolescenti, dall’altro emergono criticità significative che meritano un’attenta disamina: una protezione dall’infezione che svanisce in poche settimane, eventi avversi cardiaci esclusivamente nei vaccinati, e – aspetto più rilevante – un rapporto rischio-beneficio che nei bambini più piccoli appare sfavorevole alla vaccinazione.
2. Lo studio OpenSAFELY: metodologia e popolazione
OpenSAFELY è una piattaforma di analisi dei dati sanitari che copre circa il 40% degli ambulatori di medicina generale inglesi, collegata ai dati nazionali di sorveglianza del coronavirus, ai ricoveri ospedalieri e ai registri dei decessi. Lo studio ha utilizzato un disegno osservazionale di coorte con abbinamento (matched cohort design), confrontando individui vaccinati con controlli non vaccinati abbinati per età, sesso, regione, livello di deprivazione socioeconomica ed evidenza di infezione precedente.
SCARICA LE SLIDES DI PRESENTAZIONE
2.1 Popolazione e periodo di studio
Lo studio ha incluso due coorti distinte:
Adolescenti (12-15 anni): 820.926 soggetti non vaccinati in precedenza, di cui 410.463 (80%) abbinati dopo la prima dose, e 441.858 adolescenti che avevano ricevuto la prima dose, di cui 220.929 (81%) abbinati per l’analisi della seconda dose.
Bambini (5-11 anni): 177.360 bambini idonei, di cui 141.711 (80%) abbinati per la prima dose, e 99.102 bambini che avevano ricevuto una seconda vaccinazione, di cui 66.231 (67%) abbinati.
Il programma vaccinale nel Regno Unito ha esteso la vaccinazione agli adolescenti 12-15 anni il 20 settembre 2021 (dose da 30 µg) e ai bambini 5-11 anni dal 4 aprile 2022 (dose ridotta da 10 µg). Gli individui clinicamente vulnerabili, che avevano accesso prioritario alla vaccinazione, sono stati esclusi dall’analisi per evitare confondimenti legati alla gravità di condizioni preesistenti.
2.2 Esiti valutati
Gli esiti di efficacia comprendevano: test positivo per SARS-CoV-2 (solo adolescenti, poiché i test gratuiti erano terminati quando i bambini sono diventati idonei), accesso al Pronto Soccorso per COVID-19, ricovero ospedaliero per COVID-19, ricovero in terapia intensiva e decesso per COVID-19.
Gli esiti di sicurezza includevano: accessi al Pronto Soccorso per qualsiasi causa, ricoveri ospedalieri non programmati, pericardite e miocardite. Le fratture sono state utilizzate come esito di controllo negativo per verificare la validità del disegno dello studio.
3. I risultati negli adolescenti (12-15 anni)
3.1 Efficacia contro l’infezione: modesta e rapidamente evanescente
Lo studio ha rilevato che la prima dose di vaccino ha ridotto il rischio di test positivo al SARS-CoV-2 del 26,3% (IRR 0,74; IC 95%: 0,72-0,75) rispetto ai non vaccinati. La seconda dose ha aggiunto un ulteriore beneficio, con un’efficacia del 33,1% (IRR 0,67; IC 95%: 0,65-0,69) rispetto alla singola dose.
Tuttavia, il dato più significativo riguarda la durata di questa protezione. L’analisi delle curve di incidenza cumulativa rivela che l’effetto protettivo si è attenuato drasticamente dopo le prime 6 settimane dalla vaccinazione, scomparendo completamente entro 14-15 settimane. A 20 settimane, i rischi per 10.000 individui erano praticamente identici: 1.961 (IC 95%: 1.932-1.990) nel gruppo vaccinato e 1.979 (IC 95%: 1.950-2.008) nel gruppo non vaccinato.
Questo dato solleva interrogativi fondamentali sull’utilità di un ciclo vaccinale che richiede richiami frequenti per mantenere una protezione già di per sé modesta, con i relativi rischi cumulativi associati a ciascuna somministrazione.
3.2 Protezione dagli esiti gravi: beneficio in un contesto di rischio già bassissimo
I dati relativi agli esiti gravi mostrano una riduzione degli accessi al Pronto Soccorso per COVID-19 (IRR 0,60; IC 95%: 0,37-0,97, efficacia 40%) e delle ospedalizzazioni (IRR 0,58; IC 95%: 0,38-0,89, efficacia 42,1%) dopo la prima dose.
È fondamentale, tuttavia, contestualizzare questi dati in termini assoluti: in un follow-up di oltre 95.000 anni-persona su 820.926 adolescenti, si sono registrati appena 72 accessi al Pronto Soccorso per COVID-19 e 90 ricoveri ospedalieri. I rischi a 20 settimane per 10.000 individui erano rispettivamente di 1,91 e 3,09 nei vaccinati contro 2,54 e 4,23 nei non vaccinati – differenze infinitesimali in termini assoluti.
Non si sono verificati decessi correlati al COVID-19 in nessuno dei gruppi analizzati. I ricoveri in terapia intensiva sono stati meno di 7 in totale (numero esatto oscurato per motivi di controllo della divulgazione statistica), tutti nel gruppo non vaccinato. Questo dato conferma che il COVID-19 rappresentava già prima della vaccinazione una minaccia estremamente limitata per questa fascia d’età.
4. I risultati nei bambini (5-11 anni): la criticità principale dello studio
È nella fascia d’età 5-11 anni che emergono le criticità più significative, riconosciute dagli stessi autori dello studio.

4.1 Eventi troppo rari per stime affidabili
In un follow-up di 32.476 anni-persona su 283.422 bambini abbinati (141.711 per gruppo), i dati relativi al COVID-19 sono stati i seguenti:
• Zero accessi al Pronto Soccorso per COVID-19
• Solo 6 ricoveri ospedalieri per COVID-19 in totale (3 per gruppo)
• Zero ricoveri in terapia intensiva per COVID-19
• Zero decessi correlati al COVID-19
Questi numeri sono così bassi da non consentire stime statistiche affidabili dell’efficacia vaccinale. Il rapporto dei tassi di incidenza (IRR) per l’ospedalizzazione risulta 1,00 (IC 95%: 0,20-4,96), ovvero compatibile con assenza di qualsiasi effetto.
4.2 Aumento degli accessi sanitari nei vaccinati
Un dato che merita particolare attenzione riguarda gli esiti di sicurezza. Nei bambini, l’incidenza degli accessi al Pronto Soccorso per qualsiasi causa è risultata più elevata dopo la prima vaccinazione rispetto al gruppo non vaccinato (IRR 1,05; IC 95%: 1,01-1,10). Anche l’incidenza di ricoveri ospedalieri non programmati era superiore nei vaccinati (IRR 1,10; IC 95%: 0,95-1,26), sebbene non statisticamente significativa.
I rischi a 20 settimane per 10.000 bambini erano: 834 accessi al Pronto Soccorso nel gruppo vaccinato contro 687 nel gruppo non vaccinato; 73 ricoveri non programmati nel gruppo vaccinato contro 60 nel gruppo non vaccinato. Questi dati suggeriscono un potenziale eccesso di morbilità associata alla vaccinazione, sebbene gli autori non escludano che possa essere in parte dovuto a differenze nei comportamenti di ricerca di assistenza sanitaria.
5. Gli effetti avversi cardiaci: miocardite e pericardite
Uno degli aspetti più rilevanti dello studio riguarda gli eventi cardiaci avversi. Tutti i casi di miocardite e pericardite rilevati durante il periodo di studio si sono verificati esclusivamente nei gruppi vaccinati. Nessun caso è stato registrato nei gruppi di controllo non vaccinati.
5.1 Incidenza negli adolescenti
Dopo la prima dose negli adolescenti sono stati registrati:
• 9 casi di pericardite (tasso: 0,31 per 10.000 o circa 31 per milione)
• 3 casi di miocardite (tasso: 0,08 per 10.000 o circa 8 per milione)
Dopo la seconda dose sono stati registrati ulteriori 3 casi di pericardite (0,21 per 10.000) e nessun caso di miocardite. È importante notare che i tassi riportati dallo studio OpenSAFELY (27 e 10 casi/milione rispettivamente dopo prima e seconda dose, combinando miocardite e pericardite) sono superiori a quelli segnalati dall’MHRA britannica (13 e 8 per milione), suggerendo un possibile sottoaccertamento nei sistemi di farmacovigilanza passiva.
5.2 Pericardite nei bambini: il dato più critico
Nei bambini 5-11 anni sono stati registrati 3 casi di pericardite dopo la prima dose (tasso: 0,22 per 10.000), tutti nel gruppo vaccinato. Gli autori dello studio riconoscono esplicitamente che “la riduzione del rischio di ospedalizzazione per COVID-19 nei bambini (−0,02 per 10.000) è stata inferiore all’aumento del rischio di pericardite (0,22 per 10.000)”.
In altre parole, secondo i dati dello stesso studio, il rischio di sviluppare pericardite a seguito della vaccinazione nei bambini era circa 11 volte superiore al beneficio in termini di prevenzione delle ospedalizzazioni per COVID-19.
5.3 Gravità degli eventi cardiaci
Lo studio riporta che nessuno degli eventi di miocardite o pericardite ha causato decessi. Negli adolescenti, la durata massima del ricovero ospedaliero è stata di 1 giorno in terapia intensiva e 2 giorni in reparto ordinario per la miocardite. Nei bambini, nessun caso di pericardite ha richiesto ospedalizzazione o terapia intensiva.
Tuttavia, questi dati riguardano solo il follow-up a breve termine (20 settimane). Gli effetti a lungo termine dell’infiammazione cardiaca in età pediatrica, incluse possibili sequele come fibrosi miocardica, aritmie e riduzione della funzione cardiaca, non sono stati valutati in questo studio e rimangono oggetto di preoccupazione nella comunità scientifica.
6. Analisi critica: i limiti dello studio riconosciuti dagli autori
Gli autori dello studio riconoscono apertamente diverse limitazioni che potrebbero influenzare l’interpretazione dei risultati:
6.1 Sottostima delle infezioni
I dati sui test positivi per SARS-CoV-2 sottostimano inevitabilmente la reale incidenza delle infezioni. Sebbene i test fossero gratuiti nel Regno Unito fino al 31 marzo 2022, molte infezioni asintomatiche e sintomatiche lievi non saranno state registrate. Questo limita la possibilità di valutare l’effettiva capacità del vaccino di prevenire l’infezione.
6.2 Possibile bias di accertamento
A partire da maggio 2021, i casi di miocardite e pericardite post-vaccinazione erano stati segnalati pubblicamente. Poiché le vaccinazioni nello studio sono avvenute dopo tale data, “esiste la possibilità di un bias di accertamento qualora le soglie diagnostiche fossero inferiori negli individui vaccinati rispetto a quelli non vaccinati”. In altre parole, i medici potrebbero essere stati più propensi a diagnosticare eventi cardiaci nei vaccinati, portando potenzialmente a una sovrastima dell’incidenza nei vaccinati.
Tuttavia, questo stesso meccanismo potrebbe operare in direzione opposta: genitori e tutori di bambini vaccinati potrebbero essere più attenti ai sintomi e più propensi a cercare assistenza medica, mentre quelli di bambini non vaccinati potrebbero sottovalutare sintomi simili. L’assenza totale di casi nei non vaccinati rende difficile distinguere tra una reale differenza di rischio e un diverso comportamento di ricerca di assistenza.
6.3 Dati raccolti di routine e non da ricerca attiva
A differenza degli studi clinici randomizzati, dove i casi vengono attivamente ricercati, questo studio si basa su dati raccolti di routine. “Potenziali differenze nei comportamenti di ricerca di assistenza sanitaria, da parte dei bambini o dei loro genitori o tutori, potrebbero significare che i bambini vaccinati sono più disposti o in grado di rivolgersi ai servizi sanitari rispetto ai bambini non vaccinati”. Ciò potrebbe portare a una sottostima sia dell’efficacia che della sicurezza del vaccino.
6.4 Confondenti non misurati
Nonostante l’accurato abbinamento per molteplici caratteristiche, “non si può escludere un bias dovuto a fattori confondenti non misurati”. Gli autori citano specificamente le differenze nel comportamento di testing tra vaccinati e non vaccinati, che potrebbero aver contribuito all’apparente attenuazione dell’efficacia, e le differenze nei comportamenti di ricerca di assistenza sanitaria.
6.5 Esclusione dei clinicamente vulnerabili
Lo studio ha escluso i bambini e adolescenti clinicamente vulnerabili, proprio quelli per i quali il rapporto rischio-beneficio potrebbe teoricamente essere più favorevole alla vaccinazione. “I nostri risultati potrebbero non essere generalizzabili a questo gruppo”, ammettono gli autori. Paradossalmente, le conclusioni dello studio si applicano principalmente ai soggetti sani, ovvero quelli che già presentavano il rischio più basso di esiti gravi da COVID-19.
6.6 Mancata valutazione degli eventi avversi post-infezione
Gli autori riconoscono di non aver “esaminato gli eventi avversi successivi all’infezione da SARS-CoV-2”. Questo significa che lo studio “non fornisce informazioni sulla sicurezza relativa della vaccinazione rispetto all’infezione”. In assenza di questo confronto, è impossibile determinare se la vaccinazione rappresenti effettivamente un’opzione più sicura rispetto all’immunità naturale acquisita attraverso l’infezione.
7. Il rapporto rischio-beneficio: cosa dicono realmente i dati
Mettendo insieme i dati presentati, emergono considerazioni cruciali sul rapporto rischio-beneficio della vaccinazione pediatrica.
7.1 Negli adolescenti (12-15 anni)
Gli autori concludono che negli adolescenti il rapporto rischio-beneficio “rimane favorevole alla vaccinazione”, principalmente per la riduzione delle ospedalizzazioni. I numeri assoluti mostrano:
Beneficio: riduzione di 1,14 ospedalizzazioni per COVID-19 ogni 10.000 vaccinati (prima dose).
Rischio: aumento di 0,31 casi di pericardite e 0,08 casi di miocardite ogni 10.000 vaccinati.
In termini puramente numerici, si prevengono circa 3 ospedalizzazioni per ogni caso di evento cardiaco avverso. Tuttavia, questo calcolo non considera:
• La diversa gravità degli esiti (le ospedalizzazioni per COVID-19 in questa fascia d’età erano tipicamente brevi e non gravi, mentre gli eventi cardiaci possono avere sequele a lungo termine)
• La protezione transitoria che richiede richiami, ognuno con rischi aggiuntivi
• L’assenza di decessi per COVID-19 in entrambi i gruppi, che indica che anche senza vaccinazione il rischio di esiti fatali era nullo
7.2 Nei bambini (5-11 anni): rapporto sfavorevole
Per i bambini più piccoli, i dati dello studio indicano chiaramente un rapporto rischio-beneficio sfavorevole alla vaccinazione:
Beneficio: riduzione di 0,02 ospedalizzazioni per COVID-19 ogni 10.000 vaccinati (statisticamente non significativa).
Rischio: aumento di 0,22 casi di pericardite ogni 10.000 vaccinati.
Inoltre, si è registrato un eccesso di 146 accessi al Pronto Soccorso per qualsiasi causa e 14 ricoveri ospedalieri non programmati ogni 10.000 bambini vaccinati rispetto ai non vaccinati.
Questi dati suggeriscono che per ogni eventuale ospedalizzazione per COVID-19 prevenuta (ammesso che ve ne sia stata), si sono verificati circa 11 casi di pericardite aggiuntivi, oltre a un eccesso di ricorso ai servizi sanitari.
8. La protezione che svanisce: un problema strutturale
Uno degli aspetti più sottovalutati ma critici dello studio riguarda la rapidità con cui svanisce la protezione conferita dal vaccino.
Le curve di incidenza cumulativa mostrano chiaramente che l’effetto protettivo contro i test positivi si manifesta principalmente nelle prime 2-6 settimane dalla vaccinazione, per poi attenuarsi progressivamente. A 14-15 settimane, le curve dei gruppi vaccinati e non vaccinati si sovrappongono: la protezione è completamente svanita.
Questo dato ha implicazioni pratiche significative:
1. Necessità di richiami frequenti: per mantenere anche una protezione modesta, sarebbero necessarie somministrazioni ogni 3-4 mesi, con relativi rischi cumulativi di eventi avversi.
2. Inefficacia come strumento di prevenzione a lungo termine: la vaccinazione non conferisce una protezione duratura, limitando la sua utilità come strategia di sanità pubblica.
3. Dubbi sull’immunità sterilizzante: l’assenza di una protezione duratura dall’infezione suggerisce che la vaccinazione non contribuisce significativamente a interrompere la catena di trasmissione del virus.
9. Conclusioni: oltre la narrativa ufficiale
Lo studio OpenSAFELY rappresenta un contributo importante alla comprensione dell’efficacia e della sicurezza della vaccinazione anti-COVID-19 nella popolazione pediatrica. Tuttavia, un’analisi critica dei dati presentati rivela un quadro più complesso e sfumato rispetto alle conclusioni sintetiche.
I principali elementi che emergono dall’analisi:
1. Protezione transitoria: l’efficacia contro l’infezione svanisce completamente entro 14-15 settimane, rendendo necessari richiami frequenti per mantenere anche benefici modesti.
2. Beneficio assoluto limitato: in una popolazione già a rischio bassissimo di esiti gravi (zero decessi per COVID-19 in tutti i gruppi), la riduzione del rischio assoluto è minima.
3. Eventi cardiaci esclusivi dei vaccinati: tutti i casi di miocardite e pericardite si sono verificati nei gruppi vaccinati, confermando un nesso causale con la vaccinazione.
4. Rapporto rischio-beneficio sfavorevole nei bambini piccoli: nei bambini 5-11 anni, il rischio di pericardite supera il beneficio in termini di prevenzione delle ospedalizzazioni, come riconosciuto dagli stessi autori.
5. Eccesso di accessi sanitari nei bambini vaccinati: l’aumento statisticamente significativo degli accessi al Pronto Soccorso nei bambini vaccinati solleva ulteriori interrogativi sulla sicurezza complessiva.
Questi dati invitano a una riflessione approfondita sulle politiche di vaccinazione pediatrica. Se per gli adolescenti il rapporto rischio-beneficio può essere considerato marginalmente favorevole in termini puramente numerici (sebbene con importanti caveat), per i bambini più piccoli i dati dello stesso studio suggeriscono che la vaccinazione potrebbe causare più danni di quanti ne prevenga.
È fondamentale che le decisioni di politica sanitaria tengano conto dell’intero spettro dei dati disponibili, inclusi i limiti e le criticità riconosciuti dagli stessi ricercatori, e non si basino su letture selettive o su conclusioni sintetiche che potrebbero non riflettere la complessità del quadro epidemiologico.

* * *
Nota metodologica: Questo articolo si basa esclusivamente sui dati e sulle metodologie riportate nello studio originale pubblicato dalla collaborazione OpenSAFELY. Le interpretazioni critiche presentate derivano da un’analisi dettagliata dei numeri forniti dagli autori e delle limitazioni da essi stessi riconosciute.
Bibliografia
[1] Andrews CD, Parker EPK, Horne E, Walker V, Palmer T, Schaffer AL, Green ACA, Curtis HJ, Walker AJ, Bridges L, Wood C, Speed V, Bates C, Cockburn J, Parry J, Mehrkar A, MacKenna B, Bacon SCJ, Goldacre B, Hernan MA, Sterne JAC, Hulme WJ; per conto della collaborazione OpenSAFELY. OpenSAFELY: Effectiveness of COVID-19 Vaccination in Children and Adolescents. Epidemiology 2026;37:141-151. DOI: 10.1097/EDE.0000000000001908
Articolo originale (accesso aperto): https://doi.org/10.1097/EDE.0000000000001908
Repository codice OpenSAFELY: https://github.com/opensafely/vaccine-effectiveness-in-kids
[2] NHS England. NHS rolls out COVID-19 jab to children aged 12 to 15. Settembre 2021.
[3] NHS England. NHS rolls out COVID vaccine to five million 5 to 11 year olds. Aprile 2022.
[4] Walter EB, Talaat KR, Sabharwal C, et al. Evaluation of the BNT162b2 COVID-19 Vaccine in Children 5 to 11 Years of Age. N Engl J Med 2022;386:35-46.
[5] Frenck RWJ, Klein NP, Kitchin N, et al. Safety, Immunogenicity, and Efficacy of the BNT162b2 COVID-19 Vaccine in Adolescents. N Engl J Med 2021;385:239-250.
[6] Mevorach D, Anis E, Cedar N, et al. Myocarditis after BNT162b2 Vaccination in Israeli Adolescents. N Engl J Med 2022;386:998-999.
[7] Husby A, Hansen JV, Fosbøl E, et al. SARS-CoV-2 vaccination and myocarditis or myopericarditis: population based cohort study. BMJ 2021;375:e068665.
[8] Marshall M, Ferguson ID, Lewis P, et al. Symptomatic Acute Myocarditis in 7 Adolescents After Pfizer-BioNTech COVID-19 Vaccination. Pediatrics 2021;148:e2021052478.
[9] Copland E, Patone M, Saatci D, et al. Safety outcomes following COVID-19 vaccination and infection in 5.1 million children in England. Nat Commun 2024;15:3822.
[10] Fatima M, Khan MHA, Ali MS, et al. Development of myocarditis and pericarditis after COVID-19 vaccination in children and adolescents: a systematic review. Clin Cardiol 2023;46:243-259.
[11] Das BB, Moskowitz WB, Taylor MB, Palmer A. Myocarditis and Pericarditis Following mRNA COVID-19 Vaccination: What Do We Know So Far? Children 2021;8:607.
SEGUI LE NOSTRE INIZIATIVE SUL SITO ISTITUZIONALE


Lasciate il vostro commento