
Secondo lo studio analizzato nell’articolo, l’origine del cancro risiederebbe in un’insufficienza cronica dei mitocondri all’interno delle cellule staminali, che le porta a trasformarsi in cellule staminali tumorali (CSC).
Analizziamo quindi il contenuto di questo interessantissimo Studio
SOSTIENICI CON L’ACQUISTO DELLA TRADUZIONE IN ITALIANO DELLO STUDIO CITATO – CLICCA QUI
La Connessione Mitocondrio-Cellula Staminale nel Trattamento del Cancro: Un Protocollo Ortomolecolare Ibrido
Introduzione: Una Nuova Prospettiva sulla Natura del Cancro
Il cancro rappresenta una delle sfide più complesse della medicina contemporanea. Nonostante i progressi nella comprensione della biologia tumorale e lo sviluppo di nuove terapie, i tassi di sopravvivenza per molte tipologie di cancro rimangono deludenti. Questa realtà solleva interrogativi fondamentali: stiamo affrontando questa malattia dalla prospettiva corretta? Le terapie convenzionali che utilizziamo da decenni sono realmente efficaci come pensiamo? Un gruppo internazionale di ricercatori ha recentemente proposto una teoria innovativa che potrebbe rivoluzionare il nostro approccio al trattamento oncologico: la teoria della connessione mitocondrio-cellula staminale (MSCC, dall’inglese Mitochondrial-Stem Cell Connection).
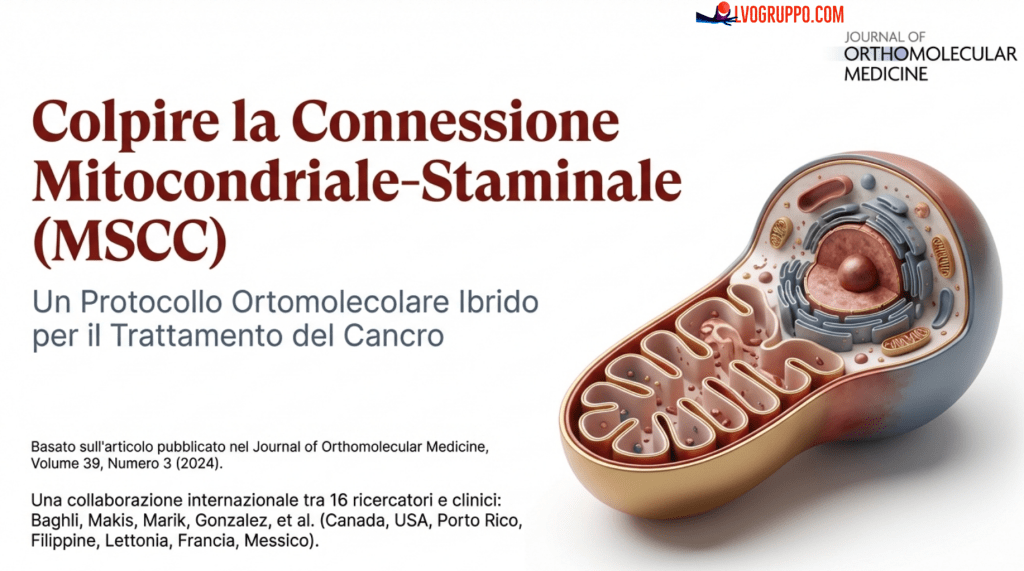
Questa teoria, pubblicata nel 2024 sul Journal of Orthomolecular Medicine, integra due concetti fondamentali già consolidati nella letteratura scientifica: la teoria metabolica del cancro e la teoria delle cellule staminali tumorali. La novità risiede nel fatto che la MSCC suggerisce che il cancro origini da un’insufficienza cronica della fosforilazione ossidativa (OxPhos) nelle cellule staminali, una condizione che porta alla formazione delle cellule staminali tumorali (CSC, Cancer Stem Cells) e, conseguentemente, alla tumorigenesi. In altre parole, il cancro non sarebbe primariamente una malattia genetica, come tradizionalmente sostenuto dalla teoria delle mutazioni somatiche, ma piuttosto una malattia metabolica che ha origine nelle cellule staminali.
Le implicazioni di questa prospettiva sono profonde e radicali.
Se il cancro è effettivamente una malattia mitocondriale che origina nelle cellule staminali, allora le terapie convenzionali che mirano esclusivamente al DNA delle cellule tumorali potrebbero essere fondamentalmente inadeguate. Questo potrebbe spiegare perché, nonostante i miliardi di euro investiti nella ricerca oncologica e lo sviluppo di nuovi farmaci, i miglioramenti nella sopravvivenza globale rimangono modesti. Uno studio ha dimostrato che negli ultimi quindici anni, le nuove terapie oncologiche hanno portato a un miglioramento della sopravvivenza globale di soli 2,4 mesi, mentre un’altra analisi ha riportato un miglioramento di appena 3,4 mesi negli ultimi trenta anni. Questi dati, per quanto shockanti, suggeriscono urgentemente la necessità di ripensare i paradigmi terapeutici attuali.
La Teoria della Connessione Mitocondrio-Cellula Staminale: Fondamenti Scientifici
Il Ruolo Centrale dei Mitocondri
Per comprendere appieno la teoria MSCC, è essenziale avere una conoscenza di base del ruolo dei mitocondri nella cellula. I mitocondri sono organelli cellulari comunemente noti come le “centrali energetiche” della cellula, poiché sono responsabili della produzione di adenosina trifosfato (ATP) attraverso un processo chiamato fosforilazione ossidativa. Questo processo è fondamentale per tutte le funzioni cellulari che richiedono energia. Tuttavia, i mitocondri non sono solo produttori di energia: svolgono ruoli cruciali nella regolazione del metabolismo, nella morte cellulare programmata (apoptosi), nella segnalazione cellulare e nella risposta allo stress ossidativo.
La teoria MSCC propone che un’alterazione della funzione mitocondriale, specificatamente dell’OxPhos, possa iniziare il processo di tumorigenesi in una o più cellule staminali normali. Quando i mitocondri di una cellula staminale non funzionano correttamente, la cellula è costretta a compensare il deficit energetico attraverso vie metaboliche alternative, come la glicolisi (il cosiddetto effetto Warburg). Questa compensazione, tuttavia, ha un costo: la cellula perde il suo normale controllo della crescita e può trasformarsi in una cellula staminale tumorale con capacità di autorinnovamento e differenziazione aberrante.
Le evidenze scientifiche supportano questa ipotesi. Studi hanno dimostrato che il grado di malignità è direttamente correlato con un numero significativamente inferiore di mitocondri e una minore capacità respiratoria totale nelle cellule tumorali. In altre parole, più le cellule tumorali sono aggressive e resistenti ai trattamenti, minore è la loro funzionalità mitocondriale. Questa relazione inversa tra malignità e funzione mitocondriale suggerisce che il ripristino della funzione mitocondriale potrebbe essere un obiettivo terapeutico cruciale nel trattamento del cancro.
SOSTIENICI CON L’ACQUISTO DELLE SLIDES IN ITALIANO DELLO STUDIO CITATO – CLICCA QUI
Le Cellule Staminali Tumorali: Il Cuore del Problema
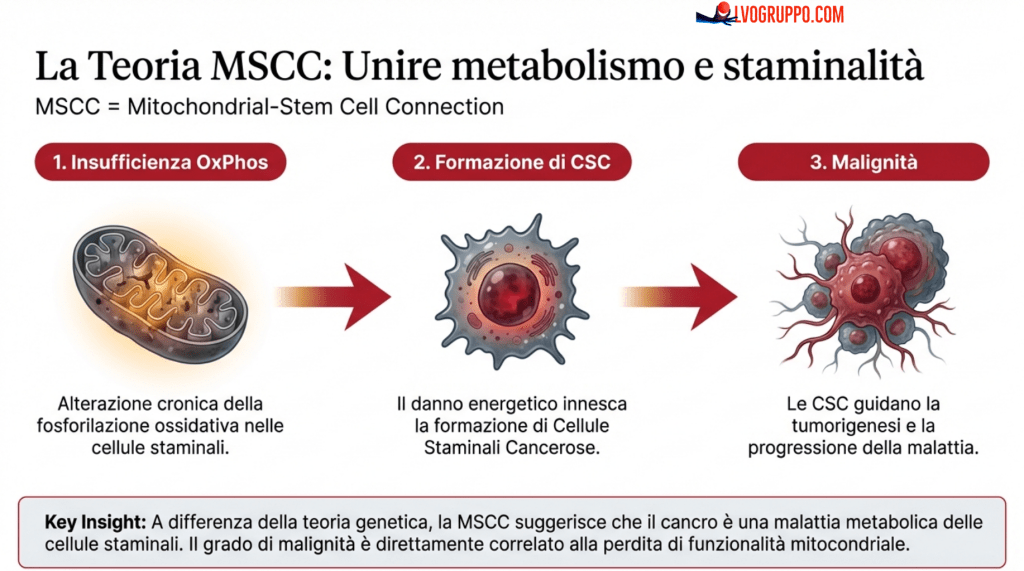
Le cellule staminali tumorali rappresentano una piccola popolazione all’interno della massa tumorale, ma la loro importanza non può essere sottovalutata. Queste cellule possiedono caratteristiche uniche che le rendono responsabili dell’iniziazione, della progressione e della recidiva del cancro. A differenza delle cellule tumorali “bulk” che costituiscono la maggior parte del tumore, le CSC hanno la capacità di autorinnovarsi indefinitamente, di differenziarsi in vari tipi cellulari tumorali e, soprattutto, di resistere alla chemioterapia e alla radioterapia convenzionali.
La resistenza delle CSC ai trattamenti convenzionali è uno dei principali motivi per cui i tumori spesso recidivano dopo il trattamento. Le terapie tradizionali, progettate per attaccare il DNA delle cellule tumorali a rapida divisione, non riescono a eliminare le CSC, che sono tipicamente in uno stato di quiescenza o divisione lenta. Questo è il motivo per cui, anche quando la chemioterapia sembra ridurre efficacemente la massa tumorale, le CSC possono sopravvivere e dare origine a nuovi tumori più resistenti e aggressivi.
Secondo la teoria MSCC, le metastasi, che rimangono la principale causa di mortalità oncologica, si sviluppano attraverso un processo di fusione ibrida tra le CSC e i macrofagi. Questa fusione crea cellule ibride con caratteristiche sia delle CSC (capacità di auto-rinnovamento e tumorigenicità) sia dei macrofagi (mobilità e capacità di migrazione). Le cellule ibride risultanti possono migrare dal tumore primario attraverso il corpo e stabilire nuove sedi tumorali metastatiche. Questa comprensione del processo metastatico ha implicazioni terapeutiche significative, poiché suggerisce che le strategie terapeutiche efficaci devono non solo eliminare le CSC, ma anche interferire con le interazioni tra CSC e macrofagi.

La Crisi delle Terapie Oncologiche Convenzionali
Limiti Fondamentali della Chemioterapia e della Radioterapia
Le terapie oncologiche convenzionali, inclusa la chemioterapia e la radioterapia, sono state sviluppate sulla base della teoria delle mutazioni somatiche, che considera il cancro primariamente una malattia genetica causata da mutazioni nel DNA. Di conseguenza, questi trattamenti sono progettati per danneggiare il DNA delle cellule tumorali, inducendo la loro morte. Tuttavia, questa strategia presenta limiti fondamentali che la teoria MSCC aiuta a chiarire.
In primo luogo, le terapie convenzionali non ripristinano la funzione mitocondriale alterata. Anzi, alcuni studi suggeriscono che la chemioterapia può ulteriormente alterare la funzione mitocondriale, contribuendo alla resistenza ai farmaci e alla tossicità sistemica. La doxorubicina, il trastuzumab e il sunitinib, farmaci chemioterapici ampiamente utilizzati, sono stati associati a disfunzioni mitocondriali significative che possono compromettere ulteriormente la salute delle cellule normali e contribuire agli effetti collaterali del trattamento.
In secondo luogo, le terapie convenzionali non riescono a eliminare le cellule staminali tumorali. Poiché le CSC sono tipicamente in uno stato di quiescenza e hanno meccanismi di riparazione del DNA più efficienti rispetto alle cellule tumorali bulk, esse sopravvivono ai trattamenti che mirano al DNA. Questa incapacità di colpire le CSC spiega perché molti pazienti rispondono inizialmente alla chemioterapia ma poi sperimentano recidive tumorali aggressive e resistenti ai trattamenti.
In terzo luogo, la chemioterapia e la radioterapia possono effettivamente promuove la progressione tumorale in alcuni casi. Uno studio sui tumori pancreatici ha dimostrato che la chemioterapia standard con gemcitabina, invece di ridurre il tumore, può aumentarne il peso e il numero delle metastasi. Analogamente, nel carcinoma epatocellulare, la chemioterapia con cisplatino può ridurre il volume tumorale ma aumentare la popolazione di CSC, potenzialmente preparando il terreno per una recidiva più aggressiva.
I Modesti Progressi nella Sopravvivenza Oncologica
I dati epidemiologici sulla sopravvivenza oncologica dipingono un quadro inquietante. Nonostante i progressi nella diagnosi precoce e lo sviluppo di nuovi farmaci, i miglioramenti nella sopravvivenza globale per molti tipi di cancro rimangono deludenti. L’analisi di Ladanie e colleghi ha rivelato che, nonostante l’approvazione di numerosi nuovi farmaci oncologici da parte della FDA tra il 2000 e il 2016, il miglioramento mediano nella sopravvivenza globale è stato di soli 2,4 mesi. Questo significa che, nonostante i costi enormi di questi nuovi trattamenti e i loro significativi effetti collaterali, il beneficio per i pazienti è minimo.
Del Paggio e collaboratori hanno condotto un’analisi ancora più ampia, esaminando l’evoluzione degli studi clinici randomizzati nell’era dell’oncologia di precisione. I loro risultati hanno mostrato un miglioramento della sopravvivenza globale di appena 3,4 mesi negli ultimi trenta anni. Questo dato è particolarmente significativo considerando gli investimenti miliardari nella ricerca oncologica e lo sviluppo di terapie mirate e immunoterapie che erano attese rivoluzionare il trattamento del cancro.
Questi risultati non significano che la ricerca oncologica sia stata vana o che non si siano fatti progressi in alcuni ambiti specifici.
Tuttavia, suggeriscono che il paradigma attuale, basato sul targeting delle mutazioni genetiche e sul danneggiamento del DNA, potrebbe essere intrinsecamente limitato. Se il cancro è effettivamente una malattia metabolica che origina nelle cellule staminali, come suggerisce la teoria MSCC, allora è necessario un cambiamento di paradigma fondamentale nel nostro approccio terapeutico.
Il Protocollo Ortomolecolare Ibrido: Una Nuova Strategia Terapeutica
Principi Fondamentali del Protocollo
Alla luce della teoria MSCC e delle evidenze scientifiche sui limiti delle terapie convenzionali, un gruppo internazionale di ricercatori ha sviluppato un protocollo ortomolecolare ibrido che mira specificamente alla connessione mitocondrio-cellula staminale. Il termine “ortomolecolare” si riferisce all’uso di molecole naturali, vitamine e minerali per ripristinare l’equilibrio molecolare del corpo. Il termine “ibrido” indica che il protocollo combina sostanze ortomolecolari, farmaci riutilizzati (off-label) e interventi aggiuntivi come la dieta e lo stile di vita.
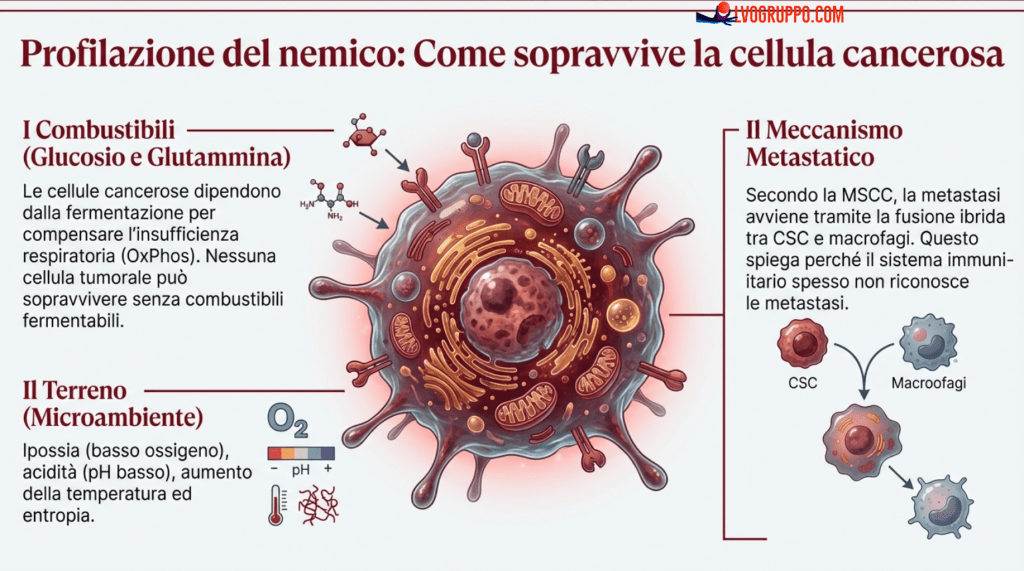
L’obiettivo del protocollo è duplice. Da un lato, mira a potenziare l’OxPhos nelle cellule sane, proteggendo così le cellule normali e promuovendo la salute complessiva. Dall’altro, mira a indurre uno stress ossidativo selettivo nelle cellule tumorali, in particolare nelle CSC, portando alla loro morte. Questo approccio sfrutta la differenza fondamentale tra cellule sane e cellule tumorali: le cellule sane possono gestire lo stress ossidativo attraverso i loro mitocondri funzionanti, mentre le cellule tumorali, con i loro mitocondri disfunzionali, sono vulnerabili all’induzione di stress ossidativo.
Il protocollo si basa su sette raccomandazioni terapeutiche principali che agiscono in modo sinergico e additivo per colpire simultaneamente diversi aspetti della biologia tumorale: potenziamento dell’OxPhos, inibizione dei carburanti fermentabili (glucosio e glutammina), targeting delle CSC e delle metastasi.

La Terapia con Vitamina C: Evidenze e Applicazioni
Meccanismi d’Azione Antitumorali
Le proprietà antitumorali della vitamina C sono note da oltre cinquant’anni, ma solo recentemente la scienza ha iniziato a comprenderne i meccanismi d’azione. La vitamina C esercita effetti citotossici sulle cellule tumorali sia in vitro che in vivo, e in alcuni studi è risultata più efficace della chemioterapia standard nell’indurre l’apoptosi nelle cellule di cancro del colon. Ancora più significativo è il fatto che la vitamina C, a differenza della chemioterapia, non aumenta la popolazione di CSC e può effettivamente ridurla.
Uno studio cruciale ha confrontato gli effetti della vitamina C ad alte dosi con la chemioterapia standard (gemcitabina) nel cancro pancreatico. I risultati hanno mostrato che la vitamina C da sola riduceva significativamente il peso tumorale e il numero delle metastasi, mentre la chemioterapia da sola aumentava entrambi i parametri. Nel carcinoma epatocellulare, la vitamina C ha dimostrato di ridurre sia le CSC che il volume tumorale, mentre la chemioterapia standard con cisplatino, pur riducendo il volume tumorale (sebbene in misura minore rispetto alla vitamina C), aumentava le CSC.
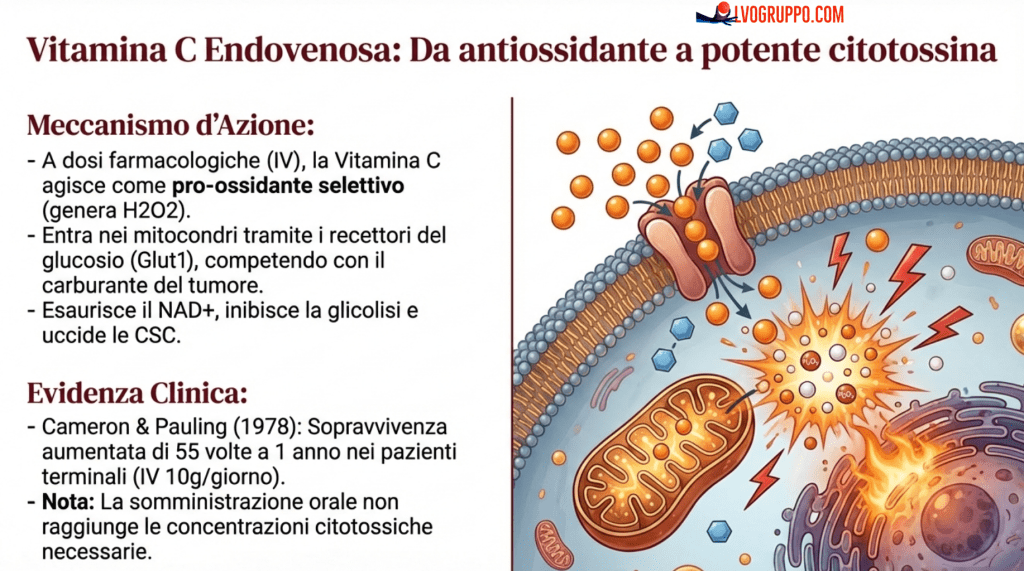
I meccanismi attraverso cui la vitamina C esercita i suoi effetti antitumorali sono molteplici. La vitamina C può penetrare direttamente nell’ambiente intracellulare tumorale, ridurre lo stress ossidativo, mirare ai mitocondri delle cellule tumorali e indurre la morte cellulare, incluse le metastasi. Inoltre, l’ambiente intracellulare alcalino delle cellule tumorali, con un pH compreso tra 7,1 e 7,7, massimizza la proliferazione delle cellule tumorali. La vitamina C, attraverso il suo pH acido, potrebbe disattivare queste adattamenti ambientali, compromettendo la crescita delle cellule tumorali e inibendo la progressione tumorale.
Un meccanismo particolarmente interessante riguarda la capacità della vitamina C di aumentare la produzione di ATP aumentando il flusso di elettroni mitocondriali, ripristinando così la funzione respiratoria cellulare e l’apoptosi. Questo effetto è cruciale perché molte cellule tumorali hanno una produzione di ATP compromessa a causa della disfunzione mitocondriale. Ripristinando la funzione mitocondriale, la vitamina C può riattivare i normali meccanismi di morte cellulare programmata che sono soppressi nelle cellule tumorali.
Targeting delle Cellule Staminali Tumorali
Una delle scoperte più significative riguardanti la vitamina C è la sua capacità di colpire ed eradicare le CSC. Studi hanno dimostrato che la vitamina C può indurre l’apoptosi nelle CSC, proteggere contro l’ipossia e l’infiammazione, e inibire la proliferazione incontrollata delle cellule tumorali e la diffusione metastatica. Inoltre, la vitamina C può indurre una polarizzazione dei macrofagi M2 (pro-tumorali) in macrofagi M1 (antitumorali), un effetto particolarmente rilevante per inibire la diffusione metastatica poiché i macrofagi M2 sono implicati nelle metastasi.
La vitamina C ha anche la capacità di inibire la glicolisi e la sintesi del glutammato, due vie metaboliche cruciali per le cellule tumorali. Può limitare specificamente la sintesi di glutammina inibendo la glutammina sintetasi (GS), portando a una diminuzione del livello di glutatione e a un aumento delle specie reattive dell’ossigeno (ROS), con conseguente morte cellulare. L’inibizione della GS può invertire il fenotipo dei macrofagi M2 e promuovere la polarizzazione dei macrofagi M1, riducendo il glutammina intracellulare e impedendo l’assorbimento di glutammina, con conseguente eliminazione delle metastasi.
Studi Clinici e Casi di Remissione
I pionieri della terapia con vitamina C per via endovenosa, Cameron e Pauling, hanno osservato tempi di sopravvivenza migliorati per molti tipi di cancro (polmone, stomaco, colon, mammella, rene, retto e vescica). Hanno osservato che i tempi di sopravvivenza erano moltiplicati per 55 dopo un anno nei pazienti terminali trattati con iniezioni endovenose di ascorbato: il 22% nel gruppo trattato e lo 0,4% nel gruppo di controllo in pazienti considerati incurabili dopo il trattamento standard. Il loro protocollo consisteva in un’iniezione endovenosa di 10 g/giorno per circa 10 giorni, seguita da somministrazione orale.
La Mayo Clinic ha tentato di riprodurre questi risultati, ma ha sostituito la vitamina C endovenosa con quella orale, ottenendo risultati negativi come previsto, poiché le concentrazioni plasmatiche e quindi gli effetti della vitamina C sono molto più bassi con la supplementazione orale. Questo errore metodologico è stato erroneamente interpretato come una refutazione dell’efficacia della vitamina C nel cancro, quando in realtà dimostrava solo l’importanza della via di somministrazione.

La clinica Riordan e collaboratori hanno pubblicato numerosi casi clinici che documentano regressioni tumorali in pazienti che hanno ricevuto vitamina C endovenosa. Inoltre, Li e colleghi hanno dimostrato che l’assunzione regolare di vitamine antiossidanti (vitamine A, C ed E) può ridurre la mortalità per cancro. Tuttavia, l’azione antiossidante della vitamina C dovrebbe essere utilizzata principalmente nella prevenzione del cancro, poiché gli antiossidanti possono talvolta promuovere la crescita tumorale.
La Terapia con Vitamina D: Un Alleato Metabolicamente Attivo
Effetti Antitumorali della Vitamina D
La vitamina D ha dimostrato effetti antitumorali in vitro e in vivo per quasi tutti i tipi di cancro. Come la vitamina C, la vitamina D mira ai mitocondri migliorando il metabolismo e regolando la respirazione mitocondriale. Può anche colpire le CSC e le metastasi, e inibire le vie della glicolisi e della glutaminolisi. Questi effetti pleiotropici rendono la vitamina D un componente prezioso di qualsiasi protocollo metabolico per il cancro.
È stato osservato che la supplementazione giornaliera di vitamina D può ridurre la mortalità totale per cancro, sebbene questo effetto non sia stato osservato per dosi infrequenti e bolus. I pazienti oncologici sono spesso carenti di vitamina D e possono beneficiare di una terapia efficace con rischi minimi. Un caso clinico documenta un paziente anziano con cancro pancreatico avanzato che non poteva sottoporsi a chemioterapia, radiazione o intervento chirurgico. Il paziente ha ricevuto una dose giornaliera di 50.000 UI di vitamina D3 per 9 mesi e ha sperimentato un periodo inaspettatamente prolungato di progressione della malattia senza recidiva, superando di gran lunga ciò che ci si aspetterebbe dalla chemioterapia convenzionale.
Studi di Prevenzione e Mortalità
Chandler e colleghi hanno dimostrato un effetto preventivo della supplementazione di vitamina D nei pazienti con indice di massa corporea (BMI) normale, mostrando una riduzione del 37% nell’incidenza di cancro metastatico (24 tumori nel gruppo della vitamina D e 39 nel gruppo placebo), con una riduzione della mortalità per cancro del 42% (38 persone nel gruppo della vitamina D e 68 nel gruppo placebo). La dose utilizzata era di 2000 UI/giorno, che è l’apporto giornaliero raccomandato per un individuo sano.
Un recente studio clinico randomizzato e controllato sulla supplementazione di vitamina D (2000 UI/giorno di vitamina D3 versus placebo) ha rilevato che i pazienti con cancro gastrointestinale che erano immunoreattivi per p53 hanno sperimentato una riduzione significativa della recidiva o della morte associata alla supplementazione di vitamina D durante un follow-up di quasi sei anni. Meta-analisi di studi osservazionali per almeno 12 diversi tipi di cancro hanno riportato correlazioni inverse tra i livelli sierici di 25-idrossivitamina D [25(OH)D] e l’incidenza di cancro.
Lo Zinco: Un Oligoelemento antitumorale
Protezione Mitocondriale e Effetti Antitumorali
La supplementazione di zinco è stata raccomandata come possibile trattamento aggiuntivo per il cancro. Lo zinco protegge specificamente i mitocondri dai danni causati dalle specie reattive dell’ossigeno che sono generate come sottoprodotti della respirazione mitocondriale. È stato dimostrato che la supplementazione di zinco induce il trasporto mitocondriale del piruvato, la fosforilazione ossidativa e la produzione di ATP sia nelle cellule normali che in quelle sottoposte a stress ossidativo tossico in vitro.
Nelle cellule di cancro ovarico umano, lo zinco induce la degradazione dei mitocondri e ripristina l’apoptosi, specialmente se introdotto insieme a ionofori dello zinco. Lo zinco può sopprimere le proprietà simili alle cellule staminali del cancro orale e delle cellule di cancro mammario in vitro, ridurre l’espressione dei marcatori della staminalità delle cellule tumorali e aumentare la sensibilità alla chemioterapia nelle cellule di cancro del colon. Un eccesso di zinco può bloccare irreversibilmente la produzione energetica delle cellule tumorali, causare perdita di NAD⁺ e inibire la glicolisi cellulare.
Esistono un totale di 151 pubblicazioni che confermano il legame tra carenza di zinco e malignità. La carenza di zinco è implicata in molti tumori, inclusi quelli dell’esofago, del fegato, del polmone, della mammella, del colon e altri. Lo zinco mostra tossicità verso le cellule tumorali senza mostrare effetti collaterali sulle cellule sane e la carenza è correlata negativamente con i tassi di sopravvivenza. Analogamente alla vitamina C, lo zinco può avere un effetto pro-ossidante specifico sulle cellule tumorali.
Farmaci Riutilizzati: L’Ivermectina
Un Antiparassitario con Proprietà Antitumorali
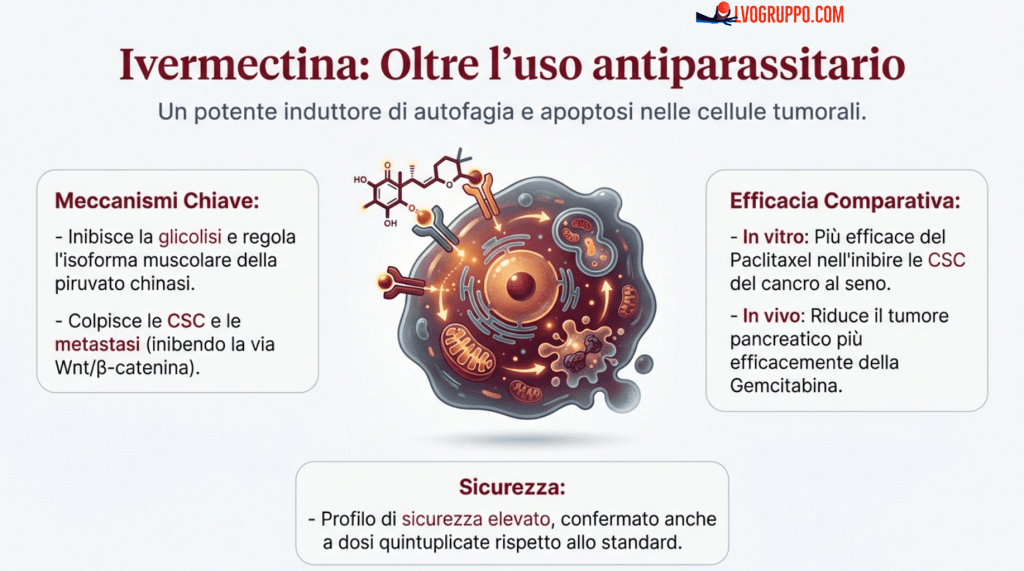
L’ivermectina, un antiparasitario derivato da un batterio chiamato Streptomyces avermitilis, possiede proprietà antitumorali significative. Questo farmaco induce l’autofagia e l’apoptosi delle cellule tumorali e ha dimostrato un impatto significativo su varie linee cellulari tumorali. L’ivermectina induce l’apoptosi nelle cellule tumorali in vivo e riduce significativamente il volume tumorale rispetto al controllo.
L’ivermectina induce l’apoptosi nelle cellule tumorali attraverso la mediazione mitocondriale. Può colpire e regolare le isoforme della piruvato chinasi muscolare nell’ultimo passaggio della glicolisi, inibire la glicolisi attraverso l’autofagia e avere un effetto pro-ossidante selettivo sulle cellule tumorali. Può anche colpire le CSC e le metastasi, nonché i macrofagi. In vitro, l’ivermectina è più efficace nell’inibire le CSC nelle cellule di cancro mammario rispetto alla chemioterapia (paclitaxel). In vivo, l’ivermectina da sola è più efficace della chemioterapia standard (gemcitabina) da sola nel ridurre il peso e il volume tumorale nel cancro pancreatico.
Sicurezza e Dosi Terapeutiche
L’ivermectina è un farmaco molto sicuro. In volontari sani, la singola dose è stata aumentata a 2 mg/Kg senza trovare reazioni avverse gravi. In un altro studio, pazienti oncologici che hanno assunto ivermectina a cinque volte la dose standard (fino a 1 mg/kg) quotidianamente per fino a 180 giorni consecutivi non hanno avuto effetti avversi gravi. In casi trattati con successo con una combinazione totale o parziale di ivermectina, dicloroacetato e omeprazolo (più tamoxifene), l’ivermectina ha inibito la crescita tumorale attraverso la disfunzione mitocondriale e ha portato all’apoptosi.

I Benzimidazoli: Mebendazolo e Fenbendazolo
Farmaci Antielmintici con Effetti Antitumorali
Un’altra famiglia di farmaci con promettenti capacità antitumorali è quella dei benzimidazoli, che include il mebendazolo e il fenbendazolo. Questi farmaci hanno effetti antitumorali attraverso la polimerizzazione microtubulare, l’induzione dell’apoptosi, l’arresto del ciclo cellulare (fase G2/M), l’anti-angiogenesi, il blocco delle vie del glucosio e della glutammina. L’apoptosi è indotta da lesioni mitocondriali ed è mediata dall’espressione p53.
Il mebendazolo è risultato più potente contro le linee cellulari di cancro gastrico rispetto ad altri farmaci chemioterapici ben noti (5-fluorouracile, oxaliplatino, gemcitabina, irinotecan, paclitaxel, cisplatino, etoposide e doxorubicina) in vitro. Il mebendazolo porta a una sopravvivenza significativamente prolungata rispetto alla chemioterapia standard (temozolomide) per il glioblastoma multiforme in vivo.
Casi Clinici di Remissione
Il mebendazolo è stabilito come farmaco sicuro. In pazienti pediatrici con idatidosi, il trattamento a lungo termine con mebendazolo (50 mg/kg al giorno per 9-18 mesi) è stato dimostrato senza effetti collaterali significativi. Pazienti che assumevano 1500 mg/giorno di mebendazolo per i gliomi sono stati notati senza tossicità dal farmaco. Pazienti con cancro gastrointestinale refrattario al trattamento che partecipavano a uno studio di fase 2 utilizzando dosi individualizzate di mebendazolo, fino a 4 g/giorno, non hanno sperimentato effetti avversi gravi.
È stata riportata una caso di remissione quasi completa in un paziente con cancro colon metastatico dopo aver assunto mebendazolo, dopo il fallimento degli agenti chemioterapici inclusi capecitabina, oxaliplatino, bevacizumab, capecitabina e irinotecan. In un altro caso clinico, un uomo di 48 anni con carcinoma surrenocorticale ha avuto progressione della malattia con tutte le terapie sistemiche. Gli è stato prescritto mebendazolo 100 mg due volte al giorno, come singolo agente. Le sue metastasi inizialmente sono regredite e successivamente sono rimaste stabili. Mentre riceveva mebendazolo come unico trattamento per 19 mesi, la sua malattia è rimasta stabile. Non ha sperimentato effetti avversi clinicamente significativi e la sua qualità di vita è stata soddisfacente.
Risultati simili sono stati osservati con il fenbendazolo: tre pazienti con cancro di stadio IV (neoplasie genitourinarie) sono stati trattati con una dose di 1000 mg tre volte a settimana per diversi mesi e hanno sperimentato la remissione completa della malattia. Due dei tre pazienti avevano sperimentato la progressione della malattia metastatica nonostante diverse linee di trattamento prima di iniziare il fenbendazolo.
Il DON (6-Diazolo-5-Oxo-L-Norleucina): Un Antagonista del Glutammina
Potenza e Meccanismo d’Azione
Il DON è un antagonista specifico del glutammina, più potente dei benzimidazoli. Il DON ha una potente attività antitumorale in vitro e in vivo. Mira specificamente al glutammina e influenza anche l’assorbimento del glucosio. Può indurre specificamente l’apoptosi nelle CSC e colpire le metastasi. Dosaggi giornalieri bassi di DON sono senza tossicità.
Il glutammina è un carburante fondamentale per le cellule tumorali, specialmente per le CSC e le metastasi. I tumori avanzati mostrano una forte dipendenza dal glutammina, e l’inibizione di questa via metabolica può essere particolarmente efficace nel fermare la crescita tumorale. Il DON, come antagonista del glutammina, può interrompere questa dipendenza metabolica e indurre la morte delle cellule tumorali.

Interventi Dietetici: Digiuno e Dieta Chetogenica
Il Digiuno come Terapia Metabolica
Il digiuno induce un miglioramento dell’attività mitocondriale attraverso l’aumento dell’OxPhos, l’autofagia e l’inibizione della glicolisi e della glutaminolisi. Il digiuno può allenare la rigenerazione delle cellule staminali “normali”, ma può anche alterare le CSC attraverso l’autofagia. L’inibizione o la privazione del glucosio porta alla morte delle CSC. In vivo, il digiuno ha effetti antitumorali e potenzia l’attività dei farmaci con cui è combinato.
Alla luce dei meccanismi molecolari della crescita tumorale, i ricercatori hanno affermato che “… prescrivere il digiuno come farmaco antitumorale potrebbe non essere lontano se ampi studi clinici randomizzati ne consolidassero la sicurezza ed efficacia”.
La Dieta Chetogenica e la Terapia Metabolica con Chetoni
La chetosi terapeutica somministrata come dieta chetogenica o terapia metabolica conchetoni (KMT) inibisce la crescita delle cellule staminali tumorali, ripristina l’apoptosi e aumenta la respirazione cellulare. La dieta chetogenica esibisce effetti antitumorali sia in vitro che in vivo, principalmente attraverso l’inibizione della via glicolitica in vari tipi di cancro, e la sua efficacia è stata dimostrata nell’uomo con glioblastoma multiforme.
I massimi benefici terapeutici del DON e del mebendazolo si sono verificati solo quando i farmaci sono stati somministrati insieme a una dieta chetogenica. Inoltre, l’associazione tra dieta chetogenica e DON riduce la tossicità del DON. Una dieta chetogenica o il digiuno potrebbero inibire i carburanti necessari per le cellule tumorali (glucosio e glutammina) mentre aumentano l’attività dell’OxPhos.
Un caso clinico ha riportato la sopravvivenza di un paziente con glioblastoma di grado IV vivo per più di 6 anni dalla diagnosi, trattato con riduzione chirurgica e dieta chetogenica sotto chetosi terapeutica senza chemioradioterapia. Foster ha analizzato 200 casi di regressione spontanea del cancro, mostrando che l’87% aveva apportato un cambiamento importante nella dieta, principalmente vegetariano, il 55% aveva utilizzato qualche forma di detossificazione e il 65% aveva utilizzato integratori nutrizionali.
L’obiettivo con la dieta chetogenica e la terapia metabolica con chetoni è di limitare simultaneamente le vie della glicolisi e della glutaminolisi mentre si porta il corpo in uno stato di chetosi per colpire le cellule tumorali, sia le CSC che le cellule non staminali tumorali. Oltre alla chetosi metabolica, studi sulla supplementazione con chetoni hanno dimostrato che i chetoni migliorano indipendentemente la funzione mitocondriale e sopprimono la crescita tumorale colpendo le metastasi e la maggior parte i marcatori di cancro.
Considerazioni Terapeutiche Aggiuntive
La Terapia Press-Pulse
La terapia Press-Pulse offre una terapia a due assi. L’asse “Press” consiste nel seguire una dieta chetogenica associata alla gestione dello stress. L’asse “Pulse” combina l’inibizione della glicolisi con il 2-deossiglucosio (2-DG), l’inibizione della glutaminolisi con il DON e l’ossigeno iperbarico (HBOT) per invertire l’ipossia e indurre stress ossidativo specifico del cancro. La teoria metabolica alla base della terapia Press-Pulse è la più vicina alla teoria MSCC proposta.
L’Attività Fisica
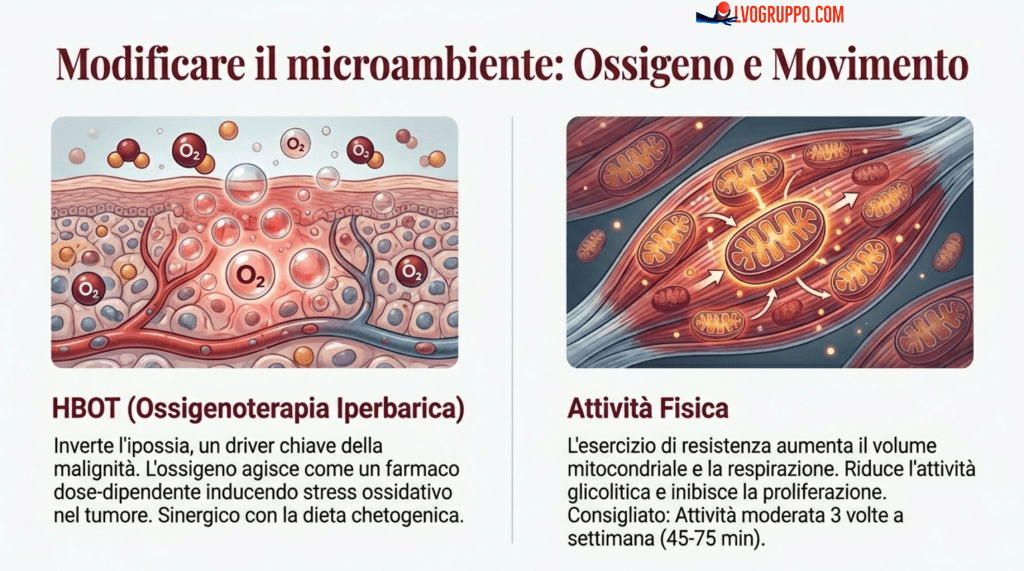
Il diabete e l’obesità sono fattori di rischio per molti tipi di cancro, probabilmente attraverso l’alterazione dell’OxPhos, promuovendo le CSC e l’aumento dell’effetto Warburg. Di conseguenza, l’attività fisica può conferire un ruolo protettivo. Gli esercizi di resistenza aumentano il volume dei mitocondri, migliorando la respirazione mitocondriale e i suoi effetti protettivi sulle cellule sane. L’esercizio diminuisce anche l’attività glicolitica. La produzione di ATP e la respirazione mitocondriale sono più elevate durante l’allenamento regolare di intensità bassa o moderata.
L’Ossigeno Iperbarico
L’ipossia è una caratteristica critica dei tumori maligni e coinvolge la sopravvivenza cellulare potenziata, l’angiogenesi, il metabolismo della glicolisi e della glutaminolisi e le metastasi. Esistono evidenze che implicano l’ossigeno come un farmaco, dipendente dalla dose, e che l’HBOT ha effetti inibitori sui tumori, specialmente quando combinato con la KMT. L’HBOT esibisce una potente attività antitumorale sia in vitro che in vivo, utilizzato da solo o in combinazione. L’HBOT può colpire le CSC e le metastasi e aumentare l’OxPhos. La KMT è sinergica con l’HBOT e produce un potente effetto sinergico sulla soppressione della crescita tumorale e della diffusione metastatica in modelli preclinici di cancro metastatico e casi clinici umani.
Il Protocollo Proposto: Raccomandazioni Dettagliate
1. Vitamina C Endovenosa
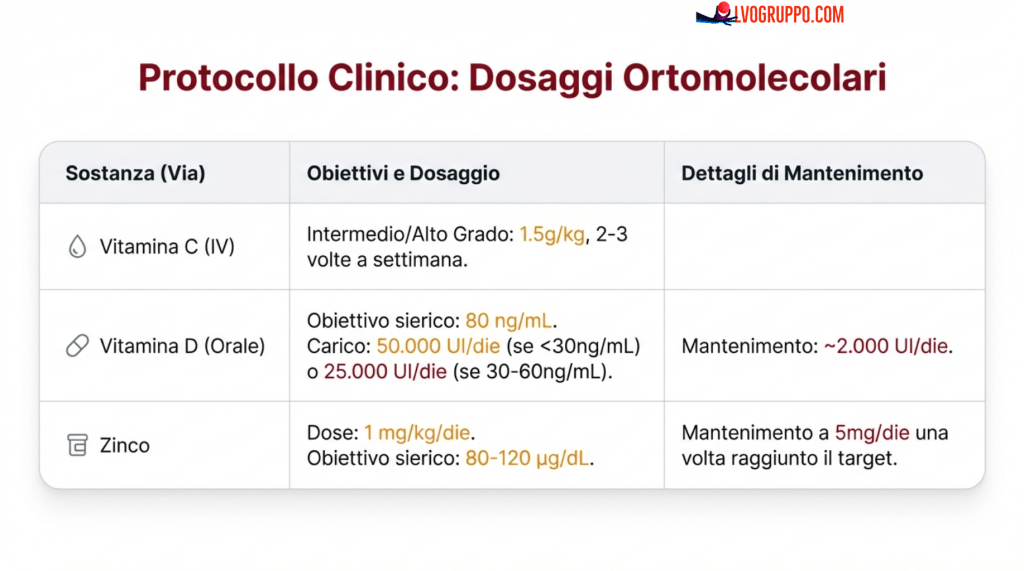
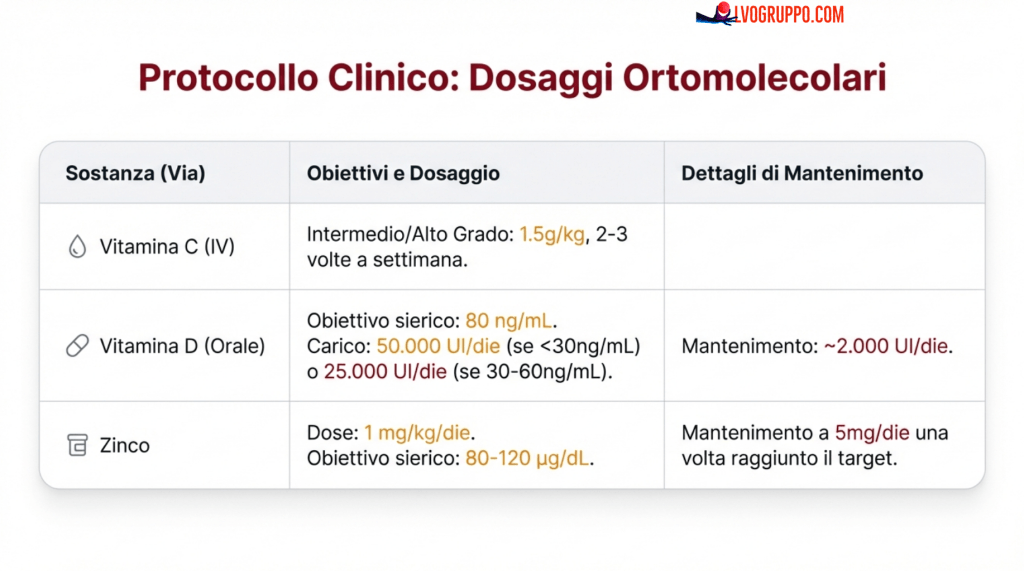
Per i tumori di grado intermedio e alto, si raccomanda una dose di 1,5 g/kg/giorno, 2-3 volte a settimana. Questa dose è stabilita come non tossica per i pazienti oncologici. La somministrazione endovenosa è essenziale per raggiungere concentrazioni plasmatiche terapeutiche che non sono ottenibili con la supplementazione orale.
2. Vitamina D Orale
Per tutti i gradi di cancro, si raccomanda una dose di 50.000 UI/giorno per pazienti con livelli ematici ≤ 30 ng/mL; 25.000 UI/giorno per livelli 30-60 ng/mL; e 5000 UI/giorno per livelli 60-80 ng/mL. È necessario raggiungere un livello ematico di 80 ng/mL di vitamina D (25-idrossivitamina D). Questo livello è non tossico. Una volta raggiunto, deve essere mantenuto con una dose giornaliera ridotta di circa 2000 UI/giorno. La concentrazione di vitamina D nel sangue deve essere misurata ogni due settimane per dosi elevate e mensilmente per dosi più basse.
3. Zinco
Per tutti i gradi di cancro, si raccomanda una dose di 1 mg/kg/giorno, stabilita come non tossica per i pazienti oncologici. L’intervallo di riferimento per la concentrazione sierica di zinco è di 80-120 μg/dL. Una volta raggiunto questo livello, deve essere mantenuto con una dose giornaliera ridotta di 5 mg/giorno. La concentrazione di zinco nel sangue deve essere misurata mensilmente.
4. Ivermectina
Per i tumori di basso grado: dose di 0,5 mg/kg, 3 volte a settimana. Per i tumori di grado intermedio: dose di 1 mg/kg, 3 volte a settimana. Per i tumori di alto grado: dose da 1 mg/kg/giorno a 2 mg/kg/giorno. Tutte queste dosi sono stabilite come tollerabili per l’uomo.
5. Benzimidazoli e DON
Per i tumori di basso grado: mebendazolo 200 mg/giorno. Per i tumori di grado intermedio: mebendazolo 400 mg/giorno. Per i tumori di alto grado: dose di mebendazolo 1500 mg/giorno o fenbendazolo 1000 mg 3 volte a settimana. I benzimidazoli possono essere sostituiti o combinati con il DON, somministrato senza tossicità per via endovenosa o intramuscolare: 0,2-0,6 mg/kg una volta al giorno; o per via orale: 0,2-1,1 mg/kg una volta al giorno. I benzimidazoli sono molto più facili da ottenere rispetto al DON. Tuttavia, per i tumori metastatici, che dipendono fortemente dal glutammina, dovrebbe essere considerata una combinazione di DON e benzimidazoli.
6. Interventi Dietetici
Per tutti i gradi di cancro, si raccomanda una dieta chetogenica (dieta povera di carboidrati e ricca di grassi, 900-1500 kcal/giorno). La terapia metabolica con chetoni consiste in circa 60-80% di grassi, 15-25% di proteine e 5-10% di carboidrati fibrosi. È necessaria un’idratazione adeguata e pasti chetogenici monoprodotto interi per raggiungere un punteggio dell’indice glucosio-chetoni (GKI) di 2,0 o inferiore. Il GKI deve essere misurato 2-3 ore postprandiale, due volte al giorno se possibile.

Per i tumori di grado intermedio e alto, la dieta chetogenica dovrebbe essere accoppiata con un digiuno idrico per 3-7 giorni consecutivi nei tumori avanzati. Il digiuno idrico dovrebbe essere ripetuto diverse volte (circa ogni 3-4 settimane) durante il trattamento, ma il digiuno deve essere intrapreso con cautela negli individui che usano alcuni farmaci e in quelli con BMI < 20, per prevenire la perdita di massa magra. Per i pazienti che non possono digiunire, può essere utilizzata la dieta che mima il digiuno (300-1100 kcal/giorno di brodi, zuppe, succhi, barrette di noci e tisane).
7. Terapeutiche Aggiuntive
Per tutti i gradi di cancro, si raccomanda un’attività fisica moderata, 3 volte a settimana. Frequenza cardiaca e respiratoria aumentate per un periodo di 45-75 minuti con attività come ciclismo, corsa, nuoto, ecc.
Per i tumori di grado intermedio e alto o per individui che non possono svolgere attività fisica: terapia con ossigeno iperbarico, 1,5-2,5 ATA per 45-60 minuti 2-3 volte a settimana.

Considerazioni sulla Durata e la Sicurezza del Trattamento
Il protocollo dovrebbe essere seguito per una durata media di 12 settimane, indipendentemente dal tipo di cancro. L’analisi delle interazioni tra ciascuna delle molecole non ha rivelato controindicazioni alla combinazione di queste sostanze. Il dosaggio e la durata del trattamento possono essere aggiustati dal medico secondo il singolo paziente, la sua capacità di ottenere le varie molecole e i risultati del trattamento. L’adattamento del protocollo per includere molecole aggiuntive per ripristinare la salute potrebbe essere considerato dal medico. Queste possono includere: vitamina K2, vitamina E, coenzima Q10, blu di metilene, niacina, riboflavina, artemisinina + acido 5-aminolevulinico (per causare accumulo di porfirine), melatonina, NADH e magnesio, per esempio. Tuttavia, i dosaggi antiossidanti dovrebbero essere evitati.

Conclusioni: Verso un Nuovo Paradigma Oncologico
La connessione mitocondrio-cellula staminale potrebbe essere un elemento chiave nell’approccio terapeutico al cancro. Alla luce delle conoscenze attuali, abbiamo selezionato e proponiamo l’uso di specifiche molecole ortomolecolari, farmaci e altre terapie per il loro potenziale di rivitalizzare l’attività dell’OxPhos cellulare e colpire le CSC, la glicolisi e la glutaminolisi. Questi sono anche mirati ad affrontare le metastasi create dalla fusione ibrida tra cellule staminali tumorali e macrofagi. Numerosi esperimenti su cellule, animali e umani supportano il ruolo del targeting della MSCC sia nella prevenzione che nel trattamento del cancro.
La teoria MSCC e il protocollo ortomolecolare ibrido rappresentano una sfida significativa al paradigma oncologico dominante. Non si tratta di rifiutare completamente le terapie convenzionali, ma di integrare nuove strategie che affrontino le cause profonde della malattia: la disfunzione mitocondriale e la persistenza delle cellule staminali tumorali. I risultati clinici, sebbene preliminari, sono incoraggianti e giustificano ulteriori studi clinici randomizzati per valutare l’efficacia e la sicurezza di questo approccio rispetto alle terapie standard.
Il futuro dell’oncologia potrebbe risiedere non tanto nella scoperta di nuovi farmaci chemioterapici o靶向, ma nella comprensione e nel ripristino del metabolismo cellulare normale. Se il cancro è davvero una malattia metabolica che origina nelle cellule staminali, allora la risposta potrebbe non essere l’ennesimo farmaco tossico, ma un approccio olistico che ripristina l’equilibrio metabolico dell’organismo. Il protocollo ortomolecolare ibrido qui presentato rappresenta un passo in questa direzione, offrendo una strategia terapeutica basata sull’evidenza scientifica che affronta il cancro alle sue radici metaboliche.
Riferimenti Bibliografici
Abraham, A., Kattoor, A. J., Saldeen T., e Mehta, J. L. (2019). “Vitamin E and its anticancer effects.” Crit Rev Food Sci Nutr. 59(17): 2831-2838. https://doi.org/10.1080/10408398.2018.1474169
Adams, J. M., e Strasser, A. (2008). “Is tumor growth sustained by rare cancer stem cells or dominant clones?” Cancer Res. 68(11): 4018-4021. https://doi.org/10.1158/0008-5472.can-07-6334
Adapa, S. R., Hunter, G. A., Amin, N. E., Marinescu, C., Borsky, A., Sagatys, E. M., Sebti, S. M., Reuther, G. W., Ferreira, G. C., e Jiang, R. H. (2024). “Porphyrin overdrive rewires cancer cell metabolism.” Life Sci Alliance. 7(7). https://doi.org/10.26508/lsa.202302547
Aguilera, O., Muñoz-Sagastibelza, M., Torrejón, B., Borrero-Palacios, A., Del Puerto-Nevado, L., Martínez-Useros, J., Rodríguez-Remirez, M., Zazo, S., García, E., Fraga, M., Rojo, F., e García-Foncillas, J. (2016). “Vitamin C uncouples the Warburg metabolic switch in KRAS mutant colon cancer.” Oncotarget. 7(30): 47954-47965. https://doi.org/10.18632/oncotarget.10087
Aljohar, A. Y., Muteeb, G., Zia, Q., Siddiqui, S., Aatif, M., Farhan, M., Khan, M. F., Alsultan, A., Jamal, A., Alshoaibi, A., Ahmad, E., Alam, M. W., Arshad, M., e Ahamed, M. I. (2022). “Anticancer effect of zinc oxide nanoparticles prepared by varying entry time of ion carriers against A431 skin cancer cells in vitro.” Front Chem. 10: 1069450. https://doi.org/10.3389/fchem.2022.1069450
ANSM. (2023). “Thesaurus des interactions médicamenteuses”. https://ansm.sante.fr/uploads/2023/09/15/20230915-thesaurus-interactions-medicamenteuses-septembre-2023.pdf
Arora, N., Pulimamidi, S., Yadav, H., Jain, S., Glover, J., Dombrowski, K., Hernandez, B., Sarma, A. K., e Aneja, R. (2023). “Intermittent fasting with ketogenic diet: A combination approach for management of chronic diseases.” Clin Nutr ESPEN. 54: 166-174. https://doi.org/10.1016/j.clnesp.2023.01.024
Ashique, S., Kumar, S., Hussain, A., Mishra, N., Garg, A., Gowda, B. H. J., Farid, A., Gupta, G., Dua, K., e Taghizadeh-Hesary, F. (2023). “A narrative review on the role of magnesium in immune regulation, inflammation, infectious diseases, and cancer.” J Health Popul Nutr. 42(1): 74. https://doi.org/10.1186/s41043-023-00423-0
Averbeck, D., e Rodriguez-Lafrasse, C. (2021). “Role of Mitochondria in Radiation Responses: Epigenetic, Metabolic, and Signaling Impacts.” Int J Mol Sci. 22(20). https://doi.org/10.3390/ijms222011047
Bai, R. Y., Staedtke, V., Aprhys, C. M., Gallia, G. L., e Riggins, G. J. (2011). Antiparasitic mebendazole shows survival benefit in 2 preclinical models of glioblastoma multiforme. Neuro Oncol. 13(9): 974-982. https://doi.org/10.1093/neuonc/nor077
Baldwin, K. M., Klinkerfuss, G. H., Terjung, R. L., Molé, P. A., e Holloszy, J. O. (1972). “Respiratory capacity of white, red, and intermediate muscle: adaptive response to exercise.” Am J Physiol. 222(2): 373-378. https://doi.org/10.1152/ajplegacy.1972.222.2.373
Bianchi, G., Martella, R., Ravera, S., Marini, C., Capitanio, S., Orengo, A., Emionite, L., Lavaello, C., Amaro, A., Petretto, A., Pfeffer, U., Sambuceti, G., Pistoia, V., Raffaghello, L., e Longo, V. D. (2015). “Fasting induces anti-Warburg effect that increases respiration but reduces ATP-synthesis to promote apoptosis in colon cancer models.” Oncotarget. 6(14): 11806-11819. https://doi.org/10.18632/oncotarget.3688
Bonuccelli, G., De Francesco, E. M., de Boer, R., Tanowitz, H. B., e Lisanti, M. P. (2017). “NADH autofluorescence, a new metabolic biomarker for cancer stem cells: Identification of Vitamin C and CAPE as natural products targeting ‘stemness’.” Oncotarget. 8(13): 20667-20678. https://doi.org/10.18632/oncotarget.15400
Bull, F. C., Al-Ansari, S. S., Biddle, S., Borodulin, K., Buman, M. P., Cardon, G., Carty, C., Chaput, J. P., Chastin, S., Chou, R., Dempsey, P. C., DiPietro, L., Ekelund, U., Firth, J., Friedenreich, C. M., Garcia, L., Gichu, M., Jago, R., Katzmarzyk, P. T., Lambert, E., Leitzmann, M., Milton, K., Ortega, F. B., Ranasinghe, C., Stamatakis, E., Tiedemann, A., Troiano, R. P., van der Ploeg, H. P., Wari, V., e Willumsen, J. F. (2020). “World Health Organization 2020 guidelines on physical activity and sedentary behaviour.” Br J Sports Med. 54(24): 1451-1462. https://doi.org/10.1136/bjsports-2020-102955
Butt, G., Farooqi, A. A., Adylova, A., Attar, R., Yilmaz, S., Konysbayevna, K. K., Sabitaliyevich, U. Y., Gasparri, M. L., e Xu, B. (2020). “Vitamin C as an Anti-cancer Agent: Regulation of Signaling Pathways.” Curr Top Med Chem. 20(21): 1868-1875. https://doi.org/10.2174/1568026620666200710102841
Cameron, E., e Pauling, L. (1978). “Supplemental ascorbate in the supportive treatment of cancer: reevaluation of prolongation of survival times in terminal human cancer.” Proc Natl Acad Sci U S A. 75(9): 4538-4542. https://doi.org/10.1073/pnas.75.9.4538
Cannon, T. L., Ford, J., Hester, D., e Trump, D. L. (2016). The Incidental Use of High-Dose Vitamin D3 in Pancreatic Cancer. In Case Rep Pancreat Cancer. 2(1): 32-35. https://doi.org/10.1089/crpc.2016.0003
Capp, J. P. (2019). “Cancer Stem Cells: From Historical Roots to a New Perspective.” JOncol. 2019: 5189232. https://doi.org/10.1155/2019/5189232
Cardone, R. A., Casavola, V., e Reshkin, S. J. (2005). “The role of disturbed pH dynamics and the Na⁺/H⁺ exchanger in metastasis.” Nat Rev Cancer. 5(10): 786-795. https://doi.org/10.1038/nrc1713
Chai, J. Y., Jung, B. K., e Hong, S. J. (2021). “Albendazole and Mebendazole as Anti-Parasitic and Anti-Cancer Agents: an Update.” Korean J Parasitol. 59(3): 189-225. https://doi.org/10.3347/kjp.2021.59.3.189
Chakraborti, C. K. (2011). “Vitamin D as a promising anticancer agent.” Indian J Pharmacol. 43(2): 113-120. https://doi.org/10.4103/0253-7613.77335
Chandler, P. D., Chen, W. Y., Ajala, O. N., Hazra, A., Cook, N., Bubes, V., Lee, I. M., Giovannucci, E. L., Willett, W., Buring, J. E., e Manson, J. E. (2020). “Effect of Vitamin D3 Supplements on Development of Advanced Cancer: A Secondary Analysis of the VITAL Randomized Clinical Trial.” JAMA Netw Open. 3(11): e2025850. https://doi.org/10.1001/jamanetworkopen.2020.25850
Chen, M., Ding, Y., Ke, Y., Zeng, Y., Liu, N., Zhong, Y., Hua, X., Li, Z., Xiong, Y., Wu, C., e Yu, H. (2020). “Anti-tumour activity of zinc ionophore pyrithione in human ovarian cancer cells through inhibition of proliferation and migration and promotion of lysosome-mitochondrial apoptosis.” Artif Cells Nanomed Biotechnol. 48(1): 824-833. https://doi.org/10.1080/21691401.2020.1770266
Chen, Q., Espey, M. G., Krishna, M. C., Mitchell, J. B., Corpe, C. P., Buettner, G. R., Shacter, E., e Levine, M. (2005). “Pharmacologic ascorbic acid concentrations selectively kill cancer cells: action as a pro-drug to deliver hydrogen peroxide to tissues.” Proc Natl Acad Sci U S A. 102(38): 13604-13609. https://doi.org/10.1073/pnas.0506390102
Chen, Q., Espey, M. G., Sun, A. Y., Pooput, C., Kirk, K. L., Krishna, M. C., Khosh, D. B., Drisko, J., e Levine, M. (2008). “Pharmacologic doses of ascorbate act as a prooxidant and decrease growth of aggressive tumor xenografts in mice.” Proc Natl Acad Sci U S A. 105(32): 11105-11109. https://doi.org/10.1073/pnas.0804226105
Chiang, R., Syed, A., Wright, J., Montgomery, B., e Srinivas, S. (2021). Fenbendazole Enhancing Anti-Tumor Effect: A Case Series. Clin Oncol Case Rep. 4(2).
Chu, J., Li, Y., He, M., Zhang, H., Yang, L., Yang, M., Liu, J., Cui, C., Hong, L., Hu, X., Zhou, L., Li, T., Li, C., Fan, H., Jiang, G., e Lang, T. (2023). “Zinc finger and SCAN domain containing 1, ZSCAN1, is a novel stemness-related tumor suppressor and transcriptional repressor in breast cancer targeting TAZ.” Front Oncol. 13: 1041688. https://doi.org/10.3389/fonc.2023.1041688
Costello, L. C., e Franklin, R. B. (2017). “Decreased zinc in the development and progression of malignancy: an important common relationship and potential for prevention and treatment of carcinomas.” Expert Opin Ther Targets. 21(1): 51-66. https://doi.org/10.1080/14728222.2017.1265506
CRAT. 2024. https://www.lecrat.fr/
da Veiga Moreira, J., Nleme, N., Schwartz, L., Leclerc-Desaulniers, K., Carmona, E., Mes-Masson, A. M., e Jolicoeur, M. (2024). “Methylene Blue Metabolic Therapy Restrains In Vivo Ovarian Tumor Growth.” Cancers (Basel). 16(2). https://doi.org/10.3390/cancers16020355
Daruwalla, J., e Christophi, C. (2006). “Hyperbaric oxygen therapy for malignancy: a review.” World J Surg. 30(12): 2112-2131. https://doi.org/10.1007/s00268-006-0190-6
de Castro, C. G. Jr., Gregorianin, L. J., e Burger, J. A. (2020). “Continuous high-dose ivermectin appears to be safe in patients with acute myelogenous leukemia and could inform clinical repurposing for COVID-19 infection.” Leuk Lymphoma. 61(10): 2536-2537. https://doi.org/10.1080/10428194.2020.1786559
De Francesco, E. M., Sotgia, F., e Lisanti, M. P. (2018). “Cancer stem cells (CSCs): metabolic strategies for their identification and eradication.” Biochem J. 475(9): 1611-1634. https://doi.org/10.1042/bcj20170164
Deligiorgi, M. V., Liapi, C., e Trafalis, D. T. (2020). “How Far Are We from Prescribing Fasting as Anticancer Medicine?” Int J Mol Sci. 21(23). https://doi.org/10.3390/ijms21239175
Del Paggio, J. C., Berry, J. S., Hopman, W. M., Eisenhauer, E. A., Prasad, V., Gyawali, B., e Booth, C. M. (2021). Evolution of the Randomized Clinical Trial in the Era of Precision Oncology. JAMA Oncology. 7(5): 728-734. https://doi.org/10.1001/jamaoncol.2021.0379
Deruelle, F., e Baron, B. (2008). “Vitamin C: is supplementation necessary for optimal health?” J Altern Complement Med. 14(10): 1291-1298. https://doi.org/10.1089/acm.2008.0165
Dobrosotskaya, I. Y., Hammer, G. D., Schteingart, D. E., Maturen, K. E., e Worden, F. P. (2011). “Mebendazole monotherapy and long-term disease control in metastatic adrenocortical carcinoma.” Endocr Pract. 17(3): e59-62. https://doi.org/10.4158/ep10390.cr
Dominguez-Gomez, G., Chavez-Blanco, A., Medina-Franco, J. L., Saldivar-Gonzalez, F., Flores-Torrontegui, Y., Juarez, M., Díaz-Chávez, J., Gonzalez-Fierro, A., e Dueñas-González, A. (2018). “Ivermectin as an inhibitor of cancer stem-like cells.” Mol Med Rep. 17(2): 3397-3403. https://doi.org/10.3892/mmr.2017.8231
Dressler, R., Laut, J., Lynn, R. I., e Ginsberg, N. (1995). “Long-term high dose intravenous calcitriol therapy in end-stage renal disease patients with severe secondary hyperparathyroidism.” Clin Nephrol. 43(5): 324-331
Ekwaru, J. P., Zwicker, J. D., Holick, M. F., Giovannucci, E., e Veugelers, P. J. (2014). “The importance of body weight for the dose response relationship of oral vitamin D supplementation and serum 25-hydroxyvitamin D in healthy volunteers.” PLoS One. 9(11): e111265. https://doi.org/10.1371/journal.pone.0111265
Elliott, R. L., Jiang, X. P., e Head, J. F. (2012). Mitochondria organelle transplantation: introduction of normal epithelial mitochondria into human cancer cells inhibits proliferation and increases drug sensitivity. Breast Cancer Res Treat. 136(2): 347-354. https://doi.org/10.1007/s10549-012-2283-2
Elsakka, A. M. A., Bary, M. A., Abdelzaher, E., Elnaggar, M., Kalamian, M., Mukherjee, P., e Seyfried, T. N. (2018). “Management of Glioblastoma Multiforme in a Patient Treated With Ketogenic Metabolic Therapy and Modified Standard of Care: A 24-Month Follow-Up.” Front Nutr. 5: 20. https://doi.org/10.3389/fnut.2018.00020
Fakih, M. G., Trump, D. L., Muindi, J. R., Black, J. D., Bernardi, R. J., Creaven, P. J., Schwartz, J., Brattain, M. G., Hutson, A., French, R., e Johnson, C. S. (2007). “A phase I pharmacokinetic and pharmacodynamic study of intravenous calcitriol in combination with oral gefitinib in patients with advanced solid tumors.” Clin Cancer Res. 13(4): 1216-1223. https://doi.org/10.1158/1078-0432.ccr-06-1165
Fan, D., Liu, X., Shen, Z., Wu, P., Zhong, L., e Lin, F. (2023). “Cell signaling pathways based on vitamin C and their application in cancer therapy.” Biomed Pharmacother. 162: 114695. https://doi.org/10.1016/j.biopha.2023.114695
Feng, Y., Wang, J., Cai, B., Bai, X., e Zhu, Y. (2022). Ivermectin accelerates autophagic death of glioma cells by inhibiting glycolysis through blocking GLUT4 mediated JAK/STAT signaling pathway activation. Environ Toxicol. 37(4): 754-764. https://doi.org/10.1002/tox.23440
Flockhart, M., Nilsson, L. C., Tais, S., Ekblom, B., Après, W., e Larsen, F. J. (2021). “Excessive exercise training causes mitochondrial functional impairment and decreases glucose tolerance in healthy volunteers.” Cell Metab. 33(5): 957-970.e956. https://doi.org/10.1016/j.cmet.2021.02.017
Florio, R., Veschí, S., di Giacomo, V., Pagotto, S., Carradori, S., Verginelli, F., De Lellis, L., e C. (2019). The Benzimidazole-Based Anthelmintic Parbendazole: A Repurposed Drug Candidate That Synergizes with Gemcitabine in Pancreatic Cancer. Cancers (Basel). 11(12). https://doi.org/10.3390/cancers11122042
Foster, H. (1988). “Lifestyle changes and the ‘Spontaneous’ regression of cancer: An initial computer analysis.” International Journal of Biosocial Research. 10(1): 17-33
Gelbard, A. (2022). “Zinc in Cancer Therapy Revisited.” Isr Med Assoc J. 24(4): 258-262
Ghanaati, S., Choukroun, J., Volz, U., Hueber, R., Mourao, C. F., Sader, R., Kawase-Koga, Y., Mazhari, R., Amrein, K., Meybohm, P., e Al-Maawi, S. (2020). “One hundred years after Vitamin D discovery: Is there clinical evidence for supplementation doses?” International Journal of Growth Factors and Stem Cells in Dentistry. 3: 3. https://doi.org/10.4103/GFSC.GFSC_4_20
Gibb, A. A., Epstein, P. N., Uchida, S., Zheng, Y., McNally, L. A., Obal, D., Katragadda, K., Trainor, P., Conklin, D. J., Brittian, K. R., Tseng, M. T., Wang, J., Jones, S. P., Bhatnagar, A., e Hill, B. G. (2017). “Exercise-Induced Changes in Glucose Metabolism Promote Physiological Cardiac Growth.” Circulation. 136(22): 2144-2157. https://doi.org/10.1161/circulationaha.117.028274
Gillies, R. J., Raghunand, N., Karczmar, G. S., e Bhujwalla, Z. M. (2002). “MRI of the tumor microenvironment.” J Magn Reson Imaging. 16(4): 430-450. https://doi.org/10.1002/jmri.10181
Gonzalez, M., Seyfried, T.N., Nicolson, G., Barclay, B., Matta, J., Vasquez, A., D’Agostino, D.P., Olalde, J., Duconge, J., Hunninghake, R., Berdiel, M., e Cintron, A. (2018). “Mitochondrial correction: a new therapeutic paradigm for cancer and degenerative diseases.” J Orthomol Med. 33: 1-20
Gonzalez, M. J., Miranda-Massari, J. R., e Olalde, J. (2023). Chapter 9 – Vitamin C and mitochondrial function in health and exercise. Molecular Nutrition and Mitochondria. S. M. Ostojic, Academic Press: 225-242
Gonzalez, M. J., Rosario-Pérez, G., Guzmán, A. M., Miranda-Massari, J. R., Duconge, J., Lavergne, J., Fernandez, N., Ortiz, N., Quintero, A., Mikirova, N., Riordan, N. H., e Ricart, C. M. (2010). “Mitochondria, Energy and Cancer: The Relationship with Ascorbic Acid.” J Orthomol Med. 25(1): 29-38
Gorini, S., De Angelis, A., Berrino, L., Malara, N., Rosano, G., e Ferraro, E. (2018). “Chemotherapeutic Drugs and Mitochondrial Dysfunction: Focus on Doxorubicin, Trastuzumab, and Sunitinib.” Oxid Med Cell Longev. 2018:7582730. https://doi.org/10.1155/2018/7582730
Grant, W. B. (2024). “Cancer Incidence Rates in the US in 2016–2020 with Respect to Solar UVB Doses, Diabetes and Obesity Prevalence, Lung Cancer Incidence Rates, and Alcohol Consumption: An Ecological Study.” Nutrients. 16(10). https://doi.org/10.3390/nu16101450
Greco, T., Glenn, T. C., Hovda, D. A., e Prins, M. L. (2016). “Ketogenic diet decreases oxidative stress and improves mitochondrial respiratory complex activity.” J Cereb Blood Flow Metab. 36(9): 1603-1613. https://doi.org/10.1177/0271678×15610584
Guzzo, C. A., Furtek, C. I., Porras, A. G., Chen, C., Tipping, R., Clineschmidt, C. M., Sciberras, D. G., Hsieh, J. Y., e Lasseter, K. C. (2002). “Safety, tolerability, and pharmacokinetics of escalating high doses of ivermectin in healthy adult subjects.” J Clin Pharmacol. 42(10): 1122-1133. https://doi.org/10.1177/009127002401382731
Göçmen, A., Toppare, M. F., e Kiper, N. (1993). “Treatment of hydatid disease in childhood with mebendazole.” Eur Respir J. 6(2): 253-257
Hadanny, A., Hachmo, Y., Rozali, D., Catalogna, M., Yaakobi, E., Sova, M., Gattegno, H., Abu Hamed, R., Lang, E., Polak, N., Friedman, M., Finci, S., Zemel, Y., Bechor, Y., Gal, N., e Efrati, S. (2022). “Effects of Hyperbaric Oxygen Therapy on Mitochondrial Respiration and Physical Performance in Middle-Aged Athletes: A Blinded, Randomized Controlled Trial.” Sports Med Open. 8(1): 22. https://doi.org/10.1186/s40798-021-00403-w
Hanahan, D., e Weinberg, R. A. (2000). “The hallmarks of cancer.” Cell. 100(1): 57-70. https://doi.org/10.1016/s0092-8674(00)81683-9
Hillers-Ziemer, L. E., McMahon, R. Q., Hietpas, M., Paderta, G., LeBeau, J., McCready, J., e Arendt, L. M. (2020). Obesity Promotes Cooperation of Cancer Stem-Like Cells and Macrophages to Enhance Mammary Tumor Angiogenesis. Cancers (Basel). 12(2). https://doi.org/10.3390/cancers12020502
Hohaus, S., Tisi, M. C., Bellesi, S., Maiolo, E., Alma, E., Tartaglia, G., Corrente, F., Cuccaro, A., D’Alo, F., Basile, U., Larocca, L. M., e De Stefano, V. (2018). “Vitamin D deficiency and supplementation in patients with aggressive B-cell lymphomas treated with immunochemotherapy.” Cancer Med. 7(1): 270-281. https://doi.org/10.1002/cam4.1166
Holick, M. F., Binkley, N. C., Bischoff-Ferrari, H. A., Gordon, C. M., Hanley, D. A., Heaney, R. P., Murad, M. H., e Weaver, C. M. (2011). “Evaluation, treatment, and prevention of vitamin D deficiency: an Endocrine Society clinical practice guideline.” J Clin Endocrinol Metab. 96(7): 1911-1930. https://doi.org/10.1210/jc.2011-0385
Holm, E., Hagmüller, E., Staedt, U., Schlickeiser, G., Günther, H., Leweling, H., Tokus, M., e Kollmar, H. (1995). “Substrate balances across colonic carcinomas in Humans.” Cancer research. 55: 1373-1378
Hoppe, C., Kutschan, S., Dörfler, J., Büntzel, J., e Huebner, J. (2021). “Zinc as a complementary treatment for cancer patients: a systematic review.” Clin Exp Med. 21(2): 297-313. https://doi.org/10.1007/s10238-020-00677-6
Huang, L., Zhao, L., Zhang, J., He, F., Wang, H., Liu, Q., Tang, L. (2021). Antiparasitic mebendazole (MBZ) effectively overcomes cisplatin resistance in human ovarian cancer cells by inhibiting multiple cancer-associated signaling pathways. Aging (Albany NY). 13(13): 17407-17427. https://doi.org/10.18632/aging.203232
Impax. (2016). “Impax Receives Approval of EMVERM™(mebendazole) Chewable Tablets, 100 mg.” https://s22.q4cdn.com/186279204/files/doc_news/archive/Impax-Receives-Approval-of-EMVERM-mebendazole-Chewable-Tablets-100-mg.pdf
Ishiguro, T., Ishiguro, R. H., Ishiguro, M., Toki, A., e Terunuma, H. (2022). “Synergistic Anti-tumor Effect of Dichloroacetate and Ivermectin.” Cureus. 14(2): e21884. https://doi.org/10.7759/cureus.21884
Jacobs, R. A., e Lundby, C. (2013). “Mitochondria express enhanced quality as well as quantity in association with aerobic fitness across recreationally active individuals up to elite athletes.” J Appl Physiol (1985). 114(3): 344-350. https://doi.org/10.1152/japplphysiol.01081.2012
Jagust, P., de Luxán-Delgado, B., Parejo-Alonso, B., e Sancho, P. (2019). “Metabolism-Based Therapeutic Strategies Targeting Cancer Stem Cells.” Front Pharmacol. 10: 203. https://doi.org/10.3389/fphar.2019.00203
Jariyal, H., Gupta, C., Andhale, S., Gadge, S., e Srivastava, A. (2021). “Comparative stemness and differentiation of luminal and basal breast cancer stem cell type under glutamine-deprivation.” J Cell Commun Signal. 15(2): 207-222. https://doi.org/10.1007/s12079-020-00603-1
Ji, C. C., Hu, Y. Y., Cheng, G., Liang, L., Gao, B., Ren, Y. P., Liu, J. T., Cao, X. L., Zheng, M. H., Li, S. Z., Wan, F., Han, H., e Fei, Z. (2020). “A ketogenic diet attenuates proliferation and stemness of glioma stem-like cells by altering metabolism resulting in increased ROS production.” Int J Oncol. 56(2): 606-617. https://doi.org/10.3892/ijo.2019.4942
Jiang, L., Sun, Y. J., Song, X. H., Sun, Y. Y., Yang, W. Y., Li, J., e Wu, Y. J. (2022). “Ivermectin inhibits tumor metastasis by regulating the Wnt/β-catenin/integrin β1/FAK signaling pathway.” Am J Cancer Res. 12(10): 4502-4519
Juarez, M., Schcolnik-Cabrera, A., e Dueñas-Gonzalez, A. (2018). “The multitargeted drug ivermectin: from an antiparasitic agent to a repositioned cancer drug.” Am J Cancer Res. 8(2): 317-331
Juarez, M., Schcolnik-Cabrera, A., Dominguez-Gomez, G., Chavez-Blanco, A., Diaz-Chavez, J., e Duenas-Gonzalez, A. (2020). Antitumor effects of ivermectin at clinically feasible concentrations support its clinical development as a repositioned cancer drug. Cancer Chemother Pharmacol. 85(6): 1153-1163. https://doi.org/10.1007/s00280-020-04041-z
Kanno, K., Akutsu, T., Ohdaira, H., Suzuki, Y., e Urashima, M. (2023). Effect of Vitamin D Supplements on Relapse or Death in a p53-Immunoreactive Subgroup With Digestive Tract Cancer: Post Hoc Analysis of the AMATERASU Randomized Clinical Trial. JAMA Netw Open. 6(8): e2328886. https://doi.org/10.1001/jamanetworkopen.2023.28886
Kc, S., Cárcamo, J. M., e Golde, D. W. (2005). “Vitamin C enters mitochondria via facilitative glucose transporter 1 (Glut1) and confers mitochondrial protection against oxidative injury.” Faseb j. 19(12): 1657-1667. https://doi.org/10.1096/fj.05-4107com
Kennel, K. A., Drake, M. T., e Hurley, D. L. (2010). “Vitamin D deficiency in adults: when to test and how to treat.” Mayo Clin Proc. 85(8): 752-757; quiz 757-758. https://doi.org/10.4065/mcp.2010.0138
Keum, N., Chen, Q. Y., Lee, D. H., Manson, J. E., e Giovannucci, E. (2022). “Vitamin D supplementation and total cancer incidence and mortality by daily vs. infrequent large-bolus dosing strategies: a meta-analysis of randomised controlled trials.” Br J Cancer. 127(5): 872-878. https://doi.org/10.1038/s41416-022-01850-2
Kolodziej, F., e O’Halloran, K. D. (2021). “Re-Evaluating the Oxidative Phenotype: Can Endurance Exercise Save the Western World?” Antioxidants (Basel). 10(4). https://doi.org/10.3390/antiox10040609
Ladanie, A., Schmitt, A. M., Speich, B., Naudet, F., Agarwal, A., Pereira, T. V., Hemkens, L. G. (2020). Clinical Trial Evidence Supporting US Food and Drug Administration Approval of Novel Cancer Therapies Between 2000 and 2016. JAMA Netw Open. 3(11): e2024406. https://doi.org/10.1001/jamanetworkopen.2020.24406
Lee, D. C., Ta, L., Mukherjee, P., Duraj, T., Domin, M., Greenwood, B., Karmacharya, S., Narain, N. R., Kiebish, M., Chinopoulos, C., e Seyfried, T. N. (2024). “Amino Acid and Glucose Fermentation Maintain ATP Content in Mouse and Human Malignant Glioma Cells.” bioRxiv. https://doi.org/10.1101/2024.04.18.589922
Lee, D. E., Kang, H. W., Kim, S. Y., Kim, M. J., Jeong, J. W., Hong, W. C., Park, J. S. (2022). Ivermectin and gemcitabine combination treatment induces apoptosis of pancreatic cancer cells via mitochondrial dysfunction. Front Pharmacol. 13: 934746. https://doi.org/10.3389/fphar.2022.934746
Lee, Y. (2023). “Role of Vitamin C in Targeting Cancer Stem Cells and Cellular Plasticity.” Cancers (Basel). 15(23). https://doi.org/10.3390/cancers15235657
Lemberg, K. M., Vornov, J. J., Rais, R., e Slusher, B. S. (2018). “We’re Not ‘DON’ Yet: Optimal Dosing and Prodrug Delivery of 6-Diazo-5-oxo-L-norleucine.” Mol Cancer Ther. 17(9): 1824-1832. https://doi.org/10.1158/1535-7163.mct-17-1148
Leone, R. D., Zhao, L., Englert, J. M., Sun, I. M., Oh, M. H., Sun, I. H., Arwood, M. L., Bettencourt, I. A., Patel, C. H., Wen, J., Tam, A., Blosser, R. L., Prchalova, E., Alt, J., Rais, R., Slusher, B. S., e Powell, J. D. (2019). “Glutamine blockade induces divergent metabolic programs to overcome tumor immune evasion.” Science. 366(6468): 1013-1021. https://doi.org/10.1126/science.aav2588
Lewis, M. T., Kasper, J. D., Bazil, J. N., Frisbee, J. C., e Wiseman, R. W. (2019). “Quantification of Mitochondrial Oxidative Phosphorylation in Metabolic Disease: Application to Type 2 Diabetes.” Int J Mol Sci. 20(21). https://doi.org/10.3390/ijms20215271
Li, J., Cao, D., Huang, Y., Chen, B., Chen, Z., Wang, R., Dong, Q., Wei, Q., e Liu, L. (2022). “Zinc Intakes and Health Outcomes: An Umbrella Review.” Front Nutr. 9: 798078. https://doi.org/10.3389/fnut.2022.798078
Li, K., Kaaks, R., Linseisen, J., e Rohrmann, S. (2012). “Vitamin/mineral supplementation and cancer, cardiovascular, and all-cause mortality in a German prospective cohort (EPIC-Heidelberg).” Eur J Nutr. 51(4): 407-413. https://doi.org/10.1007/s00394-011-0224-1
Li, N., Li, H., Wang, Y., Cao, L., e Zhan, X. (2020). Quantitative proteomics revealed energy metabolism pathway alterations in human epithelial ovarian carcinoma and their regulation by the antiparasite drug ivermectin: data interpretation in the context of 3P medicine. Epma j. 11(4): 661-694. https://doi.org/10.1007/s13167-020-00224-z
Liaghat, M., Yaghoubzad-Maleki, M., Nabi-Afjadi, M., Fathi, Z., Zalpoor, H., Heidari, N., e Bahreini, E. (2024). “A Review of the Potential Role of CoQ10 in the Treatment of Hepatocellular Carcinoma.” Biochem Genet. 62(2): 575-593. https://doi.org/10.1007/s10528-023-10490-x
Liao, J., Liu, P. P., Hou, G., Shao, J., Yang, J., Liu, K., Lu, W., Wen, S., Hu, Y., e Huang, P. (2017). “Regulation of stem-like cancer cells by glutamine through β-catenin pathway mediated by redox signaling.” Molecular Cancer. 16(1): 51. https://doi.org/10.1186/s12943-017-0623-x
Lin, L. C., Que, J., Lin, L. K., e Lin, F. C. (2006). Zinc supplementation to improve mucositis and dermatitis in patients after radiotherapy for head-and-neck cancers: a double-blind, randomized study. Int J Radiat Oncol Biol Phys. 65(3): 745-750. https://doi.org/10.1016/j.ijrobp.2006.01.015
Liu, C., Wu, X., Vulugundam, G., Gokulnath, P., Li, G., e Xiao, J. (2023). “Exercise Promotes Tissue Regeneration: Mechanisms Involved and Therapeutic Scope.” Sports Med Open. 9(1): 27. https://doi.org/10.1186/s40798-023-00573-9
Liu, J., Zhang, K., Cheng, L., Zhu, H., e Xu, T. (2020). “Progress in Understanding the Molecular Mechanisms Underlying the Antitumour Effects of Ivermectin.” Drug Des Devel Ther. 14: 285-296. https://doi.org/10.2147/dddt.s237393
Liu, X., Ye, N., Xiao, C., Wang, X., Li, S., Deng, Y., Yang, X., Li, Z., e Yang, X. (2021). “Hyperbaric oxygen regulates tumor microenvironment and boosts commercialized nanomedicine delivery for potent eradication of cancer stem-like cells.” Nano Today. 40: 101248. https://doi.org/10.1016/j.nantod.2021.101248
Liu, Y., Sun, Y., Guo, Y., Shi, X., Chen, X., Feng, W., Wu, L. L., Zhang, J., Yu, S., Wang, Y., e Shi, Y. (2023). “An Overview: The Diversified Role of Mitochondria in Cancer Metabolism.” Int J Biol Sci. 19(3): 897-915. https://doi.org/10.7150/ijbs.81609
Long, Y., Qiu, J., Zhang, B., He, P., Shi, X., He, Q., Chen, Z., Shen, W., Li, Z., e Zhang, X. (2021). “Pharmacological Vitamin C Treatment Impedes the Growth of Endogenous Glutamine-Dependent Cancers by Targeting Glutamine Synthetase.” Front Pharmacol. 12: 671902. https://doi.org/10.3389/fphar.2021.671902
Lu, H., Cai, L., Mu, L. N., Lu, Q. Y., Zhao, J., Cui, Y., Sul, J. H., Zhou, X. F., Ding, B. G., Elashoff, R. M., Marshall, J., Yu, S. Z., Jiang, Q. W., e Zhang, Z. F. (2006). “Dietary mineral and trace element intake and squamous cell carcinoma of the esophagus in a Chinese population.” Nutr Cancer. 55(1): 63-70. https://doi.org/10.1207/s15327914nc5501_8
Luo, X., Ng, C., He, J., Yang, M., Luo, X., Herbert, T. P., e Whitehead, J. P. (2022). “Vitamin C protects against hypoxia, inflammation, and ER stress in primary human preadipocytes and adipocytes.” Molecular and Cellular Endocrinology. 556: 111740. https://doi.org/10.1016/j.mce.2022.111740
Lv, H., Wang, C., Fang, T., Li, T., Lv, G., Han, Q., Wang, H. (2018). Vitamin C preferentially kills cancer stem cells in hepatocellular carcinoma via SVCT-2. NPJ Precis Oncol. 2(1): 1. https://doi.org/10.1038/s41698-017-0044-8
Lytle, N. K., Barber, A. G. e Reya, T. (2018). “Stem cell fate in cancer growth, progression and therapy resistance.” Nature Reviews Cancer. 18(11): 669-680. https://doi.org/10.1038/s41568-018-0056-x
Ma, Z., Yang, M., Foda, M. F., Zhang, K., Li, S., Liang, H., Zhao, Y., e Han, H. (2022). “Polarization of Tumor-Associated Macrophages Promoted by Vitamin C-Loaded Liposomes for Cancer Immunotherapy.” ACS Nano. 16(10): 17389-17401. https://doi.org/10.1021/acsnano.2c08446
Mansoori, S., Fryknäs, M., Alvfors, C., Loskog, A., Larsson, R., e Nygren, P. (2021). “A phase 2a clinical study on the safety and efficacy of individualized dosed mebendazole in patients with advanced gastrointestinal cancer.” Sci Rep. 11(1): 8981. https://doi.org/10.1038/s41598-021-88433-y
Marigoudar, J. B., Sarkar, D., Yuguda, Y. M., Abutayeh, R. F., Kaur, A., Pati, A., Mitra, D., Ghosh, A., Banerjee, D., Borah, S., Barman, K., Das, B., Khairnar, S. J., Šeherčehajić, E., e Kumar, S. (2022). “Role of vitamin D in targeting cancer and cancer stem cell populations and its therapeutic implications.” Med Oncol. 40(1): 2. https://doi.org/10.1007/s12032-022-01855-0
Martinez, P., Baghli, I., Gourjon, G., e Seyfried, T. N. (2024). “Mitochondrial-Stem Cell Connection: Providing Additional Explanations for Understanding Cancer.” Metabolites. 14(4). https://doi.org/10.3390/metabo14040229
Mashhadi, M., Bakhshipour, A., Zakeri, Z. e Ansari-Moghaddam, A. (2016). “Reference Range for Zinc Level in Young Healthy Population in Southeast of Iran.” Health Scope. https://doi.org/10.17795/jhealthscope-18181
Mathews, E. H., Stander, B. A., Joubert, A. M., e Liebenberg, L. (2014). “Tumor cell culture survival following glucose and glutamine deprivation at typical physiological concentrations.” Nutrition. 30(2): 218-227. https://doi.org/10.1016/j.nut.2013.07.024
Matta Reddy, A., Iqbal, M., Chopra, H., Urmi, S., Junapudi, S., Bibi, S., Kumar Gupta, S., Nirmala Pangi, V., Singh, I., e Abdel-Daim, M. M. (2022). “Pivotal role of vitamin D in mitochondrial health, cardiac function, and human reproduction.” Excli j. 21: 967-990. https://doi.org/10.17179/excli2022-4935
McCullough, P. J., Lehrer, D. S., e Amend, J. (2019). Daily oral dosing of vitamin D3 using 5000 TO 50,000 international units a day in long-term hospitalized patients: Insights from a seven year experience. J Steroid Biochem Mol Biol. 189: 228-239. https://doi.org/10.1016/j.jsbmb.2018.12.010
Medjdoub, A., Merzouk, A., Merzouk, H., e Baghli, I. (2016). “Effects of Vitamin C and NADH on in Vitro Proliferative Function of Human Lymphocytes Exposed to Pesticides (Mancozeb and Metribuzin).” Journal of Food Science and Engineering. 6. https://doi.org/10.17265/2159-5828/2016.03.006
Meidenbauer, J. J., Mukherjee, P., e Seyfried, T. N. (2015). “The glucose ketone index calculator: a simple tool to monitor therapeutic efficacy for metabolic management of brain cancer.” Nutr Metab (Lond). 12: 12. https://doi.org/10.1186/s12986-015-0009-2
Mihaylova, M. M., Cheng, C. W., Cao, A. Q., Tripathi, S., Mana, M. D., Bauer-Rowe, K. E., Abu-Remaileh, M., Clavain, L., Erdemir, A., Lewis, C. A., Freinkman, E., Dickey, A. S., La Spada, A. R., Huang, Y., Bell, G. W., Deshpande, V., Carmeliet, P., Katajisto, P., Sabatini, D. M., e Yilmaz Ö.H. (2018). “Fasting Activates Fatty Acid Oxidation to Enhance Intestinal Stem Cell Function during Homeostasis and Aging.” Cell Stem Cell. 22(5): 769-778.e764. https://doi.org/10.1016/j.stem.2018.04.001
Mikirova, N. (2017). “Ascorbic acid and dehydroascorbic acid concentrations in plasma and peripheral blood mononuclear cells after oral liposomal-encapsulated or intravenous ascorbic acid delivery.” J Orthomol Med. 32
Mocayar Marón, F. J., Ferder, L., Reiter, R. J., e Manucha, W. (2020). “Daily and seasonal mitochondrial protection: Unraveling common possible mechanisms involving vitamin D and melatonin.” J Steroid Biochem Mol Biol. 199: 105595. https://doi.org/10.1016/j.jsbmb.2020.105595
Moen, I. e Stuhr, L. E. (2012). “Hyperbaric oxygen therapy and cancer–a review.” Target Oncol. 7(4): 233-242. https://doi.org/10.1007/s11523-012-0233-x
Moertel, C. G., Fleming, T. R., Creagan, E. T., Rubin, J., O’Connell, M. J., e Ames, M. M. (1985). “High-dose vitamin C versus placebo in the treatment of patients with advanced cancer who have had no prior chemotherapy. A randomized double-blind comparison.” N Engl J Med. 312(3): 137-141. https://doi.org/10.1056/nejm198501173120301
Mohr, S. B., Gorham, E. D., Kim, J., Hofflich, H., Cuomo, R. E., e Garland, C. F. (2015). “Could vitamin D sufficiency improve the survival of colorectal cancer patients?” J Steroid Biochem Mol Biol. 148: 239-244. https://doi.org/10.1016/j.jsbmb.2014.12.010
Mohr, S. B., Gorham, E. D., Kim, J., Hofflich, H., e Garland, C. F. (2014). “Meta-analysis of vitamin D sufficiency for improving survival of patients with breast cancer.” Anticancer Res. 34(3): 1163-1166
Mukherjee, P., Augur, Z. M., Li, M., Hill, C., Greenwood, B., Domin, M. A., Kondakci, G., Narain, N. R., Kiebish, M. A., Bronson, R. T., Arismendi-Morillo, G., Chinopoulos C., e Seyfried, T. N. (2019). “Therapeutic benefit of combining calorie-restricted ketogenic diet and glutamine targeting in late-stage experimental glioblastoma.” Commun Biol. 2: 200. https://doi.org/10.1038/s42003-019-0455-x
Mukherjee, P., Greenwood, B., Aristizabal-Henao, J., Kiebish, M., e Seyfried, T.N. (2023). Ketogenic diet as a metabolic vehicle for enhancing the therapeutic efficacy of mebendazole and devimistat in preclinical pediatric glioma. bioRxiv. https://doi.org/10.1101/2023.06.09.544252
Mukhopadhyay, T., Sasaki, J., Ramesh, R., e Roth, J. A. (2002). “Mebendazole elicits a potent antitumor effect on human cancer cell lines both in vitro and in vivo.” Clin Cancer Res. 8(9): 2963-2969
Mussa, A., Mohd Idris, R. A., Ahmed, N., Ahmad, S., Murtadha, A. H., Tengku Din, C. Y., Yean, C. Y., Wan Abdul Rahman, W. F., Mat Lazim, N., Uskoković, V., Hajissa, K., Mokhtar, N. F., Mohamud, R. e Hassan, R. (2022). “High-Dose Vitamin C for Cancer Therapy.” Pharmaceuticals. 15(6): 711. https://doi.org/10.3390/ph15060711
Muñoz, A., e Grant, W. B. (2022). “Vitamin D and Cancer: An Historical Overview of the Epidemiology and Mechanisms.” Nutrients. 14(7). https://doi.org/10.3390/nu14071448
Nazio, F., Bordi, M., Cianfanelli, V., Locatelli, F., e Cecconi, F. (2019). “Autophagy and cancer stem cells: molecular mechanisms and therapeutic applications.” Cell Death & Differentiation. 26(4): 690-702. https://doi.org/10.1038/s41418-019-0292-y
Nencioni, A., Caffa, I., Cortellino, S., e Longo, V. D. (2018). “Fasting and cancer: molecular mechanisms and clinical application.” Nat Rev Cancer. 18(11): 707-719. https://doi.org/10.1038/s41568-018-0061-0
Ngo, B., Van Riper, J. M., Cantley, L. C., e Yun, J. (2019). “Targeting cancer vulnerabilities with high-dose vitamin C.” Nat Rev Cancer. 19(5): 271-282. https://doi.org/10.1038/s41568-019-0135-7
Nygren, P., e Larsson, R. (2014). “Drug repositioning from bench to bedside: tumour remission by the antihelmintic drug mebendazole in refractory metastatic colon cancer.” Acta Oncol. 53(3): 427-428. https://doi.org/10.3109/0284186x.2013.844359
Olsen, R. R., Mary-Sinclair, M. N., Yin, Z., e Freeman, K. W. (2015). Antagonizing Bcl-2 family members sensitizes neuroblastoma and Ewing’s sarcoma to an inhibitor of glutamine metabolism. PLoS One. 10(1): e0116998. https://doi.org/10.1371/journal.pone.0116998
Park, D., Lee, J. H., e Yoon, S. P. (2022). “Anti-cancer effects of fenbendazole on 5-fluorouracil-resistant colorectal cancer cells.” Korean J Physiol Pharmacol. 26(5): 377-387. https://doi.org/10.4196/kjpp.2022.26.5.377
Park, S., Ahn, S., Shin, Y., Yang, Y. e Yeom, C. H. (2018). “Vitamin C in Cancer: A Metabolomics Perspective.” Front Physiol. 9: 762. https://doi.org/10.3389/fphys.2018.00762
Pastò, A., Bellio, C., Pilotto, G., Ciminale, V., Silic-Benussi, M., Guzzo, G., Rasola, A., Frasson, C., Nardo, G., Zulato, E., Nicoletto, M. O., Manicone, M., Indraccolo, S., e Amadori, A. (2014). “Cancer stem cells from epithelial ovarian cancer patients privilege oxidative phosphorylation, and resist glucose deprivation.” Oncotarget. 5(12): 4305-4319. https://doi.org/10.18632/oncotarget.2010
Pedersen, P. L. (1978). Tumor mitochondria and the bioenergetics of cancer cells. Prog Exp Tumor Res. 22: 190-274. https://doi.org/10.1159/000401202
Persi, E., Duran-Frigola, M., Damaghi, M., Roush, W. R., Aloy, P., Cleveland, J. L., Gillies, R. J., e Ruppin, E. (2018). “Systems analysis of intracellular pH vulnerabilities for cancer therapy.” Nat Commun. 9(1): 2997. https://doi.org/10.1038/s41467-018-05261-x
Phillips, M. C. L., Leyden, J., McManus, E. J., Lowyim, D. G., Ziad, F., Moon, B. G., Haji Mohd Yasin, N. A. B., Tan, A., Thotathil, Z., e Jameson, M. B. (2022). “Feasibility and Safety of a Combined Metabolic Strategy in Glioblastoma Multiforme: A Prospective Case Series.” J Oncol. 2022: 4496734. https://doi.org/10.1155/2022/4496734
Pinto, L. C., Soares, B. M., Pinheiro Jde, J., Riggins, G. J., Assumpção, P. P., Burbano, R. M., e Montenegro, R. C. (2015). The anthelmintic drug mebendazole inhibits growth, migration and invasion in gastric cancer cell model. Toxicol In Vitro. 29(8): 2038-2044. https://doi.org/10.1016/j.tiv.2015.08.007
Poff, A., Koutnik, A. P., Egan, K. M., Sahebjam, S., D’Agostino, D.P., e Kumar, N. B. (2019). “Targeting the Warburg effect for cancer treatment: Ketogenic diets for management of glioma.” Semin Cancer Biol. 56: 135-148. https://doi.org/10.1016/j.semcancer.2017.12.011
Poff, A. M., Ari, C., Arnold, P., Seyfried, T. N., e D’Agostino, D. P. (2014). “Ketone supplementation decreases tumor cell viability and prolongs survival of mice with metastatic cancer.” Int J Cancer. 135(7): 1711-1720. https://doi.org/10.1002/ijc.28809
Poff, A. M., Kernagis, D., e D’Agostino, D. P. (2016). “Hyperbaric Environment: Oxygen and Cellular Damage versus Protection.” Compr Physiol. 7(1): 213-234. https://doi.org/10.1002/cphy.c150032
Poff, A. M., Ward, N., Seyfried, T. N., Arnold, P., e D’Agostino, D. P. (2015). “Non-Toxic Metabolic Management of Metastatic Cancer in VM Mice: Novel Combination of Ketogenic Diet, Ketone Supplementation, and Hyperbaric Oxygen Therapy.” PLoS One. 10(6): e0127407. https://doi.org/10.1371/journal.pone.0127407
Polireddy, K., Dong, R., Reed, G., Yu, J., Chen, P., Williamson, S., Chen, Q. (2017). High Dose Parenteral Ascorbate Inhibited Pancreatic Cancer Growth and Metastasis: Mechanisms and a Phase I/IIa study. Sci Rep. 7(1): 17188. https://doi.org/10.1038/s41598-017-17568-8
Praharaj, P. P., Patro, B. S., e Bhutia, S. K. (2022). “Dysregulation of mitophagy and mitochondrial homeostasis in cancer stem cells: Novel mechanism for anti-cancer stem cell-targeted cancer therapy.” British Journal of Pharmacology. 179(22): 5015-5035. https://doi.org/10.1111/bph.15401
Quigley, M., Rieger, S., Capobianco, E., Wang, Z., Zhao, H., Hewison, M., e Lisse, T. S. (2022). “Vitamin D Modulation of Mitochondrial Oxidative Metabolism and mTOR Enforces Stress Adaptations and Anticancer Responses.” JBMR Plus. 6(1): e10572. https://doi.org/10.1002/jbm4.10572
Rais, R., Lemberg, K. M., Tenora, L., Arwood, M. L., Pal, A., Alt, J., Wu, Y., Lam, J., Aguilar, J. M. H., Zhao, L., Peters, D. E., Tallon, C., Pandey, R., Thomas, A. G., Dash, R. P., Seiwert, T., Majer, P., Leone, R. D., Powell, J. D., e Slusher, B. S. (2022). “Discovery of DRP-104, a tumor-targeted metabolic inhibitor prodrug.” Sci Adv. 8(46): eabq5925. https://doi.org/10.1126/sciadv.abq5925
Riordan, H. D., Riordan, N. H., Jackson, J. A., Casciari, J. J., Hunninghake, R., González, M. J., Mora, E. M., Miranda-Massari, J. R., Rosario, N., e Rivera, A. (2004). “Intravenous vitamin C as a chemotherapy agent: a report on clinical cases.” P R Health Sci J. 23(2): 115-118
Riordan, N., Riordan, H., e Casciari, J. (2000). “Clinical and experimental experiences with intravenous vitamin c.” J Orthomol Med. 15: 13
Roa, F. J., Peña, E., Gatica, M., Escobar-Acuña, K., Saavedra, P., Maldonado, M., Cuevas, M. E., Moraga-Cid, G., Rivas, C. I., e Muñoz-Montesino, C. (2020). “Therapeutic Use of Vitamin C in Cancer: Physiological Considerations.” Front Pharmacol. 11: 211. https://doi.org/10.3389/fphar.2020.00211
Satheesh, N. J., Samuel, S. M., e Büsselberg, D. (2020). “Combination Therapy with Vitamin C Could Eradicate Cancer Stem Cells.” Biomolecules. 10(1). https://doi.org/10.3390/biom10010079
Schmit, J. (2013). In vitro anti-cancer effects of benzimidazoles on the canine osteosarcoma D17 cell line. University of Illinois at Urbana-Champaign. http://hdl.handle.net/2142/45401
Sebastian, J. P., Hugh, D. R., Stephen, M. H., Arie, K., Hoffer, L. J., e Mark, L. (2006). “Intravenously administered vitamin C as cancer therapy: three cases.” Canadian Medical Association Journal. 174(7): 937. https://doi.org/10.1503/cmaj.050346
Seraphin, G., Rieger, S., Hewison, M., Capobianco, E., e Lisse, T. S. (2023). “The impact of vitamin D on cancer: A mini review.” J Steroid Biochem Mol Biol. 231: 106308. https://doi.org/10.1016/j.jsbmb.2023.106308
Seyfried, T. N., Arismendi-Morillo, G., Mukherjee, P., e Chinopoulos, C. (2020). “On the Origin of ATP Synthesis in Cancer.” iScience. 23(11): 101761. https://doi.org/10.1016/j.isci.2020.101761
Seyfried, T. N., e Chinopoulos, C. (2021). “Can the Mitochondrial Metabolic Theory Explain Better the Origin and Management of Cancer than Can the Somatic Mutation Theory?” Metabolites. 11(9). https://doi.org/10.3390/metabo11090572
Seyfried, T. N., Flores, R. E., Poff, A. M., e D’Agostino, D. P. (2014). “Cancer as a metabolic disease: implications for novel therapeutics.” Carcinogenesis. 35(3): 515-527. https://doi.org/10.1093/carcin/bgt480
Seyfried, T. N., e Huysentruyt, L. C. (2013). “On the origin of cancer metastasis.” Crit Rev Oncog. 18(1-2): 43-73. https://doi.org/10.1615/critrevoncog.v18.i1-2.40
Seyfried, T. N., Shivane, A. G., Kalamian, M., Maroon, J. C., Mukherjee, P., e Zuccoli, G. (2021). “Ketogenic Metabolic Therapy, Without Chemo or Radiation, for the Long-Term Management of IDH1-Mutant Glioblastoma: An 80-Month Follow-Up Case Report.” Front Nutr. 8: 682243. https://doi.org/10.3389/fnut.2021.682243
Seyfried, T. N., Yu, G., Maroon, J. C., e D’Agostino, D. P. (2017). “Press-pulse: a novel therapeutic strategy for the metabolic management of cancer.” Nutr Metab (Lond). 14: 19. https://doi.org/10.1186/s12986-017-0178-2
Sharmeen, S., Skrtic, M., Sukhai, M. A., Hurren, R., Gronda, M., Wang, X., Schimmer, A. D. (2010). The antiparasitic agent ivermectin induces chloride-dependent membrane hyperpolarization and cell death in leukemia cells. Blood. 116(18): 3593-3603. https://doi.org/10.1182/blood-2010-01-262675
Sheeley, M. P., Andolino, C., Kiesel, V. A., e Teegarden, D. (2022). “Vitamin D regulation of energy metabolism in cancer.” Br J Pharmacol. 179(12): 2890-2905. https://doi.org/10.1111/bph.15424
Shelton, L. M., Huysentruyt, L. C., e Seyfried, T. N. (2010). “Glutamine targeting inhibits systemic metastasis in the VM-M3 murine tumor model.” Int J Cancer. 127(10): 2478-2485. https://doi.org/10.1002/ijc.25431
Sia, J., Szmyd, R., Hau, E., e Gee, H. E. (2020). “Molecular Mechanisms of Radiation-Induced Cancer Cell Death: A Primer.” Front Cell Dev Biol. 8: 41. https://doi.org/10.3389/fcell.2020.00041
Son, D. S., Lee, E. S., e Adunyah, S. E. (2020). “The Antitumor Potentials of Benzimidazole Anthelmintics as Repurposing Drugs.” Immune Netw. 20(4): e29. https://doi.org/10.4110/in.2020.20.e29
Song, B., Park, E. Y., Kim, K. J., e Ki, S. H. (2022). “Repurposing of Benzimidazole Anthelmintic Drugs as Cancer Therapeutics.” Cancers (Basel). 14(19). https://doi.org/10.3390/cancers14194601
Soto, A. M., e Sonnenschein, C. (2011). “The tissue organization field theory of cancer: a testable replacement for the somatic mutation theory.” Bioessays. 33(5): 332-340. https://doi.org/10.1002/bies.201100025
Sugimoto, R., Lee, L., Tanaka, Y., Morita, Y., Hijioka, M., Hisano, T., e Furukawa, M. (2024). “Zinc Deficiency as a General Feature of Cancer: a Review of the Literature.” Biol Trace Elem Res. 202(5): 1937-1947. https://doi.org/10.1007/s12011-023-03818-6
Suwannasom, N., Kao, I., Pruß, A., Georgieva, R., e Bäumler, H. (2020). “Riboflavin: The Health Benefits of a Forgotten Natural Vitamin.” Int J Mol Sci. 21(3). https://doi.org/10.3390/ijms21030950
Tamai, Y., Iwasa, M., Eguchi, A., Shigefuku, R., Sugimoto, K., Hasegawa, H., e Takei, Y. (2020). “Serum copper, zinc and metallothionein serve as potential biomarkers for hepatocellular carcinoma.” PLoS One. 15(8): e0237370. https://doi.org/10.1371/journal.pone.0237370
Tang, M., Hu, X., Wang, Y., Yao, X., Zhang, W., Yu, C., Cheng, F., Li, J., e Fang, Q. (2021). “Ivermectin, a potential anticancer drug derived from an antiparasitic drug.” Pharmacol Res. 163: 105207. https://doi.org/10.1016/j.phrs.2020.105207
Tiwari, S., Sapkota, N., e Han, Z. (2022). “Effect of fasting on cancer: A narrative review of scientific evidence.” Cancer Sci. 113(10): 3291-3302. https://doi.org/10.1111/cas.15492
Trump, D. L. (2018). “Calcitriol and cancer therapy: A missed opportunity.” Bone Rep. 9: 110-119. https://doi.org/10.1016/j.bonr.2018.06.002
van den Boogaard, W. M. C., Komninos, D. S. J., e Vermeij, W. P. (2022). “Chemotherapy Side-Effects: Not All DNA Damage Is Equal.” Cancers (Basel). 14(3). https://doi.org/10.3390/cancers14030627
Vidal. 2024. https://www.vidal.fr/medicaments.html
Vuda, M., e Kamath, A. (2016). “Drug induced mitochondrial dysfunction: Mechanisms and adverse clinical consequences.” Mitochondrion. 31: 63-74. https://doi.org/10.1016/j.mito.2016.10.005
Wan, J., Zhou, J., Fu, L., Li, Y., Zeng, H., Xu, X., Lv, C., e Jin, H. (2021). “Ascorbic Acid Inhibits Liver Cancer Growth and Metastasis in vitro and in vivo, Independent of Stemness Gene Regulation.” Front Pharmacol. 12: 726015. https://doi.org/10.3389/fphar.2021.726015
Wang, F., He, M. M., Wang, Z. X., Li, S., Jin, Y., Ren, C., Xu, R. H. (2019). Phase I study of high-dose ascorbic acid with mFOLFOX6 or FOLFIRI in patients with metastatic colorectal cancer or gastric cancer. BMC Cancer. 19(1): 460. https://doi.org/10.1186/s12885-019-5696-z
Wang, G., Yin, T., e Wang, Y. (2016). In vitro and in vivo assessment of high-dose vitamin C against murine tumors. Exp Ther Med. 12(5): 3058-3062. https://doi.org/10.3892/etm.2016.3707
Wang, J., Xu, Y., Wan, H., e Hu, J. (2018). Antibiotic ivermectin selectively induces apoptosis in chronic myeloid leukemia through inducing mitochondrial dysfunction and oxidative stress. Biochem Biophys Res Commun. 497(1): 241-247. https://doi.org/10.1016/j.bbrc.2018.02.063
Wang, Q., e Zhou, W. (2021). “Roles and molecular mechanisms of physical exercise in cancer prevention and treatment.” J Sport Health Sci. 10(2): 201-210. https://doi.org/10.1016/j.jshs.2020.07.008
Wang, Y., Sun, Z., Li, A., e Zhang, Y. (2019). “Association between serum zinc levels and lung cancer: a meta-analysis of observational studies.” World J Surg Oncol. 17(1): 78. https://doi.org/10.1186/s12957-019-1617-5
Ward, N. P., Poff, A. M., Koutnik, A. P., e D’Agostino, D. P. (2017). “Complex I inhibition augments dichloroacetate cytotoxicity through enhancing oxidative stress in VM-M3 glioblastoma cells.” PLoS One. 12(6): e0180061. https://doi.org/10.1371/journal.pone.0180061
Weber, D. D., Aminzadeh-Gohari, S., e Kofler, B. (2018). Ketogenic diet in cancer therapy. Aging (Albany NY). 10: 164-165
Weber, D. D., Aminzadeh-Gohari, S., Tulipan, J., Catalano, L., Feichtinger, R. G., e Kofler, B. (2020). “Ketogenic diet in the treatment of cancer – Where do we stand?” Mol Metab. 33: 102-121. https://doi.org/10.1016/j.molmet.2019.06.026
Wei, Q., Qian, Y., Yu, J., e Wong, C. C. (2020). “Metabolic rewiring in the promotion of cancer metastasis: mechanisms and therapeutic implications.” Oncogene. 39(39): 6139-6156. https://doi.org/10.1038/s41388-020-01432-7
Woolf, E. C., Syed, N., e Scheck, A. C. (2016). “Tumor Metabolism, the Ketogenic Diet and β-Hydroxybutyrate: Novel Approaches to Adjuvant Brain Tumor Therapy.” Front Mol Neurosci. 9: 122. https://doi.org/10.3389/fnmol.2016.00122
Wu, S., Zhang, K., Liang, Y., Wei, Y., An, J., Wang, Y., Yang, J., Zhang, H., Zhang, Z., Liu, J., e Shi, J. (2022). “Nano-enabled Tumor Systematic Energy Exhaustion via Zinc (II) Interference Mediated Glycolysis Inhibition and Specific GLUT1 Depletion.” Adv Sci (Weinh). 9(7): e2103534. https://doi.org/10.1002/advs.202103534
Wu, X., Hu, W., Lu, L., Zhao, Y., Zhou, Y., Xiao, Z., Zhang, L., Zhang, H., Li, X., Li, W., Wang, S., Cho, C. H., Shen, J., e Li, M. (2019). “Repurposing vitamin D for treatment of human malignancies via targeting tumor microenvironment.” Acta Pharm Sin B. 9(2): 203-219. https://doi.org/10.1016/j.apsb.2018.09.002
Wu, X., Tang, J., e Xie, M. (2015). “Serum and hair zinc levels in breast cancer: a meta-analysis.” Sci Rep. 5: 12249. https://doi.org/10.1038/srep12249
Xiong, Y., Yong, Z., Xu, C., Deng, Q., Wang, Q., Li, S., Wang, C., Zhang, Z., Yang, X., e Li, Z. (2023). “Hyperbaric Oxygen Activates Enzyme-Driven Cascade Reactions for Cooperative Cancer Therapy and Cancer Stem Cells Elimination.” Adv Sci (Weinh). 10(21): e2301278. https://doi.org/10.1002/advs.202301278
Xu, C., Yang, H. L., Yang, Y. K., Pan, L., e Chen, H. Y. (2022). “Zinc-finger protein 750 mitigates malignant biological behavior of oral CSC-like cells enriched from parental CAL-27 cells.” Oncol Lett. 23(1): 28. https://doi.org/10.3892/ol.2021.13146
Xv, F., Chen, J., Duan, L., e Li, S. (2018). “Research progress on the anti-cancer effects of vitamin K2.” Oncol Lett. 15(6): 8926-8934. https://doi.org/10.3892/ol.2018.8502
Yang, X., Wang, H., Huang, C., He, X., Xu, W., Luo, Y., e Huang, K. (2017). “Zinc enhances the cellular energy supply to improve cell motility and restore impaired energetic metabolism in a toxic environment induced by OTA.” Scientific Reports. 7(1): 14669. https://doi.org/10.1038/s41598-017-14868-x
Ye, H., Wu, K., Liu, Y., Zhu, Y., Luo, H., e Zou, W. (2022). “Zinc oxide nanoparticle attenuates chemotherapy resistance by inducing cell stemness progression of colorectal cancer via miR-1321/HIF-2α axis.” Arabian Journal of Chemistry. 15(7): 103938. https://doi.org/10.1016/j.arabjc.2022.103938
Yokokawa, H., Fukuda, H., Saita, M., Miyagami, T., Takahashi, Y., Hisaoka, T., e Naito, T. (2020). “Serum zinc concentrations and characteristics of zinc deficiency/marginal deficiency among Japanese subjects.” J Gen Fam Med. 21(6): 248-255. https://doi.org/10.1002/jgf2.377
Yousef, R. G., Elwan, A., Gobaara, I. M. M., Mehany, A. B. M., Eldehna, W. M., El-Metwally, S. A., A Alsfouk, B., Elkaeed, E. B., Metwaly, A. M., e Eissa, I. H. (2022). “Anti-cancer and immunomodulatory evaluation of new nicotinamide derivatives as potential VEGFR-2 inhibitors and apoptosis inducers: in vitro and in silico studies.” J Enzyme Inhib Med Chem. 37(1): 2206-2222. https://doi.org/10.1080/14756366.2022.2110868
Yu, C., Min, S., Lv, F., Ren, L., Yang, Y., e Chen, L. (2023). “Vitamin C inhibits the growth of colorectal cancer cell HCT116 and reverses the glucose-induced oncogenic effect by downregulating the Warburg effect.” Med Oncol. 40(10): 297. https://doi.org/10.1007/s12032-023-02155-x
Zeng, X., Dong, X., Xiao, Q., e Yao, J. (2022). “Vitamin C Inhibits Ubiquitination of Glutamate Transporter 1 (GLT-1) in Astrocytes by Downregulating HECTD1.” ACS Chem Neurosci. 13(5): 676-687. https://doi.org/10.1021/acschemneuro.1c00845
Zhang, C., e Le, A. (2021). “Diabetes and Cancer: The Epidemiological and Metabolic Associations.” Adv Exp Med Biol. 1311: 217-227. https://doi.org/10.1007/978-3-030-65768-0_16
Zhang, G., Sheng, M., Wang, J., Teng, T., Sun, Y., Yang, Q., e Xu, Z. (2018). “Zinc improves mitochondrial respiratory function and prevents mitochondrial ROS generation at reperfusion by phosphorylating STAT3 at Ser(727).” J Mol Cell Cardiol. 118: 169-182. https://doi.org/10.1016/j.yjmcc.2018.03.019
Zhang, P., Li, Y., Xu, W., Cheng, J., Zhang, C., Gao, J., Li, Z., Tao, L., e Zhang, Y. (2022). “Immunotoxicity induced by Ivermectin is associated with NF-κB signaling pathway on macrophages.” Chemosphere. 289:133087. https://doi.org/10.1016/j.chemosphere.2021.133087
Zheng, X. X., Chen, J. J., Sun, Y. B., Chen, T. Q., Wang, J., e Yu, S. C. (2023). “Mitochondria in cancer stem cells: Achilles heel or hard armor.” Trends Cell Biol. 33(8): 708-727. https://doi.org/10.1016/j.tcb.2023.03.009
Zhou, H.-M., Zhang, J.-G., Zhang, X., e Li, Q. (2021). “Targeting cancer stem cells for reversing therapy resistance: mechanism, signaling, and prospective agents.” Signal Transduction and Targeted Therapy. 6(1): 62. https://doi.org/10.1038/s41392-020-00430-1
Zhou, X., Zheng, W., Nagana Gowda, G. A., Raftery, D., Donkin, S. S., Bequette, B., e Teegarden, D. (2016). “1,25-Dihydroxyvitamin D inhibits glutamine metabolism in Harvey-ras transformed MCF10A human breast epithelial cell.” J Steroid Biochem Mol Biol. 163: 147-156. https://doi.org/10.1016/j.jsbmb.2016.04.022
Zuccoli, G., Marcello, N., Pisanello, A., Servadei, F., Vaccaro, S., Mukherjee, P., e Seyfried, T. N. (2010). “Metabolic management of glioblastoma multiforme using standard therapy together with a restricted ketogenic diet: Case Report.” Nutr Metab (Lond). 7: 33. https://doi.org/10.1186/1743-7075-7-33
REFERENCES Abraham, A., Kattoor, A. J., Saldeen T., and Mehta, J. L. (2019). “Vitamin E and its anticancer effects.” Crit Rev Food Sci Nutr. 59(17): 2831-2838. https://doi.org/10.1080/10408398.2018.1474169. Adams, J. M., and Strasser, A. (2008). “Is tumor growth sustained by rare cancer stem cells or dominant clones?” Cancer Res. 68(11): 4018-4021. https://doi.org/10.1158/0008-5472.can-07-6334. Adapa, S. R., Hunter, G. A., Amin, N. E., Marinescu, C., Borsky, A., Sagatys, E. M., Sebti, S. M., Reuther, G. W., Ferreira, G. C., and Jiang, R. H. (2024). “Porphyrin overdrive rewires cancer cell metabolism.” Life Sci Alliance. 7(7). https://doi.org/10.26508/lsa.202302547
SCARICA GRATUITAMENTE LO STUDIO IN INGLESE
EFFETTA UNA DONAZIONE UNA TANTUM
EFFETTUA UNA DONAZIONE MENSILE
EFFETTUA UNA DONAZIONE ANNUALE
Scegli un importo
O inserisci un importo personalizzato
Il Vostro Contributo e’ molto apprezzato e ci consente di sviluppare sempre nuovi approfondimenti
Your contribution is appreciated.
Your contribution is appreciated.
Dona ORADona ORADona ORA